聚丙烯酰胺凝胶垂直板电泳分析过氧化物酶同工酶实验报告
班级:植物092 姓名:徐炜佳 学号:0901080223
聚丙烯酰胺凝胶垂直板电泳分析过氧化物酶同工酶
研究背景及目的
带电颗粒在电场作用下向着与其电性相反的电极移动,称为电泳(electrophoresis,简称EP )。1937年瑞典科学家Tiselius建立了“移界电泳法(moving boundary EP)”,成功地将血清蛋白质分成清蛋白、α1、α2、β和γ球蛋白5个主要成分,由于他的突出贡献,1948年荣获诺贝尔奖金。50年代,许多科学家着手改进电泳仪,寻找合适的电泳支持介质,先后找到滤纸、醋酸纤维素薄膜、淀粉及琼脂作为支持物。60年代,Davis等科学家利用聚丙烯酰胺凝胶作为电泳支持物,在此基础上发展了SDS-聚丙烯酰胺凝胶电泳、等电聚焦电泳、双向电泳和印迹转移电泳等技术。这些技术具有设备简单,操作方便,分辨率高等优点。目前,电泳技术已成为生物化学与分子生物学以及与其密切相关的医学、农、林、牧、鱼、制药、某些工业 分析中必不可少的手段。
同工酶是指能催化同一种化学反应, 但其酶蛋白本身的分子结构组成却有所不同的一组酶。它们是DNA 编码的遗传信息表达的结果。最近的研究表明,同工酶与生物的遗传、生长发、代谢调节及抗性等都有一定的关系。因此,测定同工酶在理论上和实践上都有重要的意义。用聚丙烯酰胺凝胶电泳测定同工酶,方法简便、灵敏度高,重现性强,测定结果便于观察、记录和保存。过氧化物酶是植物体内普遍存在的、活性较高的一种酶。它与呼吸作用、光合作用及生长素的氧化等都有关系。在植物生长发育过程中它的活性不断发生变化。因此,测定这种酶的活性或其同工酶的变化情况,可以反映某一时期植物体内代谢的变化。本实验采用聚丙烯酰胺凝胶垂直板电泳技术,分离小麦幼苗过氧化物酶同工酶,根据酶的生物化学反映,通过染色方法显示出酶的不同区带,以鉴定小麦幼苗过氧化物酶同工酶。通过本实验,主要要掌握电泳技术的原理、方法、设计、装置、凝胶配制等问题,熟悉所有的操作过程,另外,对同工酶有一个感性的认识。
实验原理
不连续聚丙烯酰胺凝胶电泳的原理
系统的不连续性表现在以下几个方面:
(1)凝胶板由上、下两层胶组成,两层凝胶的孔径不同。上层为大孔径的浓缩胶,下层为小孔径的分离胶。
(2)缓冲液离子组成及各层凝胶的pH不同。本实验采用碱性系统。电极缓冲液为pH8.3的Tris-甘氨酸缓冲液,浓缩胶为pH6.7的Tris-HCl缓冲液。而分离胶为pH8.9的Tris-HCl缓冲液。
(3)在电场中形成不连续的电位梯度。在这样一个不连续的系统里,存在三种物理效应,即电荷效应、分子筛效应和浓缩效应。在这三种效应的共同作用下,待测物质被很好地分离开来。
下面以本实验要分离的小麦苗过氧化物酶同工酶为例,分别说明三种效应的作用:
(1)电荷效应:各种酶蛋白按其所带电荷的种类及数量,在电场作用下向一定电极,以一定速度泳动。
(2)分子筛效应:分子量小,形状为球形的分子在电泳过程中受到阻力较小,移动较快;反之,分子量大、形状不规则的分子,电泳过程中受到的阻力较大,移动较慢。这种效应与凝胶过滤过程中的情况不同。
(3)浓缩效应:待分离样品中的各组分在浓缩胶中会被压缩成层,而使原来很稀的样品得到高度浓缩。其原因如下:
① 由于两层凝胶孔径不同,酶蛋白向下移动到两层凝胶界面时,阻力突然加大,速度变慢。使得在该界面处的待分离酶蛋白区带变窄,浓度升高。
② 在聚丙烯酰胺凝胶中,虽然浓缩胶和分离胶用的都是Tris-HCl缓冲液,但上层浓缩胶为pH 6.7,下层分离胶为pH 8.9。HCl是强电解质,不管在哪层胶中,HCl几乎都全部电离,Cl-布满整个胶板。待分离的酶蛋白样品加在样品槽中,浸在pH8.3和Tris-甘氨酸缓冲液中。电泳一开始,有效泳动率最大的Cl-迅速跑到最前边,成为快离子(前导离子)。在pH6.7条件下解离度仅有0.1~1%的甘氨酸(pI = 6.0 )有效泳动率最低,跑在最后边,成为慢离子(尾随离子)。这样,快离子和慢离子之间就形成了一个不断移动的界面。在pH6.7条件下带有负电荷的酶蛋白,其有效泳动率介于快慢离子之间,被夹持分布于界面附近,逐渐形成一个区带。由于快离子快速向前移动,在其原来停留的那部分地区成了低离子浓度区,即低电导区。因为电位梯度V、电流强度I和电导率S之间有如下关系:
V=I/S
所以在电流恒定条件下低电导区两侧就产生了较高的电位梯度。这种在电泳开始后产生的高电位梯度作用于酶蛋白和甘氨酸慢离子加速前进,追赶快离子。本来夹在快慢离子之间的酶蛋白区带,在这个追赶中被逐渐地压缩聚集成一条更为狭窄的区带。这就是所谓的浓缩效应。在此区带中,各种酶蛋白又按其电荷而分成不同层次,在进入分离胶前被初步分离,形成若干条离得很近但又不同的“起跑线”。
当酶蛋白和慢离子都进入分离胶后,pH从6.7变为8.9,甘氨酸解离度剧增,有效迁移率迅速加大,从而赶上并超过所有酶蛋白分子。此时,快慢离子的界面跑到被分离的酶蛋白之前,不连续的高电位梯度不再存在。于是,此后的电泳过程中,酶蛋白在一个均一的电位梯度和pH条件下,仅按电荷效应和分子筛效应而被分离。与连续系统相比,不连续系统的分辨率大大提高,因此已成为目前广泛使用的分离分析手段。
过氧化物酶同工酶的鉴定原理
同工酶是来自同一生物不同组织或同一细胞的不同亚细胞结构,能够催化相同反应的蛋白质。同工酶作为基因编码的产物,由于模板作用,酶蛋白质中多肽链上的氨基酸顺序(通过RNA)直接反应了DNA链上碱基对的顺序,其变化能代表DNA分子水平上的变化,所以同工酶分析可解释为是从蛋白质分子水平上研究生物群体遗传分化的有效手段。在生物中酶的表达直接受遗传基因的控制,酶经聚丙烯酰胺凝胶的浓缩、分子筛效应和电泳分离的电荷效应作用下进行分离。从小麦幼苗中提取的粗酶液电泳后,进行酶的特异染色,不同的酶组分显示在凝胶的不同位置而呈现生物特有的同工酶酶谱。
选取小麦为样品的原理
同工酶是基因的直接产物,具有明显的种属、组织和发育阶段特异性。POD同工酶是植物体中常见的氧化酶,它与超氧化物歧化酶(SOD)、过氧化氢酶相互协调配合,清除过剩的自由基,使植物体内的自由基维持在一个动态的正常水平,以提高植物的抗逆性。
小麦在生长发育的后期.植株趋于衰老.子粒成熟,体内自由基及其衍生物的含量不断增加.尤其是SOD氧化自由基的产物过氧化氢的增加需要大量的POD来分解过氧化氢:另一方面,生物发育后期POD活性的增加也可能用来分解叶绿素和生长素,使植株尽早停止生长.减少营养消耗,从而加强植株抵抗自由基及其衍生物和外界不良自然环境造成的伤害。
仪器试剂
1. 实验材料
小麦样液
称取小麦幼苗叶片1 g,放入研钵内,加pH 8.0样品提取液2 mL,于冰水浴中研成匀浆,然后以4 mL提取液分几次洗入离心管,在高速离心机上以8 000r/min离心10min,倒出上清液,以等量40%蔗糖及1/5体积溴酚蓝指示剂混和,留作点样用。
同上操作,再备一份其根部的样品液。
2.仪器
(1)垂直板电泳槽及附件(玻璃板、硅胶条、梳子、导线等)
(2)稳压稳流直流电泳仪
(3)烧杯:250mL×3
(4)移液器
(5)微量进样器(100μL)
(6)大培养皿一套
(7)漏斗
3.试剂
1、2%琼脂:2g琼脂,100mL pH8.9分离胶缓冲液浸泡,用前加热溶化。
2、分离胶缓冲液,pH8.9 (pH8.9 Tris-HCl缓冲液):取48 mL 1mol/L HCl,Tris36.8g,用无离子水溶解后定容至100 mL。
3、浓缩胶缓冲液,pH6.7(pH6.7 Tris-HCl缓冲液):取48 mL 1 mol/L HCl,Tris 5.98g,用无离子水溶解后定容至100 mL。
4、分离胶丙胶贮液(Acr-Bis贮液Ⅱ):Acr 28.0g,Bis 0.735g,用无离子水溶解后定容至100 mL,过滤除去不溶物,装入棕色试剂瓶,4℃保存。
5、浓缩胶丙胶贮液(Acr-Bis贮液Ⅰ):Acr 10g,Bis 2.5g,用无离子水溶解后定容至100 mL,过滤除去不溶物,装入棕色试剂瓶,4℃保存。
6、过硫酸铵溶液:1g过硫酸铵溶于100 mL无离子水中(当天配制)。
7、电极缓冲液,pH8.3(pH8.3 Tris-甘氨酸缓冲液):Tris 6 g,甘氨酸28.8 g,溶于无离子水后定容至1 000 mL,用时稀释10倍。
8、pH4.7乙酸缓冲液:乙酸钠70.52 g,溶于500 mL蒸馏水中再加36 mL冰乙酸,蒸馏水定容至1 000 mL。
9、联大茴香胺染色液:联大茴香胺250 mg溶于140 mL 95%乙醇中,加20 mL蒸馏水,使用前加3%过氧化氢 4~5 mL(当天配制)
10、四甲基乙二胺(TEMED):原液。
实验步骤
1、电泳槽的安装
将两块玻璃板(勿用手指接触玻璃板面,可用手夹住玻璃板的两旁操作)正确放入硅胶条中,夹在电泳槽里,按对角线顺序旋紧螺丝,注意用力均衡以免夹碎玻璃板。安装好电泳槽用pH8.9缓冲液配制的2%琼脂溶液封底,待琼脂凝固后即可灌制凝胶。
2、凝胶的制备
按下表所示配制分离胶

在小烧杯中混匀后,立即灌胶,灌胶时,将电泳槽略微倾斜,用于扶稳,将小烧杯尖端
抵在长玻璃片顶端中央某点,小心估倒入两玻璃片之间,灌至距短玻璃片顶端2厘米左右即可,放平电泳槽,立即用滴管在胶的上层小心轻缓地覆盖约2~3毫米厚的水层;灌注水层时要均匀轻缓,以防在胶顶部产生漏洞,影响结果,刚加水时,可看出界面,后逐渐消失,等到再出现界面时,表明分离胶已聚合,再静置一会儿,便可将水倒出,可用滤纸条从一侧略微吸浸,注意不要碰毁胶面,然后准备灌注浓缩胶。
按下表所示配制浓缩胶

配制均匀后,立即灌胶,操作同分离胶的灌注,当胶面达到距短玻璃片?0.5?厘米左右即可,然后立即插入样品槽模板(梳子)。聚合完成后,在电泳槽内倒入电极缓冲液,然后小心拨出梳子,准备点样。
3、点样
用微量进样品小心吸取样品液加到样品槽内。
上样量:叶片样液和根部样液均以梯度上样:分别为5ul、15ul、30ul
4、电泳
接好电源线(上槽接负极,下槽接正极)。打开电源开关,调节电流,初始时控制在15mA左右,当前沿进入分离胶后,可调节电流到30mA 左右,待前沿指示染料下行至距胶板末端1~2厘米处,即可停止电泳。
5、剥胶、染色及记录结果
垂直板聚丙烯酰胺凝胶电泳结束之后,将垂直板从电泳槽上取下, 小心地将两块玻璃板分开,并小心地将凝胶置于大培养皿中,进行染色反应(样品槽可以去掉)。过氧化物酶在分解过氧化氢的过程中产生自由氧基, 能使联大茴香发生颜色反应,产生褐色的化合物,所以用联大茴香胺染色液浸泡过的凝胶板上,有过氧化物酶同工酶蛋白质带的部位可以看到褐色的谱带。
染色过程如下:
(1)向大培养皿中倒入约50mlpH4.7乙酸缓冲液,将胶板淹没,室温浸泡10分钟。
(2)用漏斗回收乙酸缓冲液,加入联大茴香胺染色液,将胶板淹没,室温下浸泡20分钟,在此期间会出现过氧化物酶同工酶的谱带,观察记录酶谱。
实验结果分析
全模式根部电泳共出现了5条酶带,由上向下可编号为1、2、3、4、5,叶部电泳共出现4条酶带,与根部对比缺少4号酶带。1、2、3号酶带靠近负极,4、5号酶带靠近正极。
对比如下:

总体:小麦幼苗根部同工酶总含量高于叶部,上方的同工酶含量根部少于叶部,下方根部多余叶部。
分析:小麦根部的POD同工酶分子量小,形状更接近球形,主要进行脂肪的β-氧化,产生乙酰辅酶A,经乙醛酸循环,由异柠檬酸裂解为乙醛酸和琥珀酸,加入三羧酸循环
小麦叶部的POD同工酶分子量较大,主要参与光呼吸作用,将光合作用的副产物乙醇酸氧化为乙醛酸和过氧化氢
思考题
1、凝胶的化学聚合与光聚合有何不同?
答:化学聚合的引发剂是过硫酸铵 (NH4)2S2O3(Ammonium persulfate,简写为Ap),催化剂是N,N,N',N'-四甲基乙二胺(Tetramethylenediamine,简写为TEMED)。在催化剂TEMED的作用下,由过硫酸铵(Ap)形成的自由基又使单体形成自由基,从而引起聚合作用。TEMED在低pH时失效,会使聚合作用延迟;冷却也可使聚合速度变慢;一些金属抑制聚合;分子氧阻止链的延长,防碍聚合作用。这些因素在实际操作时都应予以控制。
光聚合以光敏感物核黄素(即VB2)作为催化剂,在痕量氧存在下,核黄素经光解形成无色基,无色基被氧再氧化成自由基,从而引起聚合作用。过量的氧会阻止链长的增加,应避免过量氧的存在。
光聚合形成的凝胶孔径较大,而且随着时间的延长而逐渐变小,不太稳定,所以用它制备大孔径的浓缩胶较为合适。采用化学聚合形成的凝胶孔径较小,而且重复性好,常用来制备分离胶。
2、两个电泳槽中的电极缓冲液用过一次后,是否可以混合后再用?为什么?
答:不能。因为电极缓冲溶液的缓冲能力与组成缓冲溶液的组分浓度和pH值有关,在电泳过程中水会被电离生成氢气和氧气,两个电泳槽的电极缓冲液用过一次后,缓冲液里离子的浓度会增大,造成缓冲液的缓冲能力发生变化,离子强度过大,会影响到蛋白质的活性,使电泳速度减慢,条带不清晰。所以不能混合后再使用。
3、样品中加入40%蔗糖溶液的作用是什么?
答:①增加样品比重,使得样品能够沉到加样孔底部,而不会漂出来,防止样品扩散,从而可以使样品最大限度地跑到胶里去
②防止细菌生长
4、本实验的关键步骤有哪些?为什么?
答:①凝胶的制备:两种胶制备完成后需立即灌胶,因为加入TEMED和过硫酸铵后,胶即刻反应,若不及时灌胶则会导致凝胶凝固不均匀,形成条带形状不规则。覆盖水层时要轻缓,若过猛则会冲撞胶面导致分离起点不一致影响实验结果。灌胶完毕后要立即插入梳子,否则凝胶凝固再插梳子则会毁胶。拔梳子时应垂直向上,均匀用力,缓慢拔出,否则会导致样品槽损毁。总之,若凝胶制备出现问题则直接导致电泳条带不清晰、变形、拖尾等,直接影响实验结果。
②电泳:电泳时应注意正负接线柱的正确连接,矮玻板连接负极,长玻板连接正极,以免样品反方向泳动。电流的调控,接触不良、缓冲液液位太低或者缓冲液离子强度太小导致电阻太大,电流变小.这时如果通过调高电压来使电流增大还可能会烧胶。电流过大、过热也会导致凝胶变性从而达不到分离样品的目的。
参考文献
百度百科:过氧化物酶http://baike.baidu.com/view/1312174.html?wtp=tt
同工酶http://baike.baidu.com/view/83464.htm
《黑木耳菌株酯酶同工酶标记鉴定技术规程》20##-05-14 DB23/T1238-2008
《哲里木畜牧学院学报》 1999年03期 14个品种冬小麦过氧化物酶(POD)同工酶研究
《不同基因型小麦生育后期POD同工酶酶谱分析》 王育水t,权玉萍1,蒋利群2,姚素霞2,姬生栋2 (1.焦作师范高等专科学校.河南焦作454000;2.河南师范大学,河南新乡453007)
《春大豆荚果发育过程中酯酶同工酶酶谱分析》 宫纪娟1 金喜军1 龚振平2 马春梅1
(1东北农业大学农学院,150030,黑龙江哈尔滨;2国家大豆工程技术研究中心,150030,黑龙江哈尔滨)
实验小结
本次实验由于制得的样品槽深度较浅,所以只能完成5ul、15ul、30ul的点样,得到的酶带基本清晰
第二篇:聚丙烯酰胺凝胶垂直板电泳分析过氧化物酶同工酶实验报告
实验六 聚丙烯酰胺凝胶垂直板电泳分析过氧化物酶同工酶
一、研究背景
在生物学中,同工酶可用于研究物种进化、遗传变异、杂交育种和个体发育、组织分化等。动、植物的遗传变异可通过子代和亲代同工酶谱的比较来鉴别。法医学中也可用多种同工酶谱的分析来鉴定亲子关系。细胞杂交或植物杂交育种后是否出现新品种也可用周工酶谱的比较来确定。在个体发育中,从胚胎到出生,再到成年,随着组织的分化和发育,各种同工酶谱也有一个分化转变的过程。在植物的不同发育阶段,同样可见同工酶谱的相应改变。在医学方面,同工酶是研究癌瘤发生的重要手段,癌瘤组织的同工酶谱常发生胚胎化现象,即合成过多的胎儿型同工酶。如果这些变化可反映到血清中,则可利用血清同工酶谱的改变来诊断癌瘤。
所以,测定同工酶在理论上和实践上都有重要的意义。过氧化物酶是植物体内普遍存在的活性较高的一种酶,它与呼吸作用、光合作用以及生长素的氧化等都有关系。在植物生长发育过程中它的活性不断发生变化。因此,测定这种酶的活性或其同工酶的变化情况,可以反映某一时期植物体内代谢的变化。
二、实验原理
1、不连续聚丙烯酰胺凝胶电泳的原理
系统的不连续性表现在以下几个方面:
(1)凝胶板由上、下两层胶组成,两层凝胶的孔径不同。上层为大孔径的浓缩胶,下层为小孔径的分离胶。
(2)缓冲液离子组成及各层凝胶的pH不同。本实验采用碱性系统。电极缓冲液为pH8.3的Tris-甘氨酸缓冲液,浓缩胶为pH6.7的Tris-HCl缓冲液。而分离胶为pH8.9的Tris-HCl缓冲液。
(3)在电场中形成不连续的电位梯度。在这样一个不连续的系统里,存在三种物理效应,即电荷效应、分子筛效应和浓缩效应。在这三种效应的共同作用下,待测物质被很好地分离开来、
以本实验要分离的小麦苗过氧化物酶同工酶为例,分别说明三种效应的作用:
(1)电荷效应:各种酶蛋白按其所带电荷的种类及数量,在电场作用下向一定电极,以一定速度泳动。
(2)分子筛效应:分子量小,形状为球形的分子在电泳过程中受到阻力较小,移动较快;反之,分子量大、形状不规则的分子,电泳过程中受到的阻力较大,移动较慢。这种效应与凝胶过滤过程中的情况不同。
(3)浓缩效应:待分离样品中的各组分在浓缩胶中会被压缩成层,而使原来很稀的样品得到高度浓缩。其原因如下:
① 由于两层凝胶孔径不同,酶蛋白向下移动到两层凝胶界面时,阻力突然加大,速度变慢。使得在该界面处的待分离酶蛋白区带变窄,浓度升高。
② 在聚丙烯酰胺凝胶中,虽然浓缩胶和分离胶用的都是Tris-HCl缓冲液,但上层浓缩胶为pH 6.7,下层分离胶为pH 8.9。HCl是强电解质,不管在哪层胶中,HCl几乎都全部电离,Cl-布满整个胶板。待分离的酶蛋白样品加在样品槽中,浸在pH8.3和Tris-甘氨酸缓冲液中。电泳一开始,有效泳动率最大的Cl-迅速跑到最前边,成为快离子(前导离子)。在pH6.7条件下解离度仅有0.1~1%的甘氨酸(pI = 6.0 )有效泳动率最低,跑在最后边,成为慢离子(尾随离子)。这样,快离子和慢离子之间就形成了一个不断移动的界面。在pH6.7条件下带有负电荷的酶蛋白,其有效泳动率介于快慢离子之间,被夹持分布于界面附近,逐渐形成一个区带。由于快离子快速向前移动,在其原来停留的那部分地区成了低离子浓度区,即低电导区。因为电位梯度V、电流强度I和电导率S之间有如下关系:
V=I/S
所以在电流恒定条件下低电导区两侧就产生了较高的电位梯度。这种在电泳开始后产生的高电位梯度作用于酶蛋白和甘氨酸慢离子加速前进,追赶快离子。本来夹在快慢离子之间的酶蛋白区带,在这个追赶中被逐渐地压缩聚集成一条更为狭窄的区带。这就是所谓的浓缩效应。在此区带中,各种酶蛋白又按其电荷而分成不同层次,在进入分离胶前被初步分离,形成若干条离得很近但又不同的“起跑线”。
当酶蛋白和慢离子都进入分离胶后,pH从6.7变为8.9,甘氨酸解离度剧增,有效迁移率迅速加大,从而赶上并超过所有酶蛋白分子。此时,快慢离子的界面跑到被分离的酶蛋白之前,不连续的高电位梯度不再存在。于是,此后的电泳过程中,酶蛋白在一个均一的电位梯度和pH条件下,仅按电荷效应和分子筛效应而被分离。与连续系统相比,不连续系统的分辨率大大提高,因此已成为目前广泛使用的分离分析手段。
2、过氧化物酶同工酶的鉴定原理
同工酶是来自同一生物不同组织或同一细胞的不同亚细胞结构,能够催化相同反应的蛋白质。同工酶作为基因编码的产物,由于模板作用,酶蛋白质中多肽链上的氨基酸顺序(通过RNA)直接反应了DNA链上碱基对的顺序,其变化能代表DNA分子水平上的变化,所以同工酶分析可解释为是从蛋白质分子水平上研究生物群体遗传分化的有效手段。在生物中酶的表达直接受遗传基因的控制,酶经聚丙烯酰胺凝胶的浓缩、分子筛效应和电泳分离的电荷效应作用下进行分离。从小麦幼苗中提取的粗酶液电泳后,进行酶的特异染色,不同的酶组分显示在凝胶的不同位置而呈现生物特有的同工酶酶谱。
3、选取小麦为样品的原理
同工酶是基因的直接产物,具有明显的种属、组织和发育阶段特异性。POD同工酶是植物体中常见的氧化酶,它与超氧化物歧化酶(SOD)、过氧化氢酶相互协调配合,清除过剩的自由基,使植物体内的自由基维持在一个动态的正常水平,以提高植物的抗逆性。
小麦在生长发育的后期.植株趋于衰老.子粒成熟,体内自由基及其衍生物的含量不断增加.尤其是SOD氧化自由基的产物过氧化氢的增加需要大量的POD来分解过氧化氢:另一方面,生物发育后期POD活性的增加也可能用来分解叶绿素和生长素,使植株尽早停止生长.减少营养消耗,从而加强植株抵抗自由基及其衍生物和外界不良自然环境造成的伤害。
三、仪器与试剂
1.实验材料: 小麦样液
2.仪器
(1)垂直板电泳槽及附件(玻璃板、硅胶条、梳子、导线等)
(2)稳压稳流直流电泳仪:北京市六一仪器厂
(3)微量进样器:上海安亭微量进样器厂
3.试剂

四、实验步骤
1、电泳槽的安装
将两块玻璃板(勿用手指接触玻璃板面,可用手夹住玻璃板的两旁操作)正确放入硅胶条中,夹在电泳槽里,按对角线顺序旋紧螺丝,注意用力均衡以免夹碎玻璃板。安装好电泳槽用pH8.9缓冲液配制的2%琼脂溶液封底,待琼脂凝固后即可灌制凝胶。
2、凝胶的制备
按下表所示配制分离胶

在小烧杯中混匀后,立即灌胶,灌胶时,将电泳槽略微倾斜,用于扶稳,将小烧杯尖端
抵在长玻璃片顶端中央某点,小心估倒入两玻璃片之间,灌至距短玻璃片顶端2厘米左右即可,放平电泳槽,立即用滴管在胶的上层小心轻缓地覆盖约2~3毫米厚的水层;灌注水层时要均匀轻缓,以防在胶顶部产生漏洞,影响结果,刚加水时,可看出界面,后逐渐消失,等到再出现界面时,表明分离胶已聚合,再静置一会儿,便可将水倒出,可用滤纸条从一侧略微吸浸,注意不要碰毁胶面,然后准备灌注浓缩胶。
按下表所示配制浓缩胶

配制均匀后,立即灌胶,操作同分离胶的灌注,当胶面达到距短玻璃片?0.5?厘米左右即可,然后立即插入样品槽模板(梳子)。聚合完成后,在电泳槽内倒入电极缓冲液,然后小心拨出梳子,准备点样。
3、点样
用微量进样品小心吸取样品液加到样品槽内。
上样量:叶片样液和根部样液均以梯度上样:分别为5μl、15μl、30μl,50μl
4、电泳
接好电源线(上槽接负极,下槽接正极)。打开电源开关,调节电流,初始时控制在15mA左右,当前沿进入分离胶后,可调节电流到30mA 左右,待前沿指示染料下行至距胶板末端1~2厘米处,即可停止电泳。
5、剥胶、染色及记录结果
垂直板聚丙烯酰胺凝胶电泳结束之后,将垂直板从电泳槽上取下, 小心地将两块玻璃板分开,并小心地将凝胶置于大培养皿中,进行染色反应(样品槽可以去掉)。过氧化物酶在分解过氧化氢的过程中产生自由氧基, 能使联大茴香发生颜色反应,产生褐色的化合物,所以用联大茴香胺染色液浸泡过的凝胶板上,有过氧化物酶同工酶蛋白质带的部位可以看到褐色的谱带。
染色过程如下:
(1)向大培养皿中倒入约50mlpH4.7乙酸缓冲液,将胶板淹没,室温浸泡6-7分钟。
(2)用漏斗回收乙酸缓冲液,加入联大茴香胺染色液,将胶板淹没,室温下浸泡20分钟,在此期间会出现过氧化物酶同工酶的谱带,观察记录酶谱。
五、结果分析
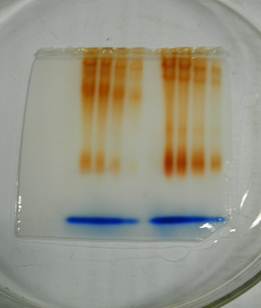

(左侧为叶,右侧为根)
全模式根部电泳共出现了4条酶带,由上向下可编号为1、2、3、4,叶部电泳共出现3条酶带,与根部对比缺少3号酶带。1、2号酶带靠近负极,3号靠近中间,4号酶带靠近正极。
对比如下:

总体:小麦幼苗根部同工酶总含量高于叶部。
分析:小麦根部的POD同工酶分子量小,形状更接近球形,主要进行脂肪的β-氧化,产生乙酰辅酶A,经乙醛酸循环,由异柠檬酸裂解为乙醛酸和琥珀酸,加入三羧酸循环。
小麦叶部的POD同工酶分子量较大,主要参与光呼吸作用,将光合作用的副产物乙醇酸氧化为乙醛酸和过氧化氢。
六、思考题
1、凝胶的化学聚合与光聚合有何不同?
化学聚合的引发剂是过硫酸铵 (NH4)2S2O3(Ammonium persulfate,简写为Ap),催化剂是N,N,N',N'-四甲基乙二胺(Tetramethylenediamine,简写为TEMED)。在催化剂TEMED的作用下,由过硫酸铵(Ap)形成的自由基又使单体形成自由基,从而引起聚合作用。TEMED在低pH时失效,会使聚合作用延迟;冷却也可使聚合速度变慢;一些金属抑制聚合;分子氧阻止链的延长,防碍聚合作用。这些因素在实际操作时都应予以控制。
光聚合以光敏感物核黄素(即VB2)作为催化剂,在痕量氧存在下,核黄素经光解形成无色基,无色基被氧再氧化成自由基,从而引起聚合作用。过量的氧会阻止链长的增加,应避免过量氧的存在。光聚合形成的凝胶孔径较大,而且随着时间的延长而逐渐变小,不太稳定,所以用它制备大孔径的浓缩胶较为合适。采用化学聚合形成的凝胶孔径较小,而且重复性好,常用来制备分离胶。
2、两个电泳槽中的电极缓冲液用过一次后,是否可以混合后再用?为什么?
不能。因为电极缓冲溶液的缓冲能力与组成缓冲溶液的组分浓度和pH值有关,在电泳过程中水会被电离生成氢气和氧气,两个电泳槽的电极缓冲液用过一次后,缓冲液里离子的浓度会增大,造成缓冲液的缓冲能力发生变化,离子强度过大,会影响到蛋白质的活性,使电泳速度减慢,条带不清晰。所以不能混合后再使用。
3、样品中加入40%蔗糖溶液的作用是什么?
①增加样品比重,使得样品能够沉到加样孔底部,而不会漂出来,防止样品扩散,从而可以使样品最大限度地跑到胶里去。
②防止细菌生长
4、本实验的关键步骤有哪些?为什么?
①凝胶的制备:两种胶制备完成后需立即灌胶,因为加入TEMED和过硫酸铵后,胶即刻反应,若不及时灌胶则会导致凝胶凝固不均匀,形成条带形状不规则。覆盖水层时要轻缓,若过猛则会冲撞胶面导致分离起点不一致影响实验结果。灌胶完毕后要立即插入梳子,否则凝胶凝固再插梳子则会毁胶。拔梳子时应垂直向上,均匀用力,缓慢拔出,否则会导致样品槽损毁。总之,若凝胶制备出现问题则直接导致电泳条带不清晰、变形、拖尾等,直接影响实验结果。
②电泳:电泳时应注意正负接线柱的正确连接,矮玻板连接负极,长玻板连接正极,以免样品反方向泳动。电流的调控,接触不良、缓冲液液位太低或者缓冲液离子强度太小导致电阻太大,电流变小.这时如果通过调高电压来使电流增大还可能会烧胶。电流过大、过热也会导致凝胶变性从而达不到分离样品的目的。
七、参考文献
1、百度百科:同工酶http://baike.baidu.com/view/83464.htm
2、《不同基因型小麦生育后期POD同工酶酶谱分析》 王育水t,权玉萍1,蒋利群2,姚素霞2,姬生栋2 (1.焦作师范高等专科学校.河南焦作454000;2.河南师范大学,河南新乡453007)
3、《春大豆荚果发育过程中酯酶同工酶酶谱分析》 宫纪娟1 金喜军1 龚振平2 马春梅1
(1东北农业大学农学院,150030,黑龙江哈尔滨;2国家大豆工程技术研究中心,150030,黑龙江哈尔滨)
八、实验小结
本次实验差点失败。原因在于拧螺丝时拧的过紧,导致拔梳子时拔不出来,用力过大且不均使凝胶被拔起并有些歪斜。放弃了4个用不了的样品槽后剩下8个可以使用。从最终的结果来看,样品槽的歪斜对最后酶带的形态还是有一定的影响。以后做实验时不能太过于紧张了,要把握好度。
-
SDS-聚丙烯酰胺凝胶电泳实验报告
分子生物学实验报告实验名称SDS聚丙烯酰胺凝胶电泳姓名同组人xxx学号xxxx日期SDS聚丙烯酰胺凝胶电泳1引言SDS聚丙烯酰胺凝…
-
实验报告2 SDS-聚丙烯酰胺凝胶电泳法
实验二SDS聚丙烯酰胺凝胶电泳法SDSPAGE测定蛋白质的分子量1原理11聚丙烯酰胺凝胶的性能及制备原理111性能聚丙烯酰胺凝胶的…
-
实验五 聚丙烯酰胺凝胶垂直板电泳分析(实验报告)
实验五聚丙烯酰胺凝胶垂直板电泳分析小麦幼苗过氧化物酶同工酶生物111班杨明轩11020xx128一研究背景及目的过氧化物酶是以过氧…
-
实验5 聚丙烯酰胺凝胶垂直板电泳
生物化学实验实验报告实验五聚丙烯酰胺凝胶垂直板电泳分析小麦幼苗过氧化物酶同工酶生物103班10020xx310赵宁宁搭档10020…
-
聚丙烯酰胺凝胶电泳实验
聚丙烯酰胺凝胶电泳SDS聚丙烯酰胺凝胶电泳SDSPAGE一目的要求1学习电泳原理和技术2学习和掌握SDS聚丙烯酰胺凝胶圆盘电泳分离…
-
SDS-聚丙烯酰胺凝胶电泳实验报告
分子生物学实验报告实验名称SDS聚丙烯酰胺凝胶电泳姓名同组人xxx学号xxxx日期SDS聚丙烯酰胺凝胶电泳1引言SDS聚丙烯酰胺凝…
-
实验报告2 SDS-聚丙烯酰胺凝胶电泳法
实验二SDS聚丙烯酰胺凝胶电泳法SDSPAGE测定蛋白质的分子量1原理11聚丙烯酰胺凝胶的性能及制备原理111性能聚丙烯酰胺凝胶的…
-
SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)实验原理和操作步骤
SDS聚丙烯酰胺凝胶电泳SDSPAGE实验原理和操作步骤实验原理SDSPAGE是对蛋白质进行量化比较及特性鉴定的一种经济快速而且可…
-
表达蛋白的SDS-聚丙烯酰胺凝胶电泳分析-实验方法
一原理细菌体中含有大量蛋白质具有不同的电荷和分子量强阴离子去污剂SDS与某一还原剂并用通过加热使蛋白质解离大量的SDS结合蛋白质使…
-
实验二十五 SDS聚丙烯酰胺凝胶电泳
实验二十五SDS聚丙烯酰胺凝胶电泳测定蛋白质相对分子质量一目的要求1掌握SDS聚丙烯酰胺凝胶电泳法的原理2巩固垂直板电泳的基本操作…
-
06 SDS 聚丙烯酰胺凝胶电泳法
实验六SDS聚丙烯酰胺凝胶电泳法蛋白质的分子量测定实验目的1掌握SDS聚丙烯酰胺电泳法的原理2学会用此种方法测定蛋白质的分子量实验…