酶的特异性(专一性)及影响酶活性的因素
酶的特异性(专一性)及影响酶活性的因素
实验目的
1. 掌握检查酶特异性的方法和原理。
2. 了解温度对酶活性的影响。
3. 了解激活剂、抑制剂对酶活力的影响。
实验原理
1. 酶的专一性
酶是生物体中一种具有催化功能的特殊蛋白质(传统酶的概念),也常称为生物催化剂。它与一般催化剂的最主要区别就是具有高度的特异性,即专一性。根据各种酶对底物的选择程度不同,可分为绝对专一性、相对专一性、立体异构专一性,。例如唾液淀粉酶属于相对专一性酶,它只能随机作用于淀粉链内部的a——1,4糖苷键,使其分子迅速断裂成较短的链,称为糊精,糊精分子量递减,淀粉——大分子糊精——中分子糊精——小分子糊精——简单分子糊精——麦芽糖和a——糊精(含a——1,6糖苷键的短链聚糖,平均分子量为8个残基)。
由于淀粉酶催化所形成的产物都是还原糖,故可用灵敏度较高的Benedict试剂检测和观察。
2.温度对酶促反应速度的影响
酶的催化作用受温度的影响很大,与一般化学反应一样,提高温度可以增加酶促反应的速度,通常温度每升高10℃,反应速度加快一倍左右。另一方面酶是一种蛋白质,温度过高可引起蛋白质变性,导致酶的失活。因此,反应速度达到最大值以后,随着温度的升高,反应速度反而逐渐下降,以至完全停止反应。反应速度达到最大值时的温度称为酶作用的最适温度。大多数动物酶的最适温度为37—40℃,植物酶的最适温度为50—60℃。但一种酶的最适温度不是完全固定的,它与作用的时间称短有关,反应时间增长时,最适温度向数值较低的方向移动。最适温度不是酶的特征性物理常数。酶对温度的稳定性与其存在形式有关。大多数酶在干燥的固体状态与比较稳定,能在室温下保存数月至一年,溶液中的酶,易被微生物污染,常难长期保存,在高温的情况与,如100℃即可失活。低温降低或抑制酶的活性,但不能使酶失活。
3.激活剂和抑制剂对酶活力的影响
酶的活性常受某些物质的影响,有些物质能增加酶的活性,称为酶的激活剂;另一些物质则会降低酶的活性,称为酶的抑制剂。例如氯离子为唾液淀粉酶的激活剂,铜离子则为该酶的抑制剂。通常情况下,很少量的激活剂或抑制剂就会影响酶的活性,而且常具有特异性,但是激活剂和抑制剂不是绝对的,有些物质对不同的酶所起的作用不同,如镁是脱羧酶烯醇化酶的激活剂,但是肌球蛋白ATP酶的抑制剂,同一种酶也可因激活剂的浓度不同而作用不同,如CL-在低浓度时是激活剂 ,达三分之一饱和度时则变为抑制剂。
器材和试剂
1.配制的溶于0.3%氯化钠的0.5%淀粉溶液:
2. 新配制的溶于0.3%氯化钠的0.1%淀粉溶液:
3.新配制的溶于0.3%氯化钠的0.2%淀粉溶液:
4.新配制的溶于0.3%氯化钠的1%淀粉溶液:
5.稀释的新鲜唾液。漱口后将唾液吐入量筒内收集约10ml加水至200ml,取0.2%的淀粉2ml,唾液2ml混匀,每间隔1分钟取1-2滴于白磁反应板内,加KI-I检测,控制酶的浓度使反应刚好在4-5分钟内完成。
6. 碘化钾-碘溶液:将碘化钾20克及碘10克溶于100毫升水中。使用前稀释10倍。
7.本尼迪克特(Benedict)试剂: 取86.5克柠檬酸钠(Na3C6O7·2H2O)和50克无水碳酸钠溶于450毫升蒸馏水中;再取硫酸铜(CuSO4·5H2O)8.7克溶于50毫升蒸馏水中;然后将硫酸铜溶液慢慢到入前液,边加边摇动;最后加蒸馏水稀释至500毫升(本试剂可长期保存)。
8. 1%氯化钠溶液:10、铜溶液:11、%硫酸钠溶液
12恒温水浴锅、沸水浴、移液管、电子天平
操作步骤
淀粉→分子糊精-→中分子糊精→小分子糊精→麦芽糖和α-糊精
KI-I 蓝 蓝紫 褐 红 不呈色 不呈色
一、酶的专一性
取5支试管,编号并按下表操作:
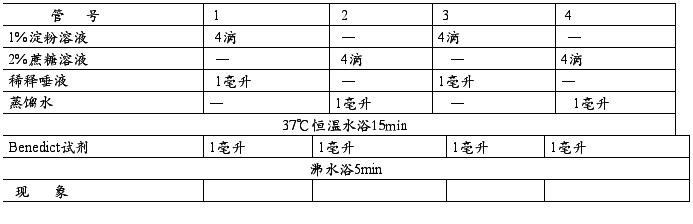
二.温度对酶活力的影响
(一)淀粉和可溶性淀粉遇碘呈蓝色。糊精按其分子的大小,遇碘可呈蓝色、紫色、暗褐色或红色。最简单的糊精遇碘不呈颜色,麦芽糖遇碘也不呈色。在不同温度下,淀粉被唾液淀粉酶水解的程度可由水解混合物遇碘呈现的颜色来判断。
(二)取三支试管,编号后按下表加入试剂:

(三)摇匀后,将1、3号两支试管放入37℃恒温水浴锅中,2号试管放入冰水中。10分钟后取出(将2号管内液体分为两半),用碘化钾-碘溶液来检验1、2、3号管内淀粉被唾液淀粉酶水解的程度。记录并解释结果,将2号管剩下的一半溶液放入37℃水浴中继续保温10分钟,再用碘液检验,结果如何?
三. 酶的激活与抑制
(一) 取三支试管,按下表编号加入相应试剂:
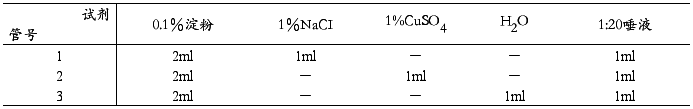
(二)加毕,摇匀,同时置37℃水浴锅中保温,每隔2分钟取液体1滴置白瓷板上用碘液试之,观察那支试管内液体最先不呈蓝色反应,那一管次之,说明原因。
注意事项
1.所用唾液,应在收集前用蒸馏水漱口,以清除食物残渣,再含一口蒸馏水,约半分钟后将其流入量筒并稀释。由于不同人或同一个人不同时间采收的唾液内淀粉酶的活性并不相同,有时差别很大。所以稀释倍数可根据各人的唾液淀粉酶活性进行调整(一般在50~300倍)。另外,稀释好的新鲜唾液若泡沫多,可进行过滤后再用。
2.实验中所用的淀粉溶液必须新鲜配制,并且在配制时必须将其煮沸至透明为止。且下次实验若再用,必须重新煮至透明,否则将影响实验结果。
3.蔗糖是典型的非还原糖,若其中的非还原糖超过一定标准,则呈现还原性,这种蔗糖不能使用。一般在实验之前要对所用蔗糖进行检查,不能呈现阳性反应,至少要用分析纯试剂。
4.唾液中除了含有淀粉酶以外,还含有少量的麦芽糖酶,该酶可使麦芽糖分解为葡萄糖。
思考题
1.什么是酶的特异性?本实验如何验证了酶的特异性?
2.蔗糖的纯度对该实验的成功与否有什么要求?
3.若将唾液酶和蔗糖酶液煮沸15分钟,其实验结果会发生什么样的变化?
4.酶反应的最适温度是酶的特征性物理常数吗?它与哪些因素有关?
参考内容
1.绝对专一性:只作用于一种底物,仅催化一种反应,如脲酶就是其中最典型的例子,只催化尿素水解而对尿素的任何衍生物均无催化水解作用。
2.相对专一性:可以催化某一类的底物或某一类的化学键,如蛋白水解酶脂酶。
3.立体异构专一性:只作用于底物的立体异构物中的一种,而且反应生成物也都是异构物中的一种。此种现象普遍存在。
第二篇:酶的专一性及影响酶促反应的因素
实验二 酶的专一性及影响酶促反应的因素
一 实验目的
通过本实验,证明酶对底物催化的专一性,以及PH、温度、激活剂、抵制剂对酶促反应速度的影响。
二 实验原理
唾液淀粉酶能专一的催化淀粉水解,生成一系列水解产物,即糊精、麦芽糖、葡萄糖等。麦芽糖或葡萄糖都属于还原糖,能使班氏试剂中的二价铜离子还原成亚铜,并生成砖红色的氧化亚铜。淀粉酶不能催化蔗糖水解,且蔗糖本身不是还原糖,所以不能与班氏试剂作用呈色。以此证明酶催化底物的专一性。
淀粉或淀粉的水解产物遇碘会呈现不同的颜色,淀粉遇碘变蓝色;糊精遇碘则根据其分子量的大小依次呈现紫色、褐色、红色;而麦芽糖、葡萄糖遇碘不呈色。通过颜色变化可以了解淀粉的程度,以观察PH、温度激活剂、抑制剂对酶促反应速度的影响。
三 药品器材
试管、试管夹、样品杯、滴瓶、温度计、恒温水浴箱,冰箱等。
1.1%淀粉溶液 称取可溶性淀粉1g,加5ml蒸馏水调成糊状,徐徐倒入80ml煮沸的蒸馏水中,不断搅拌,待其溶解后,加蒸馏水至100ml。此液应新鲜配制,防止细菌污染。
2.1%蔗糖溶液 称1g蔗糖,加蒸馏水至100ml溶解。
3.PH6.8缓冲液 取0.2mol/L磷酸氢二钠溶液154.5ml,0.1mol/L柠檬酸溶液45.5ml混合即可。
4.PH4.8缓冲液 取0.2mol/L磷酸氢二钠溶液98.6ml,0.1mol/L柠檬酸溶液101.4ml混合即可。
5.PH8.0缓冲液 取0.2mol/L磷酸氢二钠溶液194.5ml,0.1mol/L柠檬酸溶液5.5ml混合即可。
6.班氏试剂 溶解结晶硫酸铜17.3g于100ml热的蒸馏水中,冷却后加水至150ml为A液。取柠檬酸钠173g和无水碳酸钠100g,加蒸馏水600ml ,加热溶解,冷却后加水至850ml为B液。将A液缓慢倒入B液中,混合即可。
7.稀碘液 称取碘1g,碘化钾2g ,溶于300ml蒸馏水中。
8.0.9%NaCl溶液。
9.0.9%CuSO4溶液。
10.0.1%Na2SO4溶液。
11.稀释唾液 用清水漱口,清除食物残渣。再含蒸馏水30ml作咀嚼运动,2分钟后将稀释唾液收集于样品杯中备用。
四 实验方法
1.酶的专一性 取二支试管,编号,按下表操作。

2.PH对酶促反应速度的影响 取三支试管,编号,按下表操作。
3.
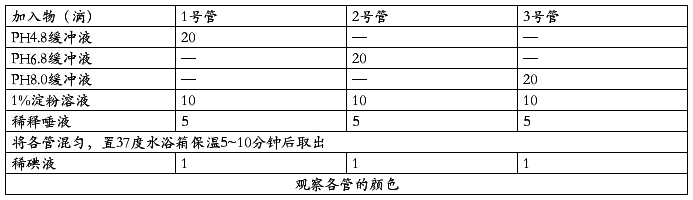
3.温度对酶促反应速度的影响 取三支试管,编号,按下表操作。

4.激活剂、抵制剂对酶促反应速度的影响 取四支试管,编号,按下表操作。

五 注意事项
1.唾液淀粉酶的活性存在个体差异,同时受唾液稀释倍数影响,收集唾液时应事先确定稀释倍数,或收集2~4人的混合唾液。
2.酶促反应的保温时间,直接影响本实验的效果。根据各实验条件通过预试,确定最佳保温时间。
六 思考题
结合本实验说明PH、温度、激活剂、抵制剂对酶促反应速度的影响。
-
实验报告-不同因素对酶的影响
实验报告课程名称:指导老师:成绩:实验名称:实验类型:分离鉴定实验同组学生姓名:Ⅰ.酶的基本性质底物专一性一、实验目的和要求1.了…
-
探究影响酶活性的因素
探究影响酶活性的因素教学设计浅秋19xx一设计理念高中生物新课程标准提出以提高学生的生物科学素养为主要目的强调学生在生物学知识科学…
-
人教版教学教案高中生物探究影响酶活性的因素(温度和pH)教学设计
高中生物探究影响酶活性的因素温度和pH教学设计安徽省淮南一中刘萍一教学目标1学会控制自变量观察和检测因变量的变化及设置对照组和实验…
-
影响酶活性的因素 (1)
探究影响酶活性的因素实验教学课例及分析高中生物蒋雪探究影响酶活性的因素实验教学课例及分析内容摘要探究实验教学能培养学生的动手动脑能…
-
实验七 探究影响酶活性的因素
实验七探究影响酶活性的因素一教材分析本节教材选自人教版必修一第五章第一节的内容由于学生已经在理论课学习了酶的概念以及酶的特性知道了…
-
实验七 探究影响酶活性的因素
实验七探究影响酶活性的因素一教材分析本节教材选自人教版必修一第五章第一节的内容由于学生已经在理论课学习了酶的概念以及酶的特性知道了…
-
实验报告-不同因素对酶的影响
实验报告课程名称:指导老师:成绩:实验名称:实验类型:分离鉴定实验同组学生姓名:Ⅰ.酶的基本性质底物专一性一、实验目的和要求1.了…
-
探究影响酶活性的因素
探究影响酶活性的因素教学设计浅秋19xx一设计理念高中生物新课程标准提出以提高学生的生物科学素养为主要目的强调学生在生物学知识科学…
-
人教版教学教案高中生物探究影响酶活性的因素(温度和pH)教学设计
高中生物探究影响酶活性的因素温度和pH教学设计安徽省淮南一中刘萍一教学目标1学会控制自变量观察和检测因变量的变化及设置对照组和实验…
-
影响酶活性的因素 (1)
探究影响酶活性的因素实验教学课例及分析高中生物蒋雪探究影响酶活性的因素实验教学课例及分析内容摘要探究实验教学能培养学生的动手动脑能…