鲁科版高中化学必修一知识点总结经典
高一化学模块I主要知识及化学方程式
一、 研究物质性质的方法和程序
1. 基本方法:观察法、实验法、分类法、比较法
第三步:用比较的方法对观察到的现象进行分析、综合、推论,概括出结论。
二、 钠及其化合物的性质:
1. 钠在空气中缓慢氧化:4Na+O2==2Na2O
2. 钠在空气中燃烧:2Na+O2点燃====Na2O2
3. 钠与水反应:2Na+2H2O=2NaOH+H2↑
现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
4. 过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑
5. 过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O2
6. 碳酸氢钠受热分解:2NaHCO3△==Na2CO3+H2O+CO2↑
7. 氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O
8. 在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO3
三、 氯及其化合物的性质
1. 氯气与氢氧化钠的反应:Cl2+2NaOH=NaCl+NaClO+H2O
2. 铁丝在氯气中燃烧:2Fe+3Cl2点燃===2FeCl3
3. 制取漂白粉(氯气能通入石灰浆)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
4. 氯气与水的反应:Cl2+H2O=HClO+HCl
5. 次氯酸钠在空气中变质:NaClO+CO2+H2O=NaHCO3+HClO
6. 次氯酸钙在空气中变质:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
四、 以物质的量为中心的物理量关系
1. 物质的量n(mol)= N/N(A)
2. 物质的量n(mol)= m/M
3. 标准状况下气体物质的量n(mol)= V/V(m)
4. 溶液中溶质的物质的量n(mol)=cV
五、 胶体:
1. 定义:分散质粒子直径介于1~100nm之间的分散系。
2. 胶体性质:
① 丁达尔现象
② 聚沉
③ 电泳
④ 布朗运动
3. 胶体提纯:渗析
六、 电解质和非电解质
1. 定义:①条件:水溶液或熔融状态;②性质:能否导电;③物质类别:化合物。
2. 强电解质:强酸、强碱、大多数盐;弱电解质:弱酸、弱碱、水等。
3. 离子方程式的书写:
① 写:写出化学方程式
② 拆:将易溶、易电离的物质改写成离子形式,其它以化学式形式出现。
下列情况不拆:难溶物质、难电离物质(弱酸、弱碱、水等)、氧化物、HCO3-等。 ③ 删:将反应前后没有变化的离子符号删去。
④ 查:检查元素是否守恒、电荷是否守恒。
4. 离子反应、离子共存问题:下列离子不能共存在同一溶液中:
① 生成难溶物质的离子:如Ba2+与SO42-;Ag+与Cl-等
② 生成气体或易挥发物质:如H+与CO32-、HCO3-、SO32-、S2-等;OH-与NH4+等。 ③ 生成难电离的物质(弱电解质)
④ 发生氧化还原反应:如:MnO4-与I-;H+、NO3-与Fe2+等
七、 氧化还原反应
1. (某元素)降价——得到电子——被还原——作氧化剂——产物为还原产物
2. (某元素)升价——失去电子——被氧化——作还原剂——产物为氧化产物
3. 氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
八、 铁及其化合物性质
1. Fe2+及Fe3+离子的检验:
① Fe2+的检验:(浅绿色溶液)
a) 加氢氧化钠溶液,产生白色沉淀,继而变灰绿色,最后变红褐色。
b) 加KSCN溶液,不显红色,再滴加氯水,溶液显红色。
② Fe3+的检验:(黄色溶液)
a) 加氢氧化钠溶液,产生红褐色沉淀。
b) 加KSCN溶液,溶液显红色。
2. 主要反应的化学方程式:
① 铁与盐酸的反应:Fe+2HCl=FeCl2+H2↑
② 铁与硫酸铜反应(湿法炼铜):Fe+CuSO4=FeSO4+Cu
③ 在氯化亚铁溶液中滴加氯水:(除去氯化铁中的氯化亚铁杂质)3FeCl2+Cl2=2FeCl3 ④ 氢氧化亚铁在空气中变质:4Fe(OH)2+O2+2H2O=4Fe(OH)3
⑤ 在氯化铁溶液中加入铁粉:2FeCl3+Fe=3FeCl2
⑥ 铜与氯化铁反应(用氯化铁腐蚀铜电路板):2FeCl3+Cu=2FeCl2+CuCl2
⑦ 少量锌与氯化铁反应:Zn+2FeCl3=2FeCl2+ZnCl2
⑧ 足量锌与氯化铁反应:3Zn+2FeCl3=2Fe+3ZnCl2
九、 氮及其化合物的性质
1. “雷雨发庄稼”涉及反应原理:
① N2+O2放电===2NO
② 2NO+O2=2NO2
③ 3NO2+H2O=2HNO3+NO
2. 氨的工业制法:N2+3H2 2NH3
3. 氨的实验室制法:
① 原理:2NH4Cl+Ca(OH)2△==2NH3↑+CaCl2+2H2O
② 装置:与制O2相同
③ 收集方法:向下排空气法
④ 检验方法:
a) 用湿润的红色石蕊试纸试验,会变蓝色。
b) 用沾有浓盐酸的玻璃棒靠近瓶口,有大量白烟产生。NH3+HCl=NH4Cl
⑤ 干燥方法:可用碱石灰或氧化钙、氢氧化钠,不能用浓硫酸。
4. 氨与水的反应:NH3+H2O=NH3?H2O NH3?H2O NH4++OH-
5. 氨的催化氧化:4NH3+5O2 4NO+6H2O(制取硝酸的第一步)
6. 碳酸氢铵受热分解:NH4HCO3 NH3↑+H2O+CO2↑
7. 铜与浓硝酸反应:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
8. 铜与稀硝酸反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
9. 碳与浓硝酸反应:C+4HNO3=CO2↑+4NO2↑+2H2O
10. 氯化铵受热分解:NH4Cl NH3↑+HCl↑
十、 硫及其化合物的性质
1. 铁与硫蒸气反应:Fe+S△==FeS
2. 铜与硫蒸气反应:2Cu+S△==Cu2S
3. 硫与浓硫酸反应:S+2H2SO4(浓)△==3SO2↑+2H2O
4. 二氧化硫与硫化氢反应:SO2+2H2S=3S↓+2H2O
5. 铜与浓硫酸反应:Cu+2H2SO4△==CuSO4+SO2↑+2H2O
6. 二氧化硫的催化氧化:2SO2+O2 2SO3
7. 二氧化硫与氯水的反应:SO2+Cl2+2H2O=H2SO4+2HCl
8. 二氧化硫与氢氧化钠反应:SO2+2NaOH=Na2SO3+H2O
9. 硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O
10. 硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O
十一、 镁及其化合物的性质
1. 在空气中点燃镁条:2Mg+O2点燃===2MgO
2. 在氮气中点燃镁条:3Mg+N2点燃===Mg3N2
3. 在二氧化碳中点燃镁条:2Mg+CO2点燃===2MgO+C
4. 在氯气中点燃镁条:Mg+Cl2点燃===MgCl2
5. 海水中提取镁涉及反应:
① 贝壳煅烧制取熟石灰:CaCO3高温===CaO+CO2↑ CaO+H2O=Ca(OH)2 ② 产生氢氧化镁沉淀:Mg2++2OH-=Mg(OH)2↓
③ 氢氧化镁转化为氯化镁:Mg(OH)2+2HCl=MgCl2+2H2O
④ 电解熔融氯化镁:MgCl2通电===Mg+Cl2↑
十二、 Cl-、Br-、I-离子鉴别:
1. 分别滴加AgNO3和稀硝酸,产生白色沉淀的为Cl-;产生浅黄色沉淀的为Br-;产生黄色沉淀的为I-
2. 分别滴加氯水,再加入少量四氯化碳,振荡,下层溶液为无色的是Cl-;下层溶液为橙红色的为Br-;下层溶液为紫红色的为I-。
十三、 常见物质俗名
①苏打、纯碱:Na2CO3;②小苏打:NaHCO3;③熟石灰:Ca(OH)2;④生石灰:CaO;⑤绿矾:FeSO4?7H2O;⑥硫磺:S;⑦大理石、石灰石主要成分:CaCO3;⑧胆矾:CuSO4?5H2O;⑨石膏:CaSO4?2H2O;⑩明矾:KAl(SO4)2?12H2O
十四、 铝及其化合物的性质
1. 铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑
2. 铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
3. 铝在空气中氧化:4Al+3O2==2Al2O3
4. 氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O
5. 氧化铝与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]
6. 氢氧化铝与强酸反应:Al(OH)3+3HCl=AlCl3+3H2O
7. 氢氧化铝与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]
8. 实验室制取氢氧化铝沉淀:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
十五、 硅及及其化合物性质
1. 硅与氢氧化钠反应:Si+2NaOH+H2O=Na2SiO3+2H2↑
2. 硅与氢氟酸反应:Si+4HF=SiF4+H2↑
3. 二氧化硅与氢氧化钠反应:SiO2+2NaOH=Na2SiO3+H2O
4. 二氧化硅与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O
5. 制造玻璃主要反应:SiO2+CaCO3高温===CaSiO3+CO2↑ SiO2+Na2CO3高温===Na2SiO3+CO2↑
鲁教版化学必修一
第一章 认识化学科学
第一节 走进化学科学
第二节 研究物质性质的方法和程序
第三节 化学中常用的物理量——物质的量
第二章 元素与物质世界
第一节 元素与物质的分类
第二节 电解质
第三节 氧化剂和还原剂
第三章 自然界中的元素
第一节 碳的多样性
第二节 氮的循环
第三节 硫的转化
第四节 海水中的化学元素
第四章 元素与材料世界
第一节 硅 无机非金属材料
第二节 铝 金属材料
第三节 复合材料
第二篇:鲁科版高中化学必修一知识点总结
高一化学模块主要知识及化学方程式
一、 研究物质性质的方法和程序
1. 基本方法:观察法、实验法、分类法、比较法
2. 基本程序:
第三步:用比较的方法对观察到的现象进行分析、综合、推论,概括出结论。
二、 钠及其化合物的性质:
1. 钠在空气中缓慢氧化:4Na+O2==2Na2O
2. 钠在空气中燃烧:2Na+O2点燃====Na2O2
3. 钠与水反应:2Na+2H2O=2NaOH+H2↑
现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处游动;④伴有嗞嗞响声;⑤滴有酚酞的水变红色。
4. 过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑
5. 过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O2
6. 碳酸氢钠受热分解:2NaHCO3△==Na2CO3+H2O+CO2↑
7. 氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O
8. 在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO3
下列关于钠的叙述错误的是 ( )
A.实验后剩余的钠粒可放回原试剂瓶中
B.用一般的化学还原法不能制取金属钠
C.自然界中无游离态的钠存在
D.钠在自然界中燃烧生成氧化钠
取一小块钠放在燃烧匙里加热,下列实验现象描述正确的是
① 钠先熔化 ②燃烧放出黄色火花 ③燃烧后得到白色固体 ④燃烧时火焰为黄色 ⑤燃烧后得到浅黄色固体
A.①② B.①②③ C.①④⑤ D.①③④
将一块钠投入到盛有煤油和水的烧杯中,观察到的现象可能是( )
A.钠在水层中反应并四处游动
B.钠停留在煤油层中不发生反应
C.钠在煤油中的液面上反应并四处游动
D.钠在煤油与水的界面处反应并可能上下跳动
下图A、B、C、D、E、F六种物质中除D为单质外其余均是常见的化合物,E和F的水溶液均呈碱性,它们的转化关系如下图所示。请回答下列问题:

(1)A、B、D的化学式A ,B ,D 。
(2)E和F可相互转化,图中己标明F向E转化的关系,请写出E转化为F的化学方程式:
。
答案:H2O CO2 Na2O2
三、 氯及其化合物的性质
1. 氯气与氢氧化钠的反应:Cl2+2NaOH=NaCl+NaClO+H2O
2. 铁丝在氯气中燃烧:2Fe+3Cl2点燃===2FeCl3
3. 制取漂白粉(氯气能通入石灰浆)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
4. 氯气与水的反应:Cl2+H2O=HClO+HCl
5. 次氯酸钠在空气中变质:NaClO+CO2+H2O=NaHCO3+HClO
6. 次氯酸钙在空气中变质:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
当不慎有大量Cl2逸出污染周围空气时,可以用浸有某种物质的一定浓度的水溶液的毛巾捂住鼻子,该物质适宜采用的是 ( )
A.NaOH B.NaCl C.Ca(OH)2 D.Na2CO3
矿泉水目前已成为人们常用的饮料,市场上有些不法商贩为牟取暴利,用自来水冒充矿泉水出售,为辨别真假,可用下列的一种化学试剂来鉴别,该试剂是( )
A.酚酞试液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
下列物质中只含有Cl2分子的是( )
A.氯水 B.液氯 C.盐酸 D.食盐
用滴管将新制的饱和氯水慢慢滴入酚酞的氢氧化钠溶液中,当滴到最后一滴时红色突然褪去。试回答下列问题:
(1)实验室保存饱和氯水的方法是 。
(2)产生上述现象的原因可能有两种:
① ;
② 。
(3)简述怎样用实验证明红色褪去的原因是①或者②?
。
(在阴凉处置于棕色试剂瓶中密封保存。氯水与氢氧化钠反应生成氯化钠和次氯酸钠,溶液碱性减弱;过量氯气与水反应生成的次氯酸具有漂白性,使溶液变成无色;向无色溶液中再滴加氢氧化钠溶液,若不再出现红色,应为原因②,若再出现红色,则为原因①。)
四、 以物质的量为中心的物理量关系
1. 物质的量n(mol)= N/N(A)
2. 物质的量n(mol)= m/M
3. 标准状况下气体物质的量n(mol)= V/V(m)
4. 溶液中溶质的物质的量n(mol)=cV
五、 胶体:
1. 定义:分散质粒子直径介于1~100nm之间的分散系。
2. 胶体性质:
① 丁达尔现象
② 聚沉
③ 电泳
④ 布朗运动
3. 胶体提纯:渗析
六、 电解质和非电解质
1. 定义:①条件:水溶液或熔融状态;②性质:能否导电;③物质类别:化合物。
2. 强电解质:强酸、强碱、大多数盐;弱电解质:弱酸、弱碱、水等。
3. 离子方程式的书写:
① 写:写出化学方程式
② 拆:将易溶、易电离的物质改写成离子形式,其它以化学式形式出现。
下列情况不拆:难溶物质、难电离物质(弱酸、弱碱、水等)、氧化物、HCO3-等。
③ 删:将反应前后没有变化的离子符号删去。
④ 查:检查元素是否守恒、电荷是否守恒。
4. 离子反应、离子共存问题:下列离子不能共存在同一溶液中:
① 生成难溶物质的离子:如Ba2+与SO42-;Ag+与Cl-等
② 生成气体或易挥发物质:如H+与CO32-、HCO3-、SO32-、S2-等;OH-与NH4+等。
③ 生成难电离的物质(弱电解质)
④ 发生氧化还原反应:如:MnO4-与I-;H+、NO3-与Fe2+等
七、 氧化还原反应
1. (某元素)降价——得到电子——被还原——作氧化剂——产物为还原产物
2. (某元素)升价——失去电子——被氧化——作还原剂——产物为氧化产物
3. 氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
(1)下列转化需要加入氧化剂才能实现的是( )
A. MnO2→MnSO4 B. AlCl3 → Al(OH)3 C. KI → KIO3 D. HNO3 →NO
(2)下列说法正确的是 ( )
A. 金属单质在反应中只做还原剂
B. 非金属在反应中只做氧化剂
C. 金属原子在反应中失电子越多还原性越强
D. Fe比Cu还原性强,Cu2+比 Fe2+氧化性强
(3)在Fe2+、 Fe3+、、Mg2+ 、S 、I- 、 H+中,只有氧化性的是_______________,只有还原性的是____________________,既有氧化性又有还原性的是___________________。
答案:(1)C (2)AD (3)Fe3+、、Mg2+ 、H+; I-;Fe2+、S 。
焊接铜器时,可用NH4Cl先除去表面的氧化铜再进行焊接,该反应可表示为
4CuO+2NH4Cl  3Cu +2CuCl2 +N2 ↑+ 4H2O
3Cu +2CuCl2 +N2 ↑+ 4H2O
(1)该反应的氧化剂是_______________,氧化产物是____________;
(2)该反应中,_________元素未被氧化;
(3)氧化剂和还原剂的质量比是_______________(最简整数比);
(4)反应中转移电子的总数为____________________。
(1)CuO;N2 (2) 氯、氧、氢 (3)240:107 (4)6e-
八、 铁及其化合物性质
1. Fe2+及Fe3+离子的检验:
① Fe2+的检验:(浅绿色溶液)
a) 加氢氧化钠溶液,产生白色沉淀,继而变灰绿色,最后变红褐色。
b) 加KSCN溶液,不显红色,再滴加氯水,溶液显红色。
② Fe3+的检验:(黄色溶液)
a) 加氢氧化钠溶液,产生红褐色沉淀。
b) 加KSCN溶液,溶液显红色。
2. 主要反应的化学方程式:
① 铁与盐酸的反应:Fe+2HCl=FeCl2+H2↑
② 铁与硫酸铜反应(湿法炼铜):Fe+CuSO4=FeSO4+Cu
③ 在氯化亚铁溶液中滴加氯水:(除去氯化铁中的氯化亚铁杂质)3FeCl2+Cl2=2FeCl3
④ 氢氧化亚铁在空气中变质:4Fe(OH)2+O2+2H2O=4Fe(OH)3
⑤ 在氯化铁溶液中加入铁粉:2FeCl3+Fe=3FeCl2
⑥ 铜与氯化铁反应(用氯化铁腐蚀铜电路板):2FeCl3+Cu=2FeCl2+CuCl2
⑦ 少量锌与氯化铁反应:Zn+2FeCl3=2FeCl2+ZnCl2
⑧ 足量锌与氯化铁反应:3Zn+2FeCl3=2Fe+3ZnCl2
(1)在FeCl3溶液、CuCl2溶液和盐酸的混合溶液中加入铁粉,反应结束后,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是( )
A. Cu2+ B. Fe3+ C. Fe2+ D. H+
(2)将下列四种铁的化合物溶于稀盐酸,滴加KSCN溶液没有颜色变化,再加入氯水即呈红色的是( )
A. FeO B. Fe2O3 C. FeCl3 D. Fe2(SO4)3
将铁粉投入到盛有Cu2+、Ag+、Fe3+ 的溶液中。反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不含的金属离子是____________;若烧杯中没有铁粉剩余,则溶液中一定含有的金属离子是____________;若溶液中不含有Cu2+时,则一定不含有的金属离子是_____________。
答案:Ag+、 Fe3+、 Cu2+; Fe2+; Ag+、 Fe3+
解析: 因为在Ag+、Fe3+、Cu2+中三种离子的氧化性顺序为Ag+> Fe3+> Cu2+ ,当加入铁粉时,按Ag+、Fe3+、Cu2+的顺序反应,当铁粉剩余时,Ag+、Fe3+、Cu2+ 将全部反应,若铁粉不剩余时,溶液中一定含有的离子只有Fe2+,溶液中不含 Cu2+ 时,因为Fe3+、Ag+的氧化性比Cu2+强,所以一定不再有Ag+和 Fe3+。
九、 氮及其化合物的性质
1. “雷雨发庄稼”涉及反应原理:
① N2+O2放电===2NO
② 2NO+O2=2NO2
③ 3NO2+H2O=2HNO3+NO
2. 氨的工业制法:N2+3H2 2NH3
3. 氨的实验室制法:
① 原理:2NH4Cl+Ca(OH)2△==2NH3↑+CaCl2+2H2O
② 装置:与制O2相同
③ 收集方法:向下排空气法
④ 检验方法:
a) 用湿润的红色石蕊试纸试验,会变蓝色。
b) 用沾有浓盐酸的玻璃棒靠近瓶口,有大量白烟产生。NH3+HCl=NH4Cl
⑤ 干燥方法:可用碱石灰或氧化钙、氢氧化钠,不能用浓硫酸。
4. 氨与水的反应:NH3+H2O=NH3?H2O NH3?H2O NH4++OH-
5. 氨的催化氧化:4NH3+5O2 4NO+6H2O(制取硝酸的第一步)
6. 碳酸氢铵受热分解:NH4HCO3 NH3↑+H2O+CO2↑
7. 铜与浓硝酸反应:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
8. 铜与稀硝酸反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
9. 碳与浓硝酸反应:C+4HNO3=CO2↑+4NO2↑+2H2O
10. 氯化铵受热分解:NH4Cl NH3↑+HCl↑
十、 硫及其化合物的性质
1. 铁与硫蒸气反应:Fe+S△==FeS
2. 铜与硫蒸气反应:2Cu+S△==Cu2S
3. 硫与浓硫酸反应:S+2H2SO4(浓)△==3SO2↑+2H2O
4. 二氧化硫与硫化氢反应:SO2+2H2S=3S↓+2H2O
5. 铜与浓硫酸反应:Cu+2H2SO4△==CuSO4+SO2↑+2H2O
6. 二氧化硫的催化氧化:2SO2+O2 2SO3
7. 二氧化硫与氯水的反应:SO2+Cl2+2H2O=H2SO4+2HCl
8. 二氧化硫与氢氧化钠反应:SO2+2NaOH=Na2SO3+H2O
9. 硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O
10. 硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O
例题1 下列关于浓硫酸的叙述正确的是( )
A. 浓硫酸具有吸水性,因而能使蔗糖炭化
B. 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C. 浓硫酸是一种干燥剂,能够干燥氨气.氢气等气体
D. 浓硫酸在常温下能够使铁铝等金属钝化
答案: D
解析:浓硫酸使蔗糖炭化,体现的是脱水性而不是吸水性,脱水性和吸水性的本质区别是看氢和氧两元素在原物质中是否是以“H2O”的形式存在。
浓硫酸与铜的反应需在加热的条件下进行。 浓硫酸作为干燥剂,不能干燥碱性和强还原性物质,氨气不能用浓硫酸干燥而氢气可以。 浓硫酸使铁铝钝化必须强调在常温下。
点评:浓硫酸的三大特性属于基础知识,应该熟练掌握、深刻理解。
例题2 强热条件下,硫酸亚铁固体发生分解:2FeSO4=Fe2O3+SO2↑+SO3↑,如将此反应生成的气体通入BaCl2溶液中,则( )
A. 析出BaSO3沉淀 B. 析出BaSO4沉淀
C. 逸出SO3气体 D. 逸出SO2气体
答案:BD
解析:在BaCl2溶液中,SO3和水剧烈反应生成H2SO4 ,H2SO4 再和BaCl2溶液反应生成BaSO4沉淀,由于BaSO4不溶于水和酸,所以析出BaSO4沉淀,不逸出SO3气体。而BaSO3虽不溶于水,但溶于酸,所以SO2和水和BaCl2溶液不会反应生成BaSO3,SO2在酸性溶液里溶解度很小,所以逸出SO2气体。
实验证明铜不能在常温下与氧气反应,铜不与稀硫酸反应,但工业上却在废铜屑与热的稀硫酸混和物中,通入空气制硫酸铜溶液。
(1)写出上述反应的化学方程式___________
(2)利用铜制备硫酸铜溶液还有什么方法?写出反应的化学方程式_____________。
比较哪种方法好?为什么?
答案:(1)方法一: 2Cu + 2H2SO4 (稀) +O2  2CuSO4 + 2H2O
2CuSO4 + 2H2O
(2)方法二: 2Cu + O2  2CuO
2CuO
CuO + H2SO4 (稀)= CuSO4 + H2O
方法三: Cu +2 H2SO4 (浓) CuSO4 + 2H2O + SO2 ↑
CuSO4 + 2H2O + SO2 ↑
第一种方法最好。若制得1mol CuSO4 ,第一种第二种方法只需要1mol硫酸,而第三种方法需要2mol 硫酸,而且生成的SO2 又造成大气污染。第一、二种方法比较,第一种方法在溶液中进行,且进行的充分。从以上分析可知第一种方法处理废铜屑最好。
解析:在稀硫酸存在的条件下,铜与氧气在加热条件下反应生成碱性氧化物CuO迅速溶解在热的稀硫酸中生成CuSO4。
方法二:是先将铜在空气中加热使之生成CuO ,在与稀硫酸反应,以上两种方法的共同特点是氧气作为氧化剂,稀硫酸只起酸的作用。
方法三:在加热条件下使铜直接与浓硫酸反应,反应中硫酸不仅起酸的作用,还起氧化剂的作用,被还原为有毒气体SO2。
点评:物质的制备应该看原料是否易得、成本低廉,是否节省原料,是否反应快,是否产生污染物等等,在评价方案时,要注意在对比中进行。
下图是实验室制取SO2并验证SO2某些性质的装置图。试回答:

①中发生反应的化学方程式为 。
②中的实验现象为 ,此实验说明SO2是 氧化物。
③的品红溶液 ,证明SO2有 。
④中的实验现象为 ,此实验说明SO2有 性。
⑤中的实验现象为 ,此实验说明SO2有 性。
⑥的作用是 ,反应方程式是 。
答案:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
试液变为红色 酸性 褪色 漂白性 产生淡黄色沉淀 氧化 褪色 还原 吸收尾气
SO2+2NaOH=Na2SO3+H2O
十一、 镁及其化合物的性质
1. 在空气中点燃镁条:2Mg+O2点燃===2MgO
2. 在氮气中点燃镁条:3Mg+N2点燃===Mg3N2
3. 在二氧化碳中点燃镁条:2Mg+CO2点燃===2MgO+C
4. 在氯气中点燃镁条:Mg+Cl2点燃===MgCl2
5. 海水中提取镁涉及反应:
① 贝壳煅烧制取熟石灰:CaCO3高温===CaO+CO2↑ CaO+H2O=Ca(OH)2
② 产生氢氧化镁沉淀:Mg2++2OH-=Mg(OH)2↓
③ 氢氧化镁转化为氯化镁:Mg(OH)2+2HCl=MgCl2+2H2O
④ 电解熔融氯化镁:MgCl2通电===Mg+Cl2↑
海水的综合利用可以制备金属镁,其流程如下图所示:
 粗盐 (水.重结晶) 精盐
粗盐 (水.重结晶) 精盐

海水
母液 Mg(OH)2(盐酸浓缩) MgCl2·6H2O
(脱水)
 MgCl2
MgCl2
(电解)
Mg

 贝壳(煅烧)CaO(水) 石灰乳
贝壳(煅烧)CaO(水) 石灰乳
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式.
____________________________________________________。
(2) Mg(OH)2沉淀中混有Ca(OH)2应怎样除去?写出实验步骤。
(3)实验室里将粗盐制成精盐的过程,在溶解、过滤、蒸发三个步骤操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
① 溶解时:___________________
② 过滤时:___________________
③ 蒸发时:___________________
(1) MgCl2·6H2O Mg(OH)Cl +HCl↑+ 5H2O ↑
Mg(OH)Cl +HCl↑+ 5H2O ↑
MgCl2·6H2O MgO+ 2HCl↑+ 5H2O ↑
MgO+ 2HCl↑+ 5H2O ↑
(2)加入MgCl2溶液,充分搅拌,过滤,沉淀用水洗涤。
(3)①搅拌,加速溶解。
②使待滤液体沿玻璃棒流入漏斗,防止外洒。
③搅拌,防止因局部过热液滴或晶体飞溅。
十二、 Cl-、Br-、I-离子鉴别:
1. 分别滴加AgNO3和稀硝酸,产生白色沉淀的为Cl-;产生浅黄色沉淀的为Br-;产生黄色沉淀的为I-
2. 分别滴加氯水,再加入少量四氯化碳,振荡,下层溶液为无色的是Cl-;下层溶液为橙红色的为Br-;下层溶液为紫红色的为I-。
溴和海水提溴
1. 与溴关系密切的一组元素——卤素
溴和氯、碘等元素在原子结构和元素性质方面有一定的相似性,它们在元素周期表中排在同一纵列(同一族)里,常一起研究。由于这些元素易形成盐,所以它们被称为卤素(卤是“成盐”的意思)。
2. 溴单质和碘单质的物理性质
(1)实验探究溴和碘的物理性质:重点色、态、味及溶解性。

此外,碘受热易升华。
(2)萃取
实验探究溴水和碘水中加入CCl4的现象
实验表明,用CCl4可以提取溴水中的溴以及碘水中的碘,这种分离方法叫萃取。
利用混合物中一种溶质在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来的分离方法叫萃取,萃取所用的仪器是分液漏斗。
小结:① 溴、碘在水中溶解度不大,但易溶于有机溶剂。
② 溴是常温下唯一呈液态的非金属,保存时应盛放在棕色、磨砂玻璃塞、细口瓶中,通常还加入少量水,形成水封,减少挥发。
③碘易升华,遇淀粉变蓝,这是碘的特性。
3. 氯、溴、碘单质氧化性的强弱
实验探究氯、溴、碘氧化性的强、弱:

有益补充:① 碘的氧化性较弱,遇变价金属得低价化合物。如碘与铁反应生成FeI2
② 氯、溴、碘的单质都能与H2反应,生成HX;HCl、HBr、HI都易溶于水,且都是强酸。
③ 氯、溴、碘的单质都能与水反应:X2+H2O=HX+HXO,但反应程度依次减弱。
④ AgBr为浅黄色难溶物;AgI为黄色难溶物。二者见光都易分解。
4. 海水提溴与海洋的综合利用
(1)海水提溴:溴单质的氧化性介于氯和碘之间,因此海水提溴可以选取氯气作氧化剂。大体分为三个步骤:
浓缩 海水中的Br-的浓度很小,大约0.067g/L,海水晒盐剩下的苦卤中的Br-浓度较大,可作提取溴的原料。
氧化 向苦卤中通入氯气。Cl2+2Br-=2Cl-+Br2
提取 向溶有溴的苦卤中鼓入热空气或水蒸气,使溴挥发而分离出来。
溴的用途很广泛。
十三、 常见物质俗名
①苏打、纯碱:Na2CO3;②小苏打:NaHCO3;③熟石灰:Ca(OH)2;④生石灰:CaO;⑤绿矾:FeSO4?7H2O;⑥硫磺:S;⑦大理石、石灰石主要成分:CaCO3;⑧胆矾:CuSO4?5H2O;⑨石膏:CaSO4?2H2O;⑩明矾:KAl(SO4)2?12H2O
十四、 铝及其化合物的性质
1. 铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑
2. 铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
3. 铝在空气中氧化:4Al+3O2==2Al2O3
4. 氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O
5. 氧化铝与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]
6. 氢氧化铝与强酸反应:Al(OH)3+3HCl=AlCl3+3H2O
7. 氢氧化铝与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]
8. 实验室制取氢氧化铝沉淀:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
十五、 硅及及其化合物性质
1. 硅与氢氧化钠反应:Si+2NaOH+H2O=Na2SiO3+2H2↑
2. 硅与氢氟酸反应:Si+4HF=SiF4+H2↑
3. 二氧化硅与氢氧化钠反应:SiO2+2NaOH=Na2SiO3+H2O
4. 二氧化硅与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O
5. 制造玻璃主要反应:SiO2+CaCO3高温===CaSiO3+CO2↑
SiO2+Na2CO3高温===Na2SiO3+CO2↑
下图中每一方格表示的有关的一种反应物和生成物。己知B是一种单质,其余物质都是含有B元素的化合物;C是一种钠盐;E是C对应的酸;B和D的晶体都是高熔点、坚硬的固体,且D为B的氧化物(其它不含B元素的反应物及各步添加的必要试剂和反应条件均己略去)。

(1)写出A、D、E的化学式:A ;D ;E 。
(2)在工业上,用碳在高温下还原D的方法可制得含少量杂质的B,其化学反应方程式为
;
A和B的互变在工业上的实际意义是 。
(3)写出D→C反应的离子方程式 。
答案:SiCl4 SiO2 H2SiO3 粗硅提纯
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32
Cl 35.5 Ca 40 Fe 56 Cu 64
第Ⅰ卷
一.单项选择题
1. 酸雨给人类带来种种灾害,与酸雨形成有关的气体是
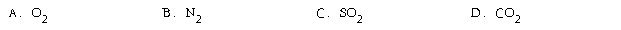
2. 下列金属可与NaOH碱溶液发生反应的是
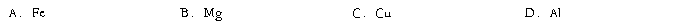
3. 最近科学家制得一种新的分子,它具有空心的类似足球状结构,化学式为C60,下列说法中不正确的是
A.C60是一种新型的化合物
B.C60和石墨都是碳的同素异形体
C.C60是一种单质
D.C60分子是由60个碳原子构成的分子
4.制取下列物质,无需用到二氧化硅(SiO2)的是
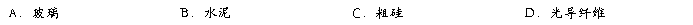
5.金属钠放置在空气中,最后生成的产物是
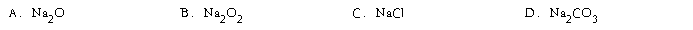
6.摩尔是表示

7.下列反应的离子方程式书写正确的是
A.BaCl2溶液与Na2SO4溶液反应:Ba2+ + SO42- = BaSO4↓
B.NaOH溶液与稀硝酸的反应:NaOH + H+ = Na+ + H2O
C.NaHCO3溶液与盐酸的反应:NaHCO3 + H+ = Na+ + H2O + CO2↑
D.KCl溶液与AgNO3溶液的反应:K+ Ag+ = AgCl↓ + K+
8.下列变化需要加入还原剂才能实现的是

9.用58.5克NaCl溶解于水,配成0.1L溶液,所得溶液的物质的量浓度为

10.关于金属钠的性质描述不正确的是
A.很软可用刀切割
B.在空气中燃烧生成白色的过氧化钠
C.金属钠通常保存在煤油里
D.钠具有银白色金属光泽,密度比水小
11.有毒、有刺激性气味,有颜色的气体是

12.下列反应发生时,会产生棕黄色烟的是
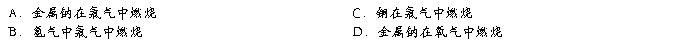
13.下列常见现象与胶体无关的是
A.清晨在密林中看到一缕缕的光束
B.向豆浆中加入硫酸钙使蛋白质等聚沉,制成可口的豆腐
C.利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上
D.FeCl3溶液加入NaOH溶液产生红褐色沉淀
14.下列物质中属于电解质的是
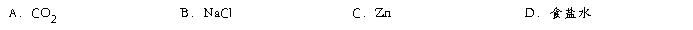
15.1molH2O含有H2O分子个数是
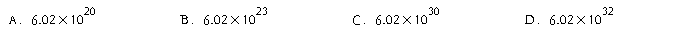
16.向NaBr、NaI的混合溶液通入足量的氯气,加热将溶液蒸干,并再灼热片刻,最后残留的物质可能是

第Ⅱ卷非选择题
二.填空题(本大题有3小题,共22分)

 17.(8分)在Fe2O3 + 3CO 2Fe + 3CO2 的反应中, 是氧化剂;
17.(8分)在Fe2O3 + 3CO 2Fe + 3CO2 的反应中, 是氧化剂;
是还原剂; 有氧化性; 有还原性。
18.(8分)在龙城高级中学第二届体艺节开幕式上,五颜六色的汽球冉冉升空。升空的汽球中填充的气体是 (填写中文名称或化学式均可) 。请你写出制取该气体的三个化学方程式:
①
②
③
 19.(6分)某工业废液里含有FeCl2、CuCl2和FeCl3。为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程:
19.(6分)某工业废液里含有FeCl2、CuCl2和FeCl3。为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程:
(1)方框内物质A和B的化学式:A ,B 。
(2)第①步通入B的化学方程式为 。
三.推断题(8分)
 20.(8分)有四种钠的化合物W、X、Y、Z能发生下列变化,其中Z是一种常见的碱,Y是我们日常生活中经常接触到的。
20.(8分)有四种钠的化合物W、X、Y、Z能发生下列变化,其中Z是一种常见的碱,Y是我们日常生活中经常接触到的。
 W X + CO2 ↑+ H2O
W X + CO2 ↑+ H2O
 X + HCl Y + H2O + CO2 ↑
X + HCl Y + H2O + CO2 ↑
 W + Z X + H2O
W + Z X + H2O
试用化学式填空:
W是 ;X是 ;
Y是 ;Z是 。
四.实验题(本大题有2小题,共15分)
21.(5分)要制取O2、NH3、CO2、NO、NO2气体,从下列各物质中,分别选出必要的物质(要求是一步制得,如有多种可能,仅需要写出一种情况), 将序号填在括号内。
①铜片 ②稀硝酸 ③浓硝酸 ④氢氧化钙 ⑤氯化铵
⑥石灰石 ⑦盐酸 ⑧高锰酸钾 ⑨碳酸氢铵 ⑩碳酸氢钠
制O2 、制NH3 、制CO2 ,
制NO 、制NO2 。
22.(10分)如下图所示,是实验室制备某常见气体的实验装置,请填空:

(1) 该实验装置制备的常见气体是(填写化学式): 。
(2) 制备该气体的化学方程式是:
。
(3) 收集该气体的方法是: 。
(4) 检验该气体是否收集满的方法是:
。
(5) 将充满该气体的试管倒立于水槽中,可以看到的现象是:
。
五.计算题(本大题有2小题,共7分)
23.(3分)某种待测浓度的H2SO4溶液5mL,加入10mL0.5mol/LBaCl2溶液,恰好完全反应。问得到BaSO4沉淀多少克?
24.(4分)在标准状况下,100mL某气体的质量是0.179克。计算这种气体的相对分子质量?
C D A B D A A C D B B C D B B B
17.(每空2分,共8分)Fe2O3,CO,Fe2O3,CO。
18.(每空2分,共8分)氢气或H2,(其他答案也可)
①2Na + 2H2O = 2NaOH + H2 ↑
②Fe + 2HCl = FeCl2 + H2 ↑
③Zn + 2HCl = ZnCl2 + H2 ↑
19.(每空2分,共6分)HCl,Cl2,2FeCl2 + Cl2 = 2FeCl3
20.(每空2分,共8分) W是NaHCO3,X是Na2CO3,Y是NaCl,Z是NaOH。
21.(每空1 分,共5分)制O2 ⑧、制NH3⑤ 或 ⑨ 或 ④与⑤ 或 ⑤与⑩、
制CO2⑥ 或 ⑨ 或 ⑩ 或 ⑥与⑦ 或 ⑦与⑩,
制NO①与②、制NO2③ 或 ①与③ 。
22.(每空2分,共10分)
(1)NH3,(2) 2NH4Cl+ Ca(OH)2 = CaCl2 + 2H2O + 2NH3 ↑
(3) 向下排空气法 (4) 用湿润的红色石蕊纸看是否变蓝,或用蘸有浓盐酸的玻棒靠近,看是否产生白烟。(5)水面上升,直至充满试管。
23.(3分)解:依题意,设得到BaSO4沉淀x,则
n(BaCl2) = 0.01L×0.5mol/L = 0.005 mol 1分
H2SO4 + BaCl2 = BaSO4↓ + 2HCl 1分
1 mol 233g
0.005 mol x
∴ x = 1.165 g 1分
答:得到BaSO4沉淀1.165克。
24.(4分)解:标准状况下,Vm=22.4mol/L
∴n=  =
= 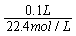 =0.00446mol 2分
=0.00446mol 2分
M=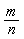 =
=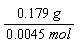 =40.1mol/L 2分
=40.1mol/L 2分
答:这种气体的相对分子质量是40。
-
人教版高一化学必修一知识点总结
一重点聚焦1混合物的分离原理和分离方法2混合物分离方法的操作3离子的检验及检验试剂的选择4物质分离与提纯过程的简单设计5物质的量及…
-
高一化学必修一知识点总结
新课标化学必修一1学习方法2研究一种物质的性质的程序3观察法4金属钠的物理性质5金属与水的反应第三章金属及其化合物1金属的化学性质…
-
高中化学必修一知识点总结
高中化学必修1复习提纲注A了解B理解C综合应用必修1全册基本内容梳理一从实验学化学一化学实验安全11做有毒气体的实验时应在通风厨中…
-
高中化学必修一知识点总结 精简版
第一章从实验学化学一化学实验安全11做有毒气体的实验时应在通风厨中进行并注意对尾气进行适当处理吸收或点燃等进行易燃易爆气体的实验时…
-
高中化学必修一知识点总结
必修1全册基本内容梳理从实验学化学一化学实验安全11做有毒气体的实验时应在通风厨中进行并注意对尾气进行适当处理吸收或点燃等进行易燃…
-
高中化学必修一知识点总结
高一化学必修I主要知识及化学方程式一、研究物质性质的方法和程序1.基本方法:观察法、实验法、分类法、比较法2.基本程序:略二、钠及…
-
高一化学必修一知识点归纳[1]
高一化学必修一知识点归纳-----------------------------------------------------…
-
高一化学必修一知识点及方程式总结
高一化学必修一知识点及方程式总结.txt如果不懂就说出来,如果懂了,就笑笑别说出来。贪婪是最真实的贫穷,满足是最真实的财富。幽默就…
-
高中化学必修一知识点总结
高中化学必修一全册基本内容梳理第一章从实验学化学一化学实验安全11做有毒气体的实验时应在通风厨中进行并注意对尾气进行适当处理吸收或…
-
高中化学必修一知识点总结
高中化学必修一全册基本内容梳理第一章从实验学化学一化学实验安全11做有毒气体的实验时应在通风厨中进行并注意对尾气进行适当处理吸收或…
-
高一化学必修一知识点总结
必修1全册基本内容梳理第一章一化学实验安全11做有毒气体的实验时应在通风厨中进行并注意对尾气进行适当处理吸收或点燃等进行易燃易爆气…