�����ˮ��֪ʶ��(ѧ����)
�������ˮ��֪ʶ��ϰ��
һ��̽������Һ�������
���ۣ�ǿ�������������ԣ�ǿ���������Լ��ԣ�ǿ��ǿ���������ԡ�
��������Һ���ֲ�ͬ����Ե�ԭ���ε�ˮ�⡣
�����ε�ˮ��ԭ��
1.���壺����Һ�У��ε�������������ӻ���������ˮ�����������H+��OH�������������������������ý��������ˮ�⡣
2.ʵ�ʼ����
ʵ�ʣ��ٽ�ˮ�ĵ���ƽ�⡣
������ε���Һ���ֳ���ͬ�̶ȵ��ᡢ���ԡ�
3.ˮ��������
a.�α�������ˮ��
b.�����ε���������������������ˮ�⣬������ˮ�⣬����˫ˮ�⣩
4.ˮ��������ˮ�������������ģ��ÿ�����š� ��
��
��С�ˮ����ɣ�������ˮ�⣬������ˮ�⣬����˫ˮ�⣬˭ǿ��˭�ԣ���ǿ�����ԡ�
5 ����Һ��ˮ�ĵ������
�����⡿1��pH=3��HCl��pH=11��NaOH��Һ����ˮ���������c(H+)�ж��٣�
2��pH=3��NH4Cl��pH=11��CH3COONa��Һ����ˮ���������c(H+)�ж��٣�
��С�����Һ��ˮ�ĵ��������¹��ɣ�
a.��ǿ����������Һ�У��ε�ˮ��ٽ���ˮ�ĵ��룬ˮ�ĵ���̶ȱȴ�ˮ��������Һ������ˮ�ĵ��룩��ˮ�ĵ���̶ȴ�
b.��������Һ�У�c(H+)��c(OH-)��С����һ����ʾˮ�ĵ��룻������Һ�У�c(H+)��c(OH-)�д����һ����ӳ��ˮ�ĵ���̶ȡ�
�ġ�ˮ�ⷽ��ʽ����д
��1���ж��ܷ�ˮ�⣻
��2��ˮ�������ģ��ÿ�����ű�ʾ��ͨ�������ɳ��������壬Ҳ�������ֽ⡣����д���ӷ���ʽʱһ�㲻�ꡰ����������Ҳ�����������H2CO3��NH3·H2O�ȣ�д����ֽ�������ʽ��
��3����Ԫ������ηֲ�ˮ�⣬�Ե�һ��Ϊ����
��4����Ԫ�����ε�ˮ����Ϊһ����ɡ�
��5��˫ˮ�⡪������ȫ˫ˮ������ȫ˫ˮ��
����ȫˮ���ÿ�����ţ���ȫˮ���õȺű�ʾ��
�塢����ˮ���Ӱ������
1������Խ��Խˮ�⣨Խ��Խˮ�⣬ԽϡԽˮ�⣩
�Դ�����Ϊ����CH3COO-+H2O  CH3COOH+OH- Kh
CH3COOH+OH- Kh

���������ĵ��볣��Խ��Խ�������������ɵ���ˮ��ij̶Ⱦ�Խ��
2�������¶ȡ�Ũ�ȡ���or�����Һ
����ϰ���ڰ�ˮ�д�������ƽ�⣺NH3·H2O  NH4++OH-���������������ʶԸ�ƽ���к�Ӱ�죿
NH4++OH-���������������ʶԸ�ƽ���к�Ӱ�죿
��NH4Cl���� ��Na2CO3���� ��FeCl3����
���ܽ�ж���Һ��ƽ���ƶ������һ��˼·��
�ټ���������Ƿ���֮��Ӧ��
�ڼ���������Ƿ���֮��ͬ����ЧӦ��
����ǰ������߱�����ˮ�����⡣
����ˮ��ƽ���Ӧ��
(1)���úʹ�����ˮ�������Һ
������FeCl3��AlCl3��CuCl2��SnCl2��ǿ����������Һʱ��Ϊ��ֹˮ�⣬���Ƚ�������������Ӧ�����У��ټ�����ˮϡ�͵�����Ũ�ȡ�
Na2SiO3��Na2CO3��NH4F�Ȳ��ܴ�������ĥ�ڲ��������Լ�ƿ�С���ˮ��ʼ��ԣ��벣����ɳɷ����ò���ij��������ʣ���ƿ����ƿ�����һ��
(2)ijЩ���ý�����ǿ�������η�Ӧ
NH4+ + H2O  NH3�qH2O + H+
NH3�qH2O + H+
þ�����²�����ˮ������Ӧ����þ�۷����Ȼ�淋�ˮ��Һ���������ų�
(3)�ж������ܷ��������
����Ľ��������ӣ���Al3+��Cu2+��NH4+��Fe3+�ȣ���������������HCO3-��CO32-��SiO32-��AlO2-��F-�ȣ�����Һ�в���ͬʱ�������档
(4)ʩ�û���
����ʩ��(NH4)2SO4��������NH4+ˮ���ʹ������������ǿ����ľ��(K2CO3)�������̬���ʻ��á�
(5)�ж�����Һ������Ի�pH
(6)�ж�����Һ�������������
(7)��������ijЩ����Һ��ȡ��������
�ж�����Һ���ɵõ�ʲô������Ҫ���������������档
aˮ��������Һˮ�������ѻӷ�����ʱ�����ɺ�һ���ԭ���ʣ���Al(SO4)2��CuSO4��Һ���ɵ�Al(SO4)2��CuSO4���壻����Һˮ�����ɲ��ӷ��������ʱ������Ҳ�õ�ԭ���ʣ���K2CO3��Na2S��Һ���ɵõ�K2CO3��Na2S���壻����Һˮ�������ӷ�����ʱ�����ɺ�һ��ö�Ӧ�������AlCl3��FeCl3��Һ���ɺ�һ���Al(OH)3��Fe(OH)3��
b�ֽ������ε����ȶ��Բ������������Һ�Ĺ����лᷢ���ֽ���ò���ԭ���ʣ��õ�������ֽ�����Ca(HCO3)2��NaHCO3��KMnO4��NH4Cl���������ֽ⣬�������Ca(HCO3)2��Һ�õ�CaCO3���壻����NaHCO3��Һ�õ�Na2CO3���壻����KMnO4��Һ�õ�K2MnO4��MnO2�Ļ�������NH4Cl��Һ���ܵõ����塣
c���������εĻ�ԭ��ǿ��������������Һ�Ĺ������ο��ܱ�O2�������ò���ԭ���ʣ��õ����������������NaSO3��Һ���ɻ�õ�Na2SO4��FeSO4��Һ���ɻ�õ�Fe2(SO4)3��Fe2O3�Ļ���
(8)��ĭ�������Al2(SO4)3��NaHCO3��
Al3+ + 3HCO3- = Al(OH)3��+3CO2��
Al3+����CO32-��HCO3-��AlO2-��S2-���棬Fe3+����CO32-��HCO3-��AlO2-����
�ߡ��ж���Һ����Ũ�ȴ�С
Na2CO3 c(Na+)��c(CO32-)��c(OH-)��c(HCO3-)��c(H+)
����غ㣺c(Na+)+c(H+) =2c(CO32-)+c(OH-)+c(HCO3-)
�����غ㣺c(Na+) = 2 [ c(CO32-) + c(HCO3-) + c(H2CO3) ]
�����غ㣺c (H+) + c (HCO3-) + 2 c (H2CO3) = c (OH-)
NaHCO3 c(Na+)��c(HCO3-)��c(OH-)��c(H+)��c (CO32-)
����غ㣺c(Na+)+c(H+) =2c(CO32-)+c(OH-)+c(HCO3-)
�����غ㣺c(Na+) =[ c(CO32-) + c(HCO3-) + c(H2CO3) ]
�����غ㣺c (H+) +c (H2CO3) = c (OH-) + c (CO32-)
NH4Cl c(Cl-)��c(NH4+)�� c(H+) �� c(OH-)
����غ㣺c (NH4+)+c( H+) = c(Cl-) + c(OH-)
�����غ㣺c (NH4+) + c(NH3·H2O) = c(Cl- )
�����غ㣺c(H+) = c(OH-) + c(NH3·H2O )
����غ����������Һ�ʵ����ԣ���������������������������������������������ĸ��������������Ϊ�㡣
�����غ���ԭ���ڱ仯���̣�ˮ�⡢���룩����Ŀ���䡣
�����غ����ڴ�ˮ�м������ʣ������Һ�в�c(H+)��������Ũ��֮��Ĺ�ϵʽ���ɵ���غ�������غ��Ƴ���
�����Һ��Ҫ���������ȷ��Һ����ԣ��Ӷ��ó�H+��OH-֮��Ĺ�ϵ����ͨ������غ㡢�����غ㡢�����غ����ع�ϵʽ�����������Ũ�ȴ�С˳��
����ϰ��
1.ͬŨ�ȵ�������ҺpH��С�����˳����
��H2SO4 ��Ba(OH)2 ��CH3COOH ��HCl ��NaCl ��NH4Cl ��CH3COONa
2.NH4Cl��Һ��HClϡ��ҺpH��Ϊ5����������Һ��ˮ�������c(H+)�ֱ�Ϊa��b����a��b����ȷ��ϵ�ǣ� ��
A. a=b B. b��a C. b=104a D. a=104b
3.Na2CO3��Һ��ϡ�����У���Һ��������Щ�������� ��
A. c(H+) B. c(OH-) C. pHֵ D. CO32-+H2O HCO3- + OH-
HCO3- + OH-
4.�ܽ�Ba(NO3)2��KCl ��Al2(SO4)3��FeCl3��CH3COOH������Һ�����Լ��� �� ��
A.pH��ֽ B.Na2CO3 C.NaOH D.NH3·H2O
5.0.2mol/LNH3·H2O��Һ��0.1mol/LHCl��Һ�������ϣ�����Ũ���ɴ�С��˳���� ��
6.�����£������������������Һ��ϣ�������ҺpH=7����Һ��c(HCOO-)��c(Na+)�Ĺ�ϵΪ�� ��
A. c(HCOO-) �� c(Na+) B. c(HCOO-) �� c(Na+)
C. c(HCOO-) = c(Na+) D. ��ȷ��
7�������ʵ�������0.1mol��HCN��NaCN���1L�����Һ����֪����c(CN-) С��c(Na+)���������ж�����ȷ���ǣ� ��
A. c(H+) �� c(OH-) B. c(HCN) �� c(CN-) =0.2mol/L
C. c(HCN) �� c(CN-) D. c(CN-) �� c(OH-) =0.1mol/L
8����Na2S��ˮ��Һ�д����Ŷ������Ӻͷ��ӣ����й�ϵ����ȷ���� �� ��
(A) c(OH-) = c(H+) + c(HS-) + c(H2S)
(B) c(OH-) = c(H+) + c(HS-) + 2c(H2S)
(C) c(Na+) + c(H+) = c(OH-) + 2c(S2-)+c(HS-)
(D) c(Na+) = 2c(S2-) + 2c(HS-) + 2c(H2S)
9����0.02mol/LCH3COOH��Һ��0.01mol/LNaOH��Һ�Ե������ϣ������Һ������Ũ
�ȹ�ϵ��ȷ���ǣ� ��
A. c(CH3COO-) �� c(Na+) B. c(CH3COOH) �� c(CH3COO-)
C. 2c(H+)=c(CH3COO-) - c(CH3COOH) D. c(CH3COOH)+c(CH3COO-)=0.02mol/L
10����������Ũ�ȴ�С�Ƚϴ�����ǣ� ��
A. c(Cl-)��c(NH4+)�� c(H+) �� c(OH-)
B. c(Cl-)��c(NH4+)�� c(OH-) �� c(H+)
C. c(Cl-)�� c(H+) �� c(NH4+) �� c(OH-)
D. c(NH4+)��c(Cl-) ��c(OH-) �� c(H+)
11����֪ij��Һ��ֻ����OH-��H+�� Na+ �� CH3COO-�������ӣ�������Һ�к����������ʣ�������������Ũ�ȴ�С˳������ǣ� )
A. c(CH3COO-)>c(Na+ )>c( OH- )>c(H+) B. c(Na+ )>c(CH3COO-) >c(H+) > c( OH- )
C. c(Na+ )=c(CH3COO-) > c( OH- ) = c(H+) D. c(Na+ )>c( OH- ) > c(CH3COO-) >c(H+)
12��Ϊ������CH3COO-��Na+����Ũ�ȱ�Ϊ1��1����Һ������CH3COONa��Һ�м���( )
A �������� B ����NaOH����
C ����KOH D ����NaCl����
13��ij�¶�(t��)ʱ��ˮ��KW=10-13,����¶ȣ�����ڡ�С�ڡ�����ڣ�__ 25�棬��
������ �������¶���pH=11��NaOH��ҺamL��pH=1��H2SO4��ҺbmL���:
(1)�����û��ҺΪ���ԣ���a:b=____;����Ũ�Ȱ���С��___________ ��
(2)�����û��Һ��pH=2����a:b=_____;����Ũ�Ȱ���С�� ____________________ ��
14����0.2mol/L CH3COONa��0.1mol/LHCl�������Ϻ���Һ�������������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ� ��
A [CH3COO-]=[Cl-]=[H+]>[CH3COOH] B [CH3COO-]=[Cl-]>[CH3COOH] >[H+]
C [CH3COO-]>[Cl-]>[H+]>[CH3COOH] D [CH3COO-]>[Cl-]>[CH3COOH]>[H+]
15����ˮ�������c(H+)=10-14mol/L����Һ�У�һ���ܴ���������������ǣ� ��
A .K+ Fe2+ SO32- MnO4- B. Na+ Cl- NO3- SO42-
C .Al3+ NH4+ Cl- SO42- D. Na+ AlO2- Br- Cl-
16��0.1mol/L��NaHS��Һ���й���Ũ�ȵĹ�ϵ����ȷ���ǣ� ��
A .[Na+]>[HS-]>[S2-]>[H+]>[OH-] B. [Na+]>[HS-]>[OH-]>[S2-]
C.[Na+]=[HS-]+2[S2-]+[OH-] D. [Na+]=[H2S]+[HS-]+[S2-]
17�������£�0.1mol·L-1ijһԪ��(HA)��Һ�� c(OH-)/c(H+)��1×10-8������������ȷ����( )
A������Һ����ˮ�������c(H��)��1×10-3 mol·L-1
B����pH��3��HA��pH��11��NaOH��Һ�������ϣ���Һ��c(Na+)��c(A-)��c(OH-)��c(H+)
C��Ũ�Ⱦ�Ϊ0.1mol/L��HA��NaA��Һ�������Ϻ�����Һ�����ԣ���
c(A-)��c(HA)��c(Na+)��c(H+)��c(OH-)
D��0.1mol·L��1HA��Һ��0.05mol·L��1NaOH��Һ�������Ϻ�������Һ��
2c(H+)��c(HA)��c(A-)��2c(OH-)
18����25��ʱ��pH��11 ��NaOH ��Һ��pH��3 ��CH3COOH��Ҵ�������Ϻ����й�ϵʽ����ȷ����( )
A��c (Na+)=c(CH3COO-)+c(CH3COOH)
B��c(H+)=c(CH3COO-)+c(OHһ)
C��c (Na+) > c (CH3COO-)>c(OH)>c(H+)
D��c (CH3COO-)>c(Na+)>c(H+)>c(OH-)
19��������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ���� ( )
A�������£���0.01 mol·L��1 NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�
c(Na+)��c(SO42-)��c(NH4+)��c(OH-)��c(H+)
B��0.1 mol·L��1�� NaHCO3��Һ�� c(Na+)��c(OH-)��c(HCO3-)��c(H+)
C��Na2CO3��Һ�� c(OH-)��c(H+)��c(HCO3-)+2 c(H2CO3)
D��25�棬pH =4.75��Ũ�Ⱦ�Ϊ0.1 mol·L��1�� CH3COOH��CH3COONa�����Һ��
c(CH3COO-)��c(OH-) �� c(CH3COOH) ��c(H+)
20����AlCl3��Һ�������գ����ĵõ���Ҫ���������ʲô��Ϊʲô�����û�ѧ����ʽ��ʾ���������Ա�Ҫ������˵����
21. Ϊ�˷�ֹ����FeCl3��Һʱ���ܻ��ǣ�Ӧ����Һ�м���_______����______ˮ�⡣Mg��Ͷ��NH4Cl��Һ�з�Ӧ�����ӷ���ʽ�� ����ĭ�����ԭ��(���ӷ���ʽ)��_____________
22�������Ƕ�Ԫ��ǿ�ᣬ����������Һ�����ԡ������£���10mL 0.01 mol/L NaHC2O4��Һ�еμ�0.01 mol/L NaOH��Һ������NaOH��Һ��������ӣ���Һ������Ũ�ȹ�ϵ��ȷ����(D)
A V(NaOH)��0ʱ��c(H+)��1×10��2 mol/L
B V(NaOH)��10 mLʱ�������ܴ���c(Na��)��2c(C2O42��)�� c(HC2O4��)
C V(NaOH)��10 mLʱ��c(H+)��1×10��7mol/L
D V(NaOH)��10 mLʱ��c(Na+)��c(C2O42-)��c(HC2O4-)
�ڶ�ƪ���߿�ר�������ˮ��֪ʶ��;���ϰ��
��25�� �����ˮ��
������������
���¿���
1.��������ˮ���ԭ������������ˮ��Ĺ��ɺ�Ӧ�á�
2���˽�����Һ������ԣ���Ƚ�����Һ������Ũ�ȵĴ�С��
������ϰ
һ������ˮ��Ķ����ʵ��
1������ˮ��Ķ��� ����Һ���ε�����������Ӹ�ˮ��
������������Ļ��ʵķ�Ӧ�����������ˮ�⡣
2������ˮ���ʵ��
�����ˮ�����θ�ˮ֮��Ļ�ѧ��Ӧ��ˮ��(��Ӧ)��ʵ���������ѵ�������ʣ�ʹˮ�ĵ���ƽ�ⱻ�ƻ������������µ�ƽ�⡣
3������ˮ�ⷴӦ���ӷ���ʽ����д
����ˮ��һ��̶Ⱥ�С��ˮ�����Ҳ���٣�ͨ�������ɳ��������壬��дˮ�ⷽ��ʽʱ��һ�㲻�á���������������ˮ���ǿ��淴Ӧ��������ǿ��˫ˮ������⣬һ�����ӷ���ʽ�в�д===�ţ���д���š�
4�������ˮ������Һ������� ��NaCl ��NH4Cl ��Na2CO3 ��CH3COONa ��AlCl3 ������Һ�г����Ե��У��ڢݡ� �ʼ��Ե��У��ۢܡ� �����Ե��У��١�
��������ˮ���Ӱ�����ؼ�Ӧ��
1���������������
(1)����Խ�����������ӵ�ˮ��̶Ⱦ�Խ����Һ����Խǿ��
(2)����Խ�����������ӵ�ˮ��̶Ⱦ�Խ����Һ����Խǿ��
2������
(1)�ƶ���ˮ��̶�����
(2)Ũ��
����������Һ��Ũ�ȣ�ˮ��ƽ�������ƶ���ˮ��̶ȼ�С����ˮ�����������Ũ������ˮϡ�ͣ�ˮ��ƽ�������ƶ���ˮ��̶�����ˮ�����������Ũ�ȼ�С��
��������c(H)���⣬����ǿ�������ε�ˮ�⣻����c(OH��)�����ε�ˮ�⡣
3������ˮ���Ӧ��(д���ӷ���ʽ)
3��(1)������ˮ��Al��
��3H2O���Al(OH)3��3H��
3��(2)�Ʊ�Fe(OH)3���壺Fe��
����3H2O=====Fe(OH)3(����)��3H��
(3)����ĭ������Al��3HCO3===Al(OH)3����3CO2����
��(4)��ľ�����̬���ʻ�ʩ��NH4��
��2��CO3��H2O���NH3��H2O��HCO3��
���繹�� 3����
�ȵ����ͻ��
�ȵ㿼��
1.����ˮ�ⷽ��ʽ����д���жϡ�
2��ˮ��ƽ���Ӱ�������Լ�����Һ����Ե��жϺͱȽϡ�
3����Һ����Ũ�ȵĴ�С�Ƚϡ�
4������ˮ���ڻ����������ճ������е�Ӧ�á�
�ȵ�̽��
�ȵ�1�����ˮ��ĸ��ʵ��
1.����
����Һ���ε�����������Ӹ�ˮ��
�������������H��OH������������
�ʵķ�Ӧ�����������ˮ�⡣�����ˮ��ɿ���������кͷ�Ӧ���淴Ӧ��
2��ʵ��
�ε������������(���������ӻ�
��������������)��ˮ���������H��OH
��������������(���������)������ƽ�⣬ʹˮ�ĵ���ƽ�������ƶ���ʹ��
����Һ�е�c(H)��c(OH)������ȣ����ԣ���Һ��ʾ��һ�������Ի���ԡ�
3�����ɣ�����Ϊ��������ˮ�⣬������ˮ�⣬Խ��Խˮ�⣬����˫ˮ�⣬˭ǿ��˭�ԣ�ͬǿ�����ԡ���
˵�����١�Խ��Խˮ�⡱ָ�����ζ�Ӧ����(���)Խ����ˮ��̶�Խ����Һ����(������)Խǿ����CH3COOH�����Ա�HCNǿ������ͬŨ�ȵ�CH3COONa
����NaCN��Һ�У�CH3COO��ˮ��̶�
����CNС�����ߵļ���ǿ��
�ڡ�����˫ˮ�⡱ָ������������
�����ֱ���ˮ�����H��OH��ˮ�⣬��
ˮ���Ȼ��ٽ���˫ˮ������������һ������Ȼ�������ӵ�ˮ����ٽ�����ˮ��̶���Ȼ��С�����Ӽ���Դ���
����2��2�����棬��NH4��CO3��HCO3��S�ȣ�
��һ����ˮ�������ȫ�����Ӽ䲻�ܴ�
3�������棬�������ɳ��������壬��Al
����2��2��3����S��HCO3��CO3��AlO2��Fe��
������2��3��CO3��HCO3��AlO2��[��Al��3HCO3
===Al(OH)3����3CO2��]��
4��Ӱ������ˮ�������
(1)����
����ˮ��̶ȵĴ�С����Ҫ���εı�������������ν��Խ��Խˮ�⡱��
(2)����
���¶ȣ��ε�ˮ�ⷴӦ�����ȷ�Ӧ����ˣ��¶�����ˮ��̶�����
��Ũ�ȣ��ε�Ũ��ԽС��ˮ��̶�Խ��
��������ܴٽ��������ε�ˮ�⡣
5��ˮ�ⷽ��ʽ����д
(1)һ������ˮ��̶Ⱥ�С��ˮ�����Ҳ���٣�����д����ˮ�ⷽ��ʽʱҪд����𡱣����ﲻ�ꡰ��������������������(��NH3��H2O��H2CO3��)д����ֽ�������ʽ��
(2)��Ԫ�����ε�ˮ���Ƿֲ����еģ���һ����������ˮ��ʱ�Ե�һ��Ϊ����һ��ֻд��һ��ˮ������ӷ���ʽ�����磺Na2CO3ˮ������ӷ���ʽд
����2������CO3��H2O���HCO3��OH��
(3)��Ԫ���������ӵ�ˮ��ʵ��Ҳ�Ƿֲ����еģ�����ѧ�ζಽ��Ϊһ����
3�����磺FeCl3ˮ���дΪFe��
��3H2O���Fe(OH)3��3H��
(4)�ܳ���ˮ��������飬���ڲ��γ�ˮ��ƽ�⣬��дʱҪ�á�===���������������ȣ���NaHCO3
��3����Һ��AlCl3��Һ��ϣ�Al��3HCO3
===Al(OH)3����3CO2����
����1�� ��һ�������£�Na2CO32����Һ����ˮ��ƽ�⣺CO3��
H2O���HCO3��OH������˵����ȷ����( )
A��ϡ����Һ��ˮ��ƽ�ⳣ������
B��ͨ��CO2��ƽ�⳯����Ӧ�����ƶ�
��c?HCO3?C�������¶ȣ�2����С c?CO3?
D������NaOH���壬��ҺpH��С
[����] ˮ��ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ�����䣬A����
��ȷ��ͨ��CO2��������ӦCO2��2OH
��2��===CO3��H2O��OH��Ũ�Ƚ��ͣ�ƽ��
������Ӧ�����ƶ���B��ȷ��ˮ�ⷴӦ
��c?HCO3?���ȣ������¶ȣ�2��c?CO3?
����C����ȷ������NaOH���壬OH��Ũ��������ҺpH����D����ȷ��
[��] B
��ʽ1 ������0.1 mol/L CH3COONa��Һ�зֱ��������NH4NO3��Na2SO3��FeCl3����(������Һ
������仯)����CH3COOŨ�ȵı仯������
��Ϊ( )
A����С������С B������С����С
C�������������� D������������
����������ˮ�⣬NH4NO3��Na2SO3��FeCl3�ֱ������ԡ����ԡ����ԣ�
�������Ի�ٽ�CH3COO��ˮ�⣬ʹ
��c(CH3COO)��С������������ƣ���CH3COO��ˮ�⣬ʹc(CH3COO)���� �𰸣�A
�ȵ�2����ˮ���Ӧ��
1.�ж�����Һ�������
2����Na2CO3��Һ��CO3��ˮ�����
�����ԣ�NH4Cl��Һ��NH4��ˮ�������
�ԡ�
2����������Һ
3����������FeCl3��Һʱ������Fe
��ˮ��ʹ��Һ���Ƕ��ò���������Һ����������ʱ��Ҫ����һ������HCl����
3����Fe��ˮ�⡣ͬ��������FeSO4��SnCl2
����ҺʱҲ��Ҫ������Ӧ����������ˮ�⡣
3���Ƚ�����Һ�е�����Ũ�ȴ�С ��NH4Cl��Һ�и�����Ũ�ȵĴ�С
����˳���жϣ�NH4��H2O���NH3��H2O��H��
���������ˮ�⣬��Һ��c(NH4)��c(Cl)��
��������ˮ��Ĵ��ڣ�c(NH4)���ͣ���ͬ
������ʱ������һ������H��c(H)>c(OH)��
������������c(Cl)>c(NH4)>c(H)>c(OH)��
4������ijЩ�ε��Ʊ�����
��AlCl3���Ʊ�������ͨ��������Һ��Ũ���ᾧ�ķ�������Ϊ�¶����ߣ�ˮ��̶���������Al(OH)3���������������գ�Al(OH)3���ֽ�����Al2O3��
5����ѧ���ϵ�ʩ��
���ԵĻ�ѧ���ϲ��ܺͼ��Է��ϻ��ã�������狀Ͳ�ľ��(��Ҫ��Ч�ɷ�ΪK2CO3)���ܻ��ʩ�ã���NH4NO3ˮ�������ԣ�K2CO3ˮ���Լ��ԣ���Ͻ��ٽ�ˮ�⣬���ͷ�Ч��
6���εľ�ˮ����
3����������ˮ��ԭ����Al����ˮ��
��Ӧ��Al��3H2O���Al(OH)3��3H��������״������������������ˮ�е�������Ӷ�ʹˮ���塣
7�������е�Ӧ��
���ô�����Һϴ�����ۡ���Ϊ������Ҫ���������ʣ�Na2CO3ˮ��ʹ��Һ�Լ��ԣ�����������������ˮ����������ˮ�Ĵ��������ƣ�����ʹNa2CO3ˮ��̶�������Һ������ǿ�����ȵĴ�����Һϴ��Ч������ĺá�
����2�� ���Ȼ�����Һ�д�������ƽ�⣺
FeCl3��3H2O���Fe(OH)3��3HCl����H>0
(1)������FeCl3��Һ��������ڵ�����ˮ�пɵõ�һ�ֺ��ɫ��Һ�塣������Һ���м���ϡH2SO4����������Ϊ
________________________________________________________________________��
(2)���ϼ���FeCl3��Һ��������ˮ3����
�ֲ����յõ��Ĺ��������________________________________________________________________________��
(3)������FeCl3��Һʱ��Ϊ��ֹ�������ǣ�Ӧ________________________________________________________________________��
(4)��FeCl3��Һ�м�������Ũ��������Һ��Ԥ�ƿ��ܿ�����������________________________________________________________________________��
[����] ��FeCl3��Һ������ڵ�����ˮ�У��õ�Fe(OH)3���壬����ϡH2SO4����۳����õ����ɫ��������H2SO4����ʱ�������ܽ����ɻ�ɫ��Һ��
(2)���ȿɴٽ�����ˮ�⣬����HCl�ӷ�����ʹˮ����г��ף��õ�Fe(OH)3������Fe(OH)3���ȷֽ⣬���ղ���ΪFe2O3��
(3)Ϊ��ֹFeCl3ˮ�⣬Ӧ����Ũ��������FeCl3ˮ�⡣
[��] (1)�����ɺ��ɫ�����������ܽ����ɻ�ɫ��Һ (2)Fe2O3 (3)��������Ũ���� (4)�������ɫ����������Һ��Ϊ��ɫ
��ʽ2 (1)Na2CO3��Һ�е����̪�ʺ�ɫ��ԭ����(�����ӷ���ʽ��ʾ)__________________________�����Ⱥ���ɫ��________(���dz)��ԭ����_____________________________________��
(2)���ڸ���Һ���ٵ���������Ȼ�����Һ�����۲쵽��������________����ԭ����(�����ӷ���ʽ�ͼ�Ҫ����˵��)________________ ___________________��
��2���𰸣�(1)CO3��H2O���HCO3��OH
�� �� ���¶����ߣ�ˮ��ƽ������
��c(OH)��������ǿ������Һ�ĺ�ɫ����
(2)������ɫ�������Һ�ɫ��ȥ ��
2��2����BaCl2��Ba��CO3===BaCO3��(��
2��2��ɫ)������c(CO3)��С��CO3ˮ��ƽ��
�����ƣ�c(OH)��С����Һ����ɫ
�ȵ�3��Һ����Ũ�ȵĴ�С�Ƚ�
1.����Һ�����Һ
������Һ��������Ũ�ȼ�c(H)���
������Һ������������Ũ�ȼ�c(OH)��
����������Ũ��Ӧ��������ĵ���̶ȱȽϡ���Ԫ������Ԫ�����Ե�һ������Ϊ����
���磺H2S�и�����Ũ�ȱȽ�Ϊ��c(H������2��)>c(HS)>c(S)>c(OH)��
2������Һ
(1)��Ԫ�����������ӺͶ�Ԫ����������Ӷ��Ƿֲ�ˮ�⣬���Ե�һ��ˮ��Ϊ����
���磺NH4Cl��Һ�У�c(Cl��������)>c(NH4)>c(H)>c(OH)��
(2)��ȷ��ʽ������ӵ���̶ȡ�ˮ��̶ȵ���Դ�С��
��������ʽ���У�NaHSO3��NaH2PO4�Ե���Ϊ������Na2HPO4��������ʽ��һ����ˮ��Ϊ�����磺
NaHCO3��Һ�У�c(Na��������2��)>c(HCO3)>c(OH)>c(H)>c(CO3)��
(3)�Ƚ�ͬһ���ӵ�Ũ��ʱ��Ҫע���������ӶԸ����ӵ�Ӱ�졣
�����磺����Һ��c(NH4)�Ƚ�Ϊ��
c(NH4HSO4)>c(NH4Cl)>c(CH3COONH4)��
3��������õ���غ�������غ�
(1)����غ�
�������Һ������������������������������������������������������
�����磺NaHCO3��Һ��c(H)��c(Na
������2��)��c(HCO3)��2c(CO3)��c(OH)��
(2)�����غ�
�������Һ�У�ͬ��Ԫ�ص�ԭ�������غ�ġ�
��1���磺0.1 mol��L��NaHCO3��Һ
�У�
����2��c(Na)��c(HCO3)��c( CO3)��
��1c(H2CO3)��0.1mol��L��
ע�⣺��Щ���������Ũ�ȹ�ϵ���ɵ���غ��ϵʽ�������غ��ϵʽ��
�����ó�������NaHCO3��Һ��c(H)��
��2��c(CO3)��c(OH)��c(H2CO3)��ϵʽ����
����3(1)��(2)�е�������ϵʽ����ó���
����3�� ������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����( )
��1A�������£���0.01 mol��L
NH4HSO4��Һ�еμ�NaOH��Һ����
������2���ԣ�c(Na)>c(SO4)>c(NH4)>c(OH)����c(H)
��1B��0.1 mol��L NaHCO3��Һ��c(Na
��������)>c(OH)>c(HCO3)>c(H)
����C��Na2CO3��Һ��c(OH)��c(H)��
��c(HCO3)��2c(H2CO3)
D��25��ʱ��pH��4.75��Ũ�Ⱦ�Ϊ
0.1 mol��L��CH3COOH��CH3COONa
�������Һ��c(CH3COO)��c(OH
����)<c(CH3COOH)��c(H)
[����] Aѡ������Һ�����ԣ���c(H)��c(OH)��
�ݵ���غ�ԭ���У�
��������c(Na)��c(H)��c(NH4)��c(OH)��2��2c(SO4)
����2������c(Na)��c(NH4)��2c(SO4)
����2������NH4ˮ��ʹc(NH4)<c(SO4)����2���Ӷ���c(Na)>c(SO4)��A��ȷ��
Bѡ����NaHCO3��Һ�Լ��ԣ�������c(OH)��c(HCO3)С��B����ȷ�� Cѡ������Na2CO3��Һ�У��������غ��
������c(OH)��c(H)��c(HCO3)��2c(H2CO3)
����������c(OH)��c(H)��c(HCO3)��
2c(H2CO3)��C��ȷ��
Dѡ����pH��4.75��˵��c(H����)>c(OH)
��������c(Na)��c(H)��c(CH3COO)����1
c(OH)
��������c(Na)<c(CH3COO)��
��������֪��2c(Na)��c(CH3COO)��
c(CH3COOH)
����c(Na)>c(CH3COOH)
���������c(Na)��c(H)��c(CH3COO)����c(OH)
����c(CH3COOH)��c(H)<c(CH3COO
����)��c(OH)��D����ȷ��
[��] AC
��ʽ3 ����Ũ�ȹ�ϵ��ȷ����
( )
��A����ˮ�У�c(Cl2)��2[c(ClO)��c(Cl
��)��c(HClO)]
����B����ˮ�У�c(Cl)>c(H)>c(OH
����)>c(ClO)
C���������Ũ�ȵ��������������
������ϣ�c(Na)��c(CH3COO)
D��Na2CO3��Һ�У�c(Na��������2��)>c(CO3)>c(OH)>c(HCO3)>c(H)
1��������A��ˮ�У�c(Cl2)��2c(ClO)��
��c(Cl)��c(HClO)]����c(H)>c(Cl)��
A��B������ȷ���������Ũ�ȵ���������������ϣ��õ���������Һ������
������CH3COOˮ�⣬ʹc(Na)>c(CH3COO)��C����ȷ��
�𰸣�D
�������ɼ���
��ˮ���ε���ȡ������Һ������
1��������Һ
Ҫ����һЩ������ˮ������Һʱ����Ϊ�ε�ˮ����ʻ��ǣ�����������������Ӧ��������ˮ�⡣������FeCl3��Һʱ��ͨ���Ƚ����ܽ���Ũ�����У��ټ�ˮϡ���Եõ��������Һ��
2�������Ȼ���(��MgCl2��AlCl3��FeCl3��CuCl2��)���Ʊ�
AlCl3��FeCl3��һЩ��ˮ��������Ʊ�ʱҪ��ֹˮ�IJ��롣����Ҫ���ǵ���ˮ��������˶�ʵ��װ�õ�˳���Ӷ��������Ҫ�� ������
(1)��Ӧԭ��(��AlCl3Ϊ��)2Al����2AlCl3�� 3Cl3=====
(2)ʵ�鷽�� װ����ͼ��
�����Ӻ�װ�ã����װ�õ������ԡ�
(�������������ܵ�һ�˲���ˮ�У��رշ�Һ©���������þƾ��Ƹ���ƿ����)
��װ��ҩƷ���ȵ�ȼ��߾ƾ�����ȡ������
���Ժ��ȼ�ұ߾ƾ��ơ�
(3)ע������
��Ϊ��ֹ��ȡ���Ȼ����ˮ�⣬ͨ�������������Ӧ�ܺ�Ӹ����(��������ü�ʯ�һ���ʯ�ҡ��ռ����)��
�ڱ������������ž�װ���ڵĿ������ٵ�ȼE���ƾ��ơ�
�۸���ܵ����ã�һ�Ƿ�ֹˮ�������룬���������ж���������
�������� ��ҵ�Ʊ��Ȼ�ͭʱ����
Ũ����������������80 �����ң����������(CuO)��ĩ(������Fe2O3��FeO)����ֽ��裬ʹ֮�ܽ⣬��һǿ���ԵĻ����Һ�������Ӹû����Һ���Ʊ�������CuCl2��Һ���������²���[�ο����ݣ�
2��pH��9.6ʱ��Fe��ȫˮ���Fe(OH)2��
2��pH��6.4ʱ��Cu��ȫˮ���Cu(OH)2��
3��pH��3.7ʱ��Fe��ȫˮ���Fe(OH)3]��
��ش��������⣺
2��(1)��һ����ȥFe���ܷ�ֱ�ӵ���
2��pH��9.6����Fe������ȥ��________��
������____________________________������
2��3����ǿ������NaClO��Fe����ΪFe��
�ټ���NaClO����Һ��pH�仯��________(�����)��
A��һ������ B��һ����С
C���������� D�����ܼ�С
������Ϊ��NaClO���������Ƿ�����________��������___________________________________��
�������м��ֳ��õ�������������
2���ڳ�ȥ�����Һ��Fe����________(��
����ѡ�����������)��
A��ŨHNO3 B��KMnO4 C��Cl2
D��O2 E��H2O2
3��(2)��ȥ��Һ��Fe�ķ����ǵ�����
Һ��pH��3.7�����������Լ���������ʹǿ������Һ��pH������3.7����ѡ�õ���________(��ѡ����)��
A��NaOH B����ˮ
C��Cu2(OH)2CO3 D��Na2CO3 E��CuO F��Cu(OH)2
[����] �����ۺ���ǿ������˼ά�������Ժ�ǰ��֪ʶ����ϵ���������֪��2��Fe������pH��9.6�����ֱ�ӵ���pH
2��3��2����9.6��Cu��Fe����Fe����(������
2�����ӳ�����pH����Fe������pHС)��
2���ʲ���ֱ�ӵ���pH��9.6���ɽ�Fe����
3��2����Fe��NaClO��������������Fe��
����2��3����Ӧ��2Fe��ClO��2H===2Fe��Cl
������H2O�����ڷ�Ӧ������Ҫ����H����
2��ҺpHһ�����ߡ�NaClO���Խ�Fe��
����Fe����������������Na��ʵ��
2���ϲ��ܲ��á�����Ӧ�ü�������Fe��
�����������ʵ�������������Cl2��O2��H2O2��ͬ��������pH���Լ�CuO��Cu2(OH)2CO3��Cu(OH)2�Ȳ������������ʡ�
2��[��] (1)���� ��Fe������pH
2��2��3�����Fe������ȫʱ��Cu��Fe�������ȫ ��A �ڲ��� ���������ʣ�Na CDE (2)CEF
��ʽ ����˵����ȷ����( )
A��AlCl3��Һ��NaAlO2��Һ���ȡ�������Ũ�����ᾧ�����գ����ù���ijɷ���ͬ
B������FeCl3��Һʱ����FeCl3�����ܽ��������У�Ȼ������ˮϡ�͵������Ũ��
C���ü��ȵķ����ɳ�ȥKNO3��Һ
3���л��е�Fe
D����ĭ������г�ʹ�õ�ԭ����̼���ƺ�������
������AlCl3��Һ��NaAlO2��Һ��3����
ˮ�ⷽ��ʽ�ֱ�ΪAlCl3��3H2O���Al(OH)3��3HCl��NaAlO2��2H2O���Al(OH)3��NaOH�����ȴٽ�ˮ�⣬���������ǻӷ����ᣬ���ǰ�����ղ���ΪAl2O3��������ΪNaAlO2��ѡ��A����ѡ��B�к���Ȼ����õ�FeCl32����Һ�л�������SO4����˲������⡣
��3������Fe��3H2O���Fe(OH)3��3H����
���¶ȿɴٽ�ˮ��������������Ӷ���
3��ȥFe���ʣ�C��ȷ��ѡ��D�У�Ϊ�˼ӿ����CO2��������ʣ���ĭ������г�ʹ�õ�ԭ����̼�����ƺ���������
�𰸣�C
��ѡϰ��
1.(2010���ɶ������¿�)���з�Ӧ������ˮ�ⷴӦ��ˮ�ⷽ��ʽ����ȷ����
( )
������HCl��H2O���H3O��Cl
��AlCl3��3H2O===Al(OH)3��3HCl ��Na2CO3��2H2O���H2CO3��
2NaOH
����̼��������Һ��HCO3��
��2��H2O���CO3��H3O
����NH4Cl����D2O��NH4��
��D2O���NH3��D2O��H
A���٢ڢۢ� B���٢ڢ�
C���ڢۢ� D��ȫ��
�������٢��ǵ��룻����ˮ�ⷴӦ����Ӧ�á���𡱣��۵�ˮ�ⷽ��ʽ����
��Ӧ�ֲ����У���ӦΪNH4��
��D2O���NH3��HDO��D��
�𰸣�D
2������˵����ȷ����( )
A��25 ��ʱ��pHΪ9��Na2CO3��Һ��pHΪ5��FeCl3��Һ�У�ˮ�ĵ���̶Ȳ�ͬ
3��B���ں���Fe��KNO3��Һ�У���
3��ͨ�����ȵķ�����ȥFe��֤���ε�ˮ
�������ȷ�Ӧ
C��25 ��ʱ������������ʵ���Ũ�ȵ�NaCl��NaClO��Һ�����������������
D�������ʵ���Ũ�ȵĢ�NH4Cl����NH4HSO4����Na2S����NaNO3����pH�ɴ�С������Ϊ��>��>��>��
������A�У�Na2CO3��FeCl3��ˮ�⣬�ٽ�ˮ�ĵ��룬pHΪ9��Na2CO3
����5��Һ�У���ˮ���������c(OH)��10
��1mol��L��pHΪ5��FeCl3��Һ�У���ˮ
����5��1���������c(H)��10 mol��L������
��ˮ�ĵ����Ӱ��Ч�����൱�ģ�B�У�
��3��Fe��3H2O���Fe(OH)3��3H������
Fe(OH)3�����������ӣ��������
3��Fe(OH)3�������Ӷ���ȥFe��C��ClO
������ˮ��ClO��H2O���HClO��OH��ClO������ˮ��������OH����������c(OH������14��)��c(H)��10��������Һ��c(OH)��
����c(H)��Ȼ��С����NaClO��Һ������������������NaCl���١�D�У���������ˮ����ɿ�֪��Na2S��Һˮ��ʼ��ԣ�NH4Clˮ������ԣ�NaNO3��ˮ��
�������ԣ�NH4HSO4��Һ�У�HSO4�����
����Hʹ��Һ��ǿ���ԣ������ǵ�pH�ɴ�С��˳��Ϊ��>��>��>�ڡ�
�𰸣�BD
���������ֵ������Һ��pH��С�Ƚ�������һ����ɣ�(1)ǿ�������Σ���Խ������Һ����Խǿ������ǿ���Σ���Խ������Һ����Խǿ��(2)ͬ���ʵ���Ũ�ȵĶ�Ԫ���ἰ������Һ��pH��ϵ�ǣ���H3PO4Ϊ����H3PO4<NaH2PO4<Na2HPO4<Na3PO4��
3����4�ֻ����Һ���ֱ��ɵ����
��10.1 mol��L��2����Һ��϶��ɣ���CH3COONa��HCl����CH3COONa��NaOH����CH3COONa��NaCl����CH3COONa��NaHCO3
���и���������ȷ����( )
A��pH����>��>��>��
��B��c(CH3COO)����>��>��>��
��C����Һ��c(H)����>��>��>��
D��c(CH3COOH)����>��>��>�� ����������������Һ��Ӱ��ˮ������ء����ֻ����Һ����CH3COONa�����ֻ��Ƚ����������ʶ�CH3COONa
��ˮ���Ӱ�켴�ɡ�CH3COO��
H2O���CH3COOH��OH���Լ��ԣ���ˮ���ܴٽ��̶ȣ�HCl>NaCl>NaHCO3>NaOH�������Ƴ̶��෴��
����CH3COONa��HCl===NaCl��CH3COOH����Һ�����ԣ�pH��С��
����>��>��>�٣�A����pH����lgc(H)��
����c(H)��С˳����pH˳���෴������<��<��<�٣�C�������ݡ�����������
�����жϢ���CH3COOŨ����С��
��c(CH3COO)��С����>��>��>�٣�B�ԡ�
������Ԫ���غ㣬c(CH3COO)Խ����
c(CH3COOH)ԽС����c(CH3COOH)Ϊ����>��>��>�ڣ�D����
�𰸣�B
4����������£����Դ����������������( )
��2��A�����ڴ���AlO2����Һ�У�Fe��
����2��NO3��SO4��Na
����14B����ˮ�����c(H)��1��10
��1������2��mol��L����Һ�У�Ba��K��Cl��HCO3
C��������Ӧ�ų�������������Һ��
��2��2����NH4��SO4��CO3��Na
����12��D����c(H)/c(OH)��10����Һ�У�
����3��2��NH4��Al��Ca��Cl
���������⿼�����ӹ������⡣��
���ڴ�����AlO2��˵����Һ�Լ��ԣ�����
2��Feˮ�������ԣ�����Aѡ�����Bѡ�����Һ���������ԣ�Ҳ�����Լ��ԣ�
��HCO3�Ȳ�������������棬Ҳ�������
�������棬Bѡ�����������Ӧ�ų���������Һ������������Һ��Ҳ������
����������Һ��NH4������OH�������棬
��2��CO3������H�������棬Cѡ�����
�𰸣�D
5��(2010������)�����£���0.1000 ��1mol��L NaOH��Һ�ζ�20.00 mL0.1000
��1mol��L CH3COOH��Һ���õζ�������
ͼ��ʾ������˵����ȷ����(
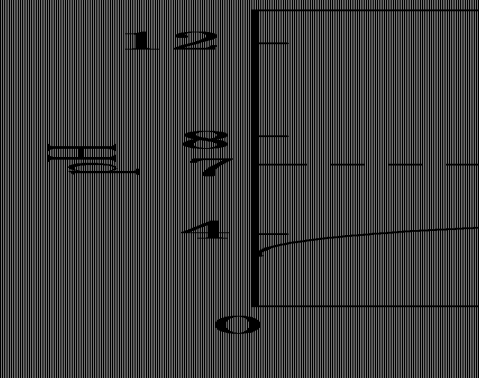
)
A�������ʾ��Һ�У�
��c(CH3COO)��c(OH ��)��
c(CH3COOH)��c(H)
B�������ʾ��Һ�У�
��c(Na)��c(CH3COOH)��c(CH3COO��)
C�������ʾ��Һ�У�
��������c(Na)>c(OH)>c(CH3COO)>c(H)
D���ζ������п��ܳ��֣�
��c(CH3COOH)>c(CH3COO)>c(H
������)>c(Na)>c(OH)
���������⿼����Һ�еĵ���غ㡢�����غ�������غ�ȹ�ϵ�����ڿ��鿼������������������غ��ϵ��������A����ݵ���غ��ϵ�У�
��������c(CH3COO)��c(OH)��c(Na)��c(H)��
����ʱ��Һ�е�c(CH3COOH)��c(Na)��
��ȣ��ʲ���ȷ��B������Һ�����ԣ������������������Һ�����С��20 mL����ʱ���������غ��֪c(Na����)<c(CH3COO)��c(CH3COOH)���ʲ���ȷ��C������Һ������ǡ����ȫ��Ӧ����Һ�и�����Ũ�ȹ�ϵӦΪ��c(Na��������)>c(CH3COO)>c(OH)>c(H)���ʲ�����
ȷ��D����ռ�����������������Һʱ���ܻ�����������������ȷ��
�𰸣�D
6����������A��B��C��D������ɫ��Һ�����Ƿֱ���CH3COONa��Һ��NH4Cl��Һ��HCl��Һ��Na2SO4��Һ�е�һ�֡�
(1)��֪A��B��Һ��ˮ�ĵ���̶���ͬ��A��C��Һ��pH��ͬ��A��__________��Һ��B��__________��Һ��C��__________��Һ��D��__________��Һ��
(2)A��Һ�и�����Ũ�ȴ�С�Ĺ�ϵ��(�ò��Ⱥ�����)____________________________________��
������CH3COONa��Һ�Լ��ԣ��ٽ�ˮ�ĵ��룻NH4Cl��Һ�����ԣ��ٽ�ˮ�ĵ��룻���������ԣ�����ˮ�ĵ��룻Na2SO4��Һ�����ԣ���ˮ�ĵ�����Ӱ�졣ͨ����������֪A��NH4Cl��Һ��B��CH3COONa��Һ��C�����D��Na2SO4
��Һ��NH4Cl��Һ����NH4ˮ�⣬ʹ��
����Һ�����ԣ���c(Cl)>c(NH4)>c(H
����)>c(OH)��
�𰸣�(1)NH4Cl CH3COONa HCl Na2SO4
��������(2)c(Cl)>c(NH4)>c(H)>c(OH) ��
- �����ˮ��֪ʶ��(ѧ����)
-
�����ˮ��֪ʶ��
�����ˮ��һ����ˮ���Һ��cHcOH���Գ�����pH7cHltcOH���Գ�����pHgt7cHltcOH���Գ�����pHlt7ʵ��ȡ�١�
-
�����ˮ��֪ʶ��
�����ˮ�������г��õ�NaCl�Ȱ�����ζ��Na2CO3NaHCO3�ȶ���������NaCl�Ȱ�������Ҫ����ʳƷ��ζ��Na2CO3Na��
- 20xx���л�ѧ֪ʶ������ȫ �����ˮ��
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
-
��ѧѡ��4�����µ����ڡ������ˮ�⡷֪ʶ�ܽ�
��ѧѡ���ĵ����µ�3�ڡ������ˮ�⡷֪ʶ�ܽ�һ��̽������Һ�������ǿ�������ε�ˮ��Һ���ʼ��ԣ�ǿ�������ε�ˮ��Һ�������ԣ�ǿ��ǿ�
-
���л�ѧѡ��4������ˮ��Һ�е�����ƽ��֪ʶ��������ܽ�
ˮ��Һ�е�����ƽ��1֪ʶҪ��һ������ʵĵ���1�������ʷǵ����ǿ�����������ʻ����ǿ�����ǿ��ǿ�����������������������HC��
-
���˽̰桿���л�ѧѡ��4֪ʶ���ܽ������ˮ��Һ�е�����ƽ��
������ˮ��Һ�е�����ƽ��һ������ʵĵ���α�Ҫ��1�˽����ʺͷǵ����ǿ����ʺ�������ʵĸ���2����������ʵĵ���ƽ��3���������⡭
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
- ����ˮ��֪ʶ���ܽ�