四川理工实验报告电导法测定乙酸电离平衡常数 (2)
实验六 电导法测定乙酸电离平衡常数
报告人:曾辉 实验时间20##年03月07日
一.实验目的:
1.掌握电导、电导率、摩尔电导率的概念以及它们之间的相互关系。
3.掌握电导法测定弱电解质电离平衡常数的原理。
二.实验原理:
1.电离平衡常数Kc的测定原理
在弱电解质溶液中,只有已经电离的部分才能承担传递电量的任务。在无限稀释的溶液中可以认为弱电解质已全部电离,此时溶液的摩尔电导率为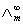 ,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率
,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率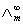 是有区别的,这由两个因素造成,一是电解质的不完全离解,二是离子间存在相互作用力。二者之间有如下近似关系:
是有区别的,这由两个因素造成,一是电解质的不完全离解,二是离子间存在相互作用力。二者之间有如下近似关系:
 (1)
(1)
式中为弱电解质的电离度。
对AB型弱电解质,如乙酸(即醋酸),在溶液中电离达到平衡时,其电离平衡常数Kc与浓度c和电离度α的关系推导如下:
CH3COOH →CH3COO- + H+
起始浓度 c 0 0
平衡浓度 c(1-α) cα cα
则
Kc=ca2/(1-a) (2)
以式(1)代入上式得: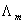 c= c
c= c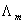 2/[
2/[ 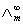 (
(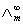 -
- 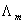 )] (3)
)] (3)
因此,只要知道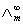 和
和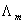 就可以算得该浓度下醋酸的电离常数Kc。
就可以算得该浓度下醋酸的电离常数Kc。
将式(2)整理后还可得:
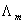 c=
c=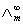 2Kc(1/
2Kc(1/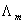 ) -
) - 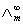 Kc
Kc
(4)
由上式可知,测定系列浓度下溶液的摩尔电导率∧m,将∧mc对1/Λm作图可得一条直线,由直线斜率可测出在一定浓度范围内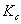 的平均值。
的平均值。
2.摩尔电导率∧m的测定原理
电导是电阻的倒数,用G表示,单位S(西门子)。电导率则为电阻率的倒数,用k表示,单位为S·m-1。
摩尔电导率的定义为:含有一摩尔电解质的溶液,全部置于相距为1m的两个电极之间,这时所具有的电导称为摩尔电导率。摩尔电导率与电导率之间有如下的关系。
∧m= K/c (5)
式中c为溶液中物质的量浓度,单位为mol·m-3。
在电导池中,电导的大小与两极之间的距离l成反比,与电极的面积A成正比。
G =KA/ l (6)
由(6)式可得
κ=lG/A=KcellG (7)
对于固定的电导池,l和A 是定值,故比值l/A为一常数,以Kcell表示,称为电导池常数,单位为m-1。为了防止极化,通常将铂电极镀上一层铂黑以增大表面积,因此真实面积A无法直接测量,通常将已知电导率κ的电解质溶液(一般用KCl溶液)注入电导池中,然后测定其电导G,即可由(7)式算得电导池常数Kcell。
当电导池常数Kcell确定后,就可用该电导池测定某一浓度的醋酸溶液的电导,再用式(7)算出κ,将c、κ值代入(5)式,可算得该浓度下醋酸溶液的摩尔电导率。
在这里,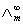 的求测是一个重要问题,对于强电解质溶液可测定其在不同浓度下摩尔电导率,再外推而求得,但对弱电解质溶液则不能用外推法,通常是将该弱电解质正、负两种离子的无限稀释摩尔电导率加和计算而得,即:
的求测是一个重要问题,对于强电解质溶液可测定其在不同浓度下摩尔电导率,再外推而求得,但对弱电解质溶液则不能用外推法,通常是将该弱电解质正、负两种离子的无限稀释摩尔电导率加和计算而得,即:
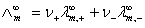 (8)
(8)
不同温度下醋酸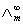 的值见表2.5。
的值见表2.5。
表2.5 不同温度下醋酸的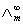 (S·m2·mol-1)
(S·m2·mol-1)

三.仪器与试剂:
DDBJ-350便携式电导率仪,电导电极,恒温槽,烧杯、锥型瓶,移液管(25mL);
0.0200 mol·L-1 KCl标准溶液,0.200 mol·L-1 HAc标准溶液
四.实验步骤:
1.调节恒温水槽水浴温度至25℃(室温偏高,则水浴温度调节到35℃)。将实验中要测定的溶液和一定量的蒸馏水恒温。
2.校准便携式电导率仪的电导池常数
按下电导率仪“on/off”键打开仪器,按“▲”或“▼”键到CON(通常打开即是此模式),按“模式/测量”键到模式状态,按“▲”或“▼”键调节模式状态,至左下角出现CONT,按“▲”或“▼”键至左下角出现CAL,按“确定”键,左下角出现CA-M,按“▲”或“▼”键调节0.02mol/L的KCl溶液的电导率大小至0.276 S/m(35℃时为 0.331 S/m ),按“确定”键出现标定好的电导池常数,再按“确定”键输入电导池常数。按“模式/测量”键到测量状态。
3.测量醋酸溶液的电导率
标定好电导池常数后,将两电极用蒸馏水洗净,用吸水纸吸干液体。处理好的电极插入到25mL0.2 mol/L醋酸溶液中测量电导率。再用标有“电导水”字样的移液管吸取25mL水并注入到醋酸溶液中稀释到0.1 mol/L。此时不要将电极取出。测量后,用标有“0.1”字样的移液管吸取25mL溶液弃去,用标有“电导水”字样的移液管吸取25mL水并注入到醋酸溶液中稀释到0.05 mol/L,摇匀后测量电导率。如此依次测定0.2 mol/L、0.1 mol/L、0.05 mol/L、0.025 mol/L、0.0125 mol/L醋酸溶液的电导率。
记录相应浓度醋酸的电导率,并计算电离度和解离常数。
4.用蒸馏水清洗电导电极和温度传感器,将电极浸泡在盛有蒸馏水的锥形瓶中,以备下一次实验用。
五.数据处理:
1.将原始数据及处理结果填入下表:
实验温度: T=25℃
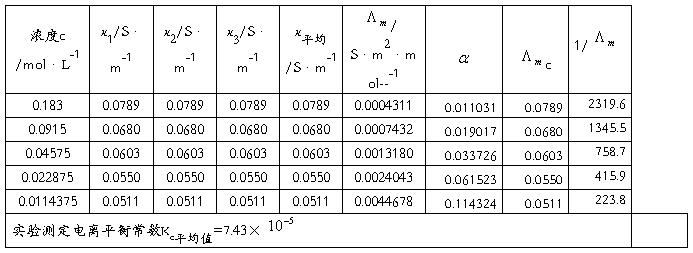
2.根据测得的各种浓度的醋酸溶液的电导率,求出各相应的摩尔电导率∧m和电离度a及电离平衡常数Kc。
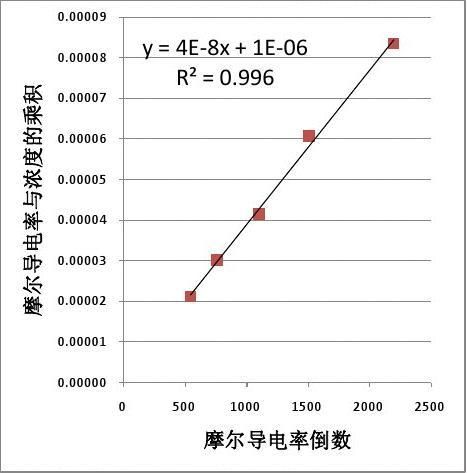
3.用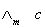 对1/∧m作图或进行线性回归,求出相应的斜率和截距,求出平均电离常数Kc
对1/∧m作图或进行线性回归,求出相应的斜率和截距,求出平均电离常数Kc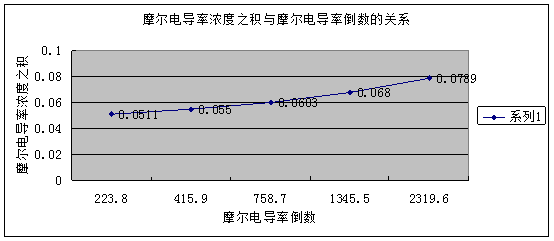
由图知,直线斜率为1.13×10-7 ,又因为斜率表示为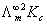 所以可得:
所以可得: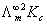 =1.13×10-7 ,得
=1.13×10-7 ,得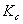 =7.43×
=7.43×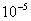
六.注意事项:
1.计算∧m和kc时,需注意浓度c单位的区别,详见原理部分。
2.温度对溶液的电导(或电阻)影响较大,因此测量时应保持恒温。
七.思考题:
1.电导池常数是否可用测量几何尺寸的方法确定?
答:不能。测定电导池常数可以用标准溶液测定法,用氯化钾为标准物质;还可以用与标准电极比较法测定。
2.实际过程中,若电导池常数发生改变,对平衡常数测定有何影响?
答:溶液电导经测定后,则与Kcell成正比。当电导池常数测值偏大,那么算得的溶液的溶解度、电离常数都偏大,反之,电导池常数测值偏小,则电离常数偏小。
八.实验总结:
通过本次的操作实验,我知晓了一个道理:大型的实验都不是一个人能够完成的,它需要多个人合作去共同完成,他考究了众人在操作中的团结和分配,各司其职。
第二篇:导电法测定乙酸电离平衡常数-数据处理表-四川理工学院
浓度c
κ1/S·κ2/S·κ
3/S·κ平均/S· / S·m2·
m
-1
?m
-1
m
-1
m
-1
m
-1
mol
0.1830.09150.045750.0228750.01143750.08350.06060.04150.03010.02130.08330.06080.04150.03020.02110.08350.06070.04170.03030.02110.0834330.0607000.0415670.0302000.0211674.55920E-046.63388E-049.08561E-041.32022E-031.85064E-03
实验测定电离平衡常数Kc平均值 =2.62563E-05
说明:
色部分为数据填入部分
E表示科学计数法的10,其他部分能自动生成,但是KC需要大家手动计
/ S·m·
-1mol
3.80389E-11
4.02677E-11
3.77659E-11
3.98706E-11
3.91718E-11?2m2?1.16663E-021.69751E-022.32487E-023.37825E-024.73551E-02Kc1/?mc0.000080.000060.000040.000030.000022.52009E-0521932.68215E-0515072.53166E-0511012.70190E-057572.69236E-05540
8?2斜率表示 (=4×10?Kmc
Kc=2.6191E-05
成,但是KC需要大家手动计算一下!
-
实验四 醋酸解离常数的测定
实验四醋酸解离常数的测定一pH法一实验目的1学习溶液的配制方法及有关仪器的使用2学习醋酸解离常数的测定方法3学习酸度计的使用方法二…
-
无机化学实验六 醋酸电离度和电离常数的测定1
实验六醋酸电离度和电离常数的测定pH法一实验目的1测定醋酸的电离度和电离常数2学习pH计的使用教学重点醋酸的电离度电离常数的测定教…
-
电导法测定乙酸电离平衡常数 实验报告
物理化学实验报告姓名何思思班级工艺五班学号教师李慎新学院材料化学与工程学院10031010526电导法测定乙酸电离平衡常数一实验目…
-
醋酸电离度和电离常数的测定
实验题目醋酸电离度和电离常数的测定教材p5759一实验目的1测定醋酸的电离度和电离常数2掌握滴定原理滴定操作及正确判断滴定终点3练…
-
四川理工实验报告电导法测定乙酸电离平衡常数 (2)
实验六电导法测定乙酸电离平衡常数报告人曾辉实验时间20xx年03月07日一实验目的1掌握电导电导率摩尔电导率的概念以及它们之间的相…
-
第四版无机化学实验报告实验十三:醋酸解离度和解离常数的测定——pH计的使用
实验名称醋酸解离和解离常数的测定pH计的使用实验日期温度气压一实验目的1测定醋酸的解离度和解离常数2掌握滴定原理滴定操作及正确判断…
-
采用分光光度法测定弱电解质的电离常数实验报告
采用分光光度法测定弱电解质的电离常数实验报告一实验目的1了解一种测定弱电解质电离常数的方法2掌握分光光度计的测试原理和使用方法3进…
-
实验3 食用白醋的总酸度、电离度和电离常数的测定
实验3食用白醋的总酸度电离度和电离常数的测定教学目的与要求1学习食用白醋的总酸度电离度和电离常数的的原理和方法2学习酸度计的原理和…
-
报告示例:实验三__醋酸解离度和解离常数的测定
山东轻工业学院实验报告成绩课程名称基础化学实验1指导教师周磊实验日期院系专业班级实验地点实验楼A座412学生姓名学号同组人实验项目…
-
无机化学实验六 醋酸电离度和电离常数的测定1
实验六醋酸电离度和电离常数的测定pH法一实验目的1测定醋酸的电离度和电离常数2学习pH计的使用教学重点醋酸的电离度电离常数的测定教…
-
实验四 醋酸解离常数的测定
实验四醋酸解离常数的测定一pH法一实验目的1学习溶液的配制方法及有关仪器的使用2学习醋酸解离常数的测定方法3学习酸度计的使用方法二…