化工原理吸收实验
吸收实验
一、实验目的
1、了解填料塔的构造并学习操作方法;
2、测定填料塔体积吸收系数KYa。
二、实验原理
对填料吸收塔的要求,既希望它的传质效率高,又希望它的压降低以省能耗。但两者往往是矛盾的,故面对一台吸收塔应摸索它的适宜操作条件。
(一)、吸收系数与吸收效率
本实验用水吸收空气与氨混合气体中的氨,氨易溶于水,故此操作属气膜控制。若气相中氨的浓度较小,则氨溶于水后的气液平衡关系可认为符合亨利定律,吸收平均推动力可用对数平均浓度差法进行计算。其吸收速率方程可用下式表示:
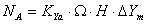 (1)
(1)
式中:NA——被吸收的氨量[kmolNH3/h];
 ——塔的截面积[m2]
——塔的截面积[m2]
H——填料层高度[m]
 Ym——气相对数平均推动力
Ym——气相对数平均推动力
KYa——气相体积吸收系数[kmolNH3/m3·h]
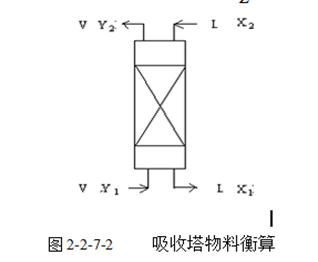
被吸收氨量的计算,对全塔进行物料衡算(见图2-2-7-2):
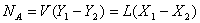 (2)
(2)
式中:V——空气的流量[kmol空气/h]
L——吸收剂(水)的流量[kmolH20/h]
Y1——塔底气相浓度[kmolNH3/kmol空气]
Y2——塔顶气相浓度[kmolNH3/kmol空气]
X1,X2——分别为塔底、塔顶液相浓度[kmolNH3/kmolH20]
由式(1)和式(2)联解得:
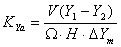 (3)
(3)
为求得KYa必须先求出Y1、Y2和 Ym之值。
Ym之值。
1、Y1值的计算:
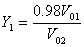 (4)
(4)
式中:V01——氨气换算为标态下的流量[m3/h]
V02——空气换算为标态下的流量[m3/h]
0.98——氨气中含纯NH3分数
对氨气:
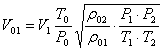 (5)
(5)
式中:V1——氯气流量计上的读数[m3/h]
T。,P。——标准状态下氨气的温度[K]和压强[mmHg]
T1,P1——氨气流量计上标明的温度[K]和压强[mmHg]
T2,P2——实验所用氨气的温度[K]和压强[mmHg]
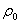 ——标准状态下氨气的密度(=0.769kg/m3)
——标准状态下氨气的密度(=0.769kg/m3)
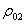 ——标准状态下空气的密度(=1.293kg/m3)
——标准状态下空气的密度(=1.293kg/m3)
对空气:
 (6)
(6)
式中:V2——空气流量计读数[m3/h]
T。,P。——标准状态下空气的温度[K]和压强[mmHg]
T3,P3——空气流量计上标明的温度[K]和压强[mmHg]
T4,P4——实验所用空气的温度[K]和压强[mmHg]
Y1也可用取样分析法确定(略)。
2、Y2值分析计算
在吸收瓶内注入浓度为NS的H2SO4VS[ml],把塔顶尾气通入吸收瓶中。设从吸收瓶出口的空气体积为V4[ml]时瓶内H2SO4Vs即被NH3中和完毕,那么进入吸收瓶的NH3体积Vo3可用下式计算:
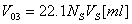 (7)
(7)
通过吸收瓶空气化为标准状态体积为:
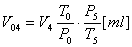 (8)
(8)
式中:V4——通过吸收瓶空气体积[ml],由湿式气量计读取
T。,P。——标准状态下空气的温度[K]和压强[mmHg]
T5,P5——通过吸收瓶后空气的温度[K]和压强[mmHg]
故塔顶气相浓度为:
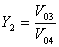 (9)
(9)
3、塔底X1~Y*1的确定
由式(2)知: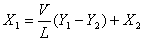 ,若X2=0,则得:
,若X2=0,则得:
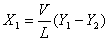 (10)
(10)
X1值亦可从塔底取氨水分析而得。设取氨水VN`[ml],用浓度为NS`的H2SO4来滴定,中和后用量为VS`[ml],则:
 (11)
(11)
又根据亨利定律知,与塔底X1成平衡的气相浓度Y1*为:
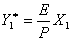 (12)
(12)
式中:P——塔底操作压强绝对大气压(atm)
E——亨利系数大气压,可查下表取得:
液相浓度5%以下的E值
表2-2-7-1

或用下式计算:
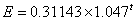 (13)
(13)
4、塔顶的X2~Y2*的确定
因用水为吸收剂,故X2=0 ,所以Y2*=0
5、 吸收平均推动力ΔYm
 (14)
(14)
6、吸收效率η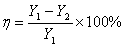 (15)
(15)
三、 设备流程简介
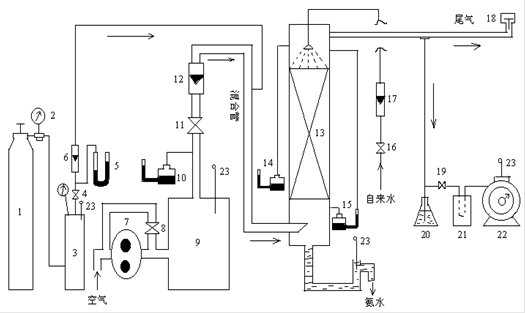
1、氨瓶 2、减压阀 3、氨缓冲罐 4、氨气调节阀 5、氨表压计
6、氨转子流量计 7、叶氏风机 8、空气旁路阀 9、空气缓冲罐 10、空气表压计
11、空气调节阀 12、空气转子流量计 13、吸收塔 14、塔顶表压计
15、塔压降压差计 16、水调节阀 17、水转子流量计 18、尾气调节阀
19、取样旋塞 20、分离水三角瓶 21、吸收瓶 22、湿式气量计 23、温度计
图2-2-7-3 吸收装置流程图
吸收装置如图2-2-7-3所示,塔径为110(mm),塔内填料有一套为塑料阶梯环,其它为瓷拉西环,均为乱堆。填料层高为600—700(mm)(请自量准确)。氨气由氨瓶1顶部针形阀放出,经减压阀2到达缓冲缺罐3,用阀4调节流量,经温度计23,表压计5和流量计6分别测量温度、压力和流量后到达混合管。空气经风机7压送至缓冲罐9,由旁路阀8和调节阀11调节风量,经温度计23,表压计10和流量计12分别测量温度、压力和流量后到达混合管与氨气混合,后被送进吸收塔13的下部,通过填料层缝隙向上流动。吸收剂(水)由阀16调节,经流量计17测定流量后从塔顶喷洒而下。在填料层内,下流的水滴与上流的混合气接触,氨被水吸收变氨水从塔底排出,氨水温度由温度计23测定,塔顶表压和填料层压降由压差计14和15测定。从塔顶排出含有微量氨的空气成为尾气从阀18排出大气中,分析尾气含氨量是用旋塞19取样,先从三角瓶20除去水分,后经吸收瓶21分析氨,气量计22计量取出空气量。
四、实验步骤
(一)测吸收系数步骤
1、全开旁路阀8,关闭空气流量调节阀11,启动风机7,慢慢打开阀11使风量由零至最大,同时观察压差计15的读数变化。
2、在吸收瓶内置入已知浓度的H2SO41ml及2滴甲基红,加适量蒸馏水摇匀后装于尾气分析管路上。关闭取样旋塞19,记下湿式气量计原始读数。
3、将水流量计17及空气流量计12(采用旁路调节法)调到指定读数。
4、关闭氨气缓冲罐上的氨气流量调节阀4,松开减压阀旋钮,打开氨瓶上的总阀,然后,慢慢拧紧减压阀旋钮把氨气引进缓冲罐3,待罐上压力表读数达0.05MP左右时,停止转动减压阀旋钮,慢慢打开调节阀4,把氨气送进混合管。
5、待塔的操作稳定后(不液泛,不干塔,各仪表读数稳定),记录各仪表读数,同时进行塔顶尾气分析。
6、尾气分析方法是打开取样旋塞19,使尾气成泡状通过吸收瓶液层,至瓶内液体的红色变淡黄色为止,即关闭旋塞,记下气量计读数。(8分)
7、保持空气和水流量不变,改变氨气流量,重复上述操作一次。
8、实验完毕,先关氨瓶上的总阀,待氨气缓冲罐上压力表读数为0后,再关闭氨气缓冲罐上的氨气流量调节阀4,然后,全开旁路阀8,同时关闭空气流量调节阀11,最后停风机和关水阀,清洗吸收瓶。
五.原始数据记录表
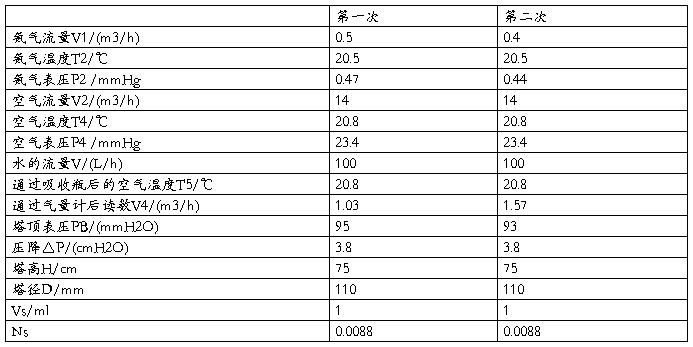
六、数据处理表及图

七、举例计算
以第一组数据作为举例计算:
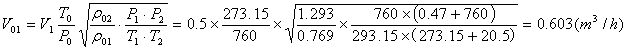
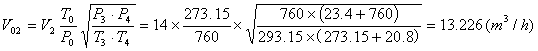

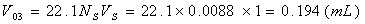
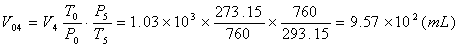
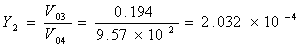
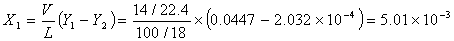
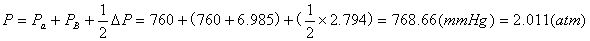

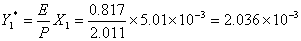
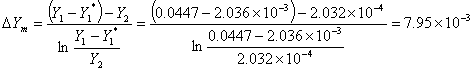



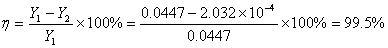
五、结果讨论
这次实验做的还是蛮成功的。对比这两组实验,可以看出:当氨气流量减小的时候,塔底气相浓度和塔顶气相浓度均减小,平均推动力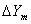 也减小,气相体积吸收系数
也减小,气相体积吸收系数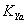 略增大。总结了实验误差的主要来源:1、在实验过程中,调节的转子流量计不停地在上下浮动,导致实验的流速不稳定,造成试验误差;2、在读数时,人为因素造成实验误差;
略增大。总结了实验误差的主要来源:1、在实验过程中,调节的转子流量计不停地在上下浮动,导致实验的流速不稳定,造成试验误差;2、在读数时,人为因素造成实验误差;
六、思考题
1、影响传质系数的因素有哪些?
答:吸收剂用量、吸收剂的平均浓度差、操作压力和温度。
2、影响吸收操作稳定性的因素有哪些?
答:空气的流速、氨气的压强和吸收剂(水)的流率。
3、填料的作用是什么?
答:填料的作用是给通过的气液两相提供足够大的接触面积,保证两相充分接触。
4、填料吸收塔塔底为什么要有密封装置?
答:液封的目的是保证塔内的操作压强。
-
化工原理实验报告_吸收
填料塔流体力学特性与吸收系数的测定一实验目的1观察填料塔内气液两相流动情况和液泛现象2测定干湿填料层压降在双对数坐标纸上标绘出空塔…
-
化工原理实验报告吸收实验
广西大学实验报告姓名专业月实验内容吸收实验指导教师一实验名称吸收实验二实验目的1学习填料塔的操作2测定填料塔体积吸收系数KYa三实…
-
化工原理实验报告(正文)---例3吸收
南京工业大学化工原理实验报告1实验一流体流动阻力测定实验实验日期一实验目的1测定流体在圆直等径管内流动时的摩擦系数与雷诺数Re的关…
-
化工原理吸收实验
吸收实验一、实验目的1、了解填料塔的构造并学习操作方法;2、测定填料塔体积吸收系数KYa。二、实验原理对填料吸收塔的要求,既希望它…
-
化工原理氧解吸实验报告
北京化工大学学生实验报告院部化学与化学工程姓名张道兴学号20xx11226专业化学工程与工艺班级化工0808同组人员余斌张文芊课程…
-
内蒙古工业大学化工原理认知实习报告
化工学院本科认识实习报告学生姓名系别专业班级实习地点化工学院实训中心指导教师高智老师二零一三年一月内蒙古工业大学化工学院认识实习报…
-
内蒙古工业大学化工原理认知实习报告[1]
化工学院本科认识实习报告学生姓名系别专业班级实习地点化工学院实训中心指导教师高智老师二零一三年一月内蒙古工业大学化工学院认识实习报…
-
化工原理实验报告(正文)---例3吸收
南京工业大学化工原理实验报告1实验一流体流动阻力测定实验实验日期一实验目的1测定流体在圆直等径管内流动时的摩擦系数与雷诺数Re的关…
-
化工原理氧解吸实验报告
北京化工大学学生实验报告院部化学与化学工程姓名张道兴学号20xx11226专业化学工程与工艺班级化工0808同组人员余斌张文芊课程…
-
化工原理实验报告
化工原理实验指导书1填料吸收塔实验11常压填料吸收塔实验111实验目的1了解加压常压填料塔吸收装置的基本结构及流程2掌握总体积传质…