AEFI监测分析报告
苍溪县20##年1—3月
疑似预防接种异常反应监测分析
为加强疫苗使用的安全性监测,进一步做好疑似预防接种异常反应(AEFI)监测和处置,现将我县本季度监测工作进行分析。
一、 AEFI监测结果
(一) AEFI报告及临测指标完成情况
20##年一季度全县通过“AEFI信息管理系统”共报告AEFI病例2例,但还有陵江、龙王、元坝、歧坪、东溪、文昌、龙山7个片区和县城接种点没有AEFI病例报告。完成情况如下:
苍溪县20##年1—3月AEFI监测完成情况
表1 AEFI报告/调查及时率
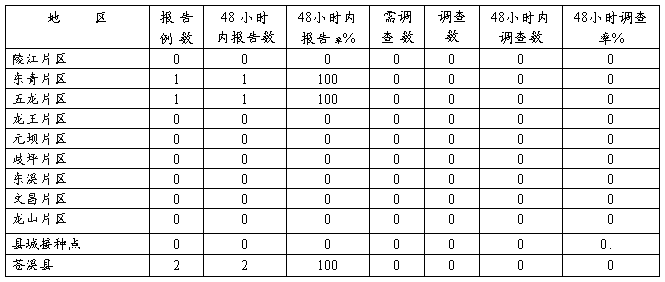
(二) 报告病例分布
截止20##年3月31日,全县20##年1—3月通过“AEFI信息管理系统”共报告AEFI病例2例,分布如下:
表2 20##年1—3月苍溪县报告AEFI地区分布

陵江片区
东青片区 1
五龙片区 1
龙王片区
元坝片区
歧坪片区
东溪片区
文昌片区
龙山片区
县城接种点
合计 2

(三) 报告病例临床诊断分布
AEFI主要临床诊断分布情况,一般反应中2例临床症状均为发热/红肿/硬结。
表3 20##年1—3月苍溪县报告AEFI病例临床诊断分布

发热/红肿/硬结 2 - - 2
合计 2 - - 2

(四) AEFI疫苗分布
2例AEFI中,百白破疫苗1 例,23价肺炎疫苗1例。
表4 20##年苍溪县AEFI疫苗分布情况

百白破疫苗 1 50
23价肺炎疫苗 1 50
合计 2 100

(五) 年龄分布
1岁1例,72岁1例。
(六) 性别分布
AEFI病例中,男性1例,女性1例。
二、 存在的问题
大部分片区对开展AEFI监测工作的重要性认识不够,监测工作未很好开展,7个片区和县城接种点没有病例报告,报告片区覆盖率20%。
三、建议
(一)充分认识做好AEF监测工作是保障预防接种安全性的一项必不可少的工作,要求各接种单位加强AEFI主动监测。
(二)要求各片区落实对临床医生和预防接种人员的培训。增进报告意识,完整、准确地填写个案调查表,及时网络录入上报。
第二篇:全国AEFI监测方案
全国疑似预防接种异常反应监测方案(试行)
(征求意见稿)
随着免疫规划工作的发展,使用疫苗的种类和数量不断增加,疫苗针对疾病的发病大幅度下降,疑似预防接种异常反应(Adverse Event Following Immunization,AEFI)受到越来越广泛的关注。为保障预防接种的安全、提高服务质量,加强AEFI监测工作,在部分省试点工作的基础上,根据《疫苗流通和预防接种管理条例》、《预防接种工作规范》的要求,并参照世界卫生组织(WHO)的AEFI监测方法,制定本方案。
一、目的
动态监测AEFI发生情况和原因,保障预防接种的安全性和服务质量,为改进疫苗质量提供依据。
(一)分析不同疫苗的AEFI发生率,评价疫苗的安全性。
(二)分析AEFI是否与疫苗品种或批次有关,评价疫苗的质量。
(三)分析AEFI是否与预防接种实施差错有关,评价预防接种服务的质量。
二、监测内容
(一)AEFI定义
AEFI是指在预防接种过程中或接种后发生的可能造成受种者机体组织器官或功能损害,且怀疑与预防接种有关的反应。
(二)AEFI报告
1、责任报告人
医疗机构、接种单位和疾病预防控制机构执行职务的人员为AEFI的责任报告人。
1
2、报告内容
在预防接种实施过程中或接种后发生下列AEFI,需进行报告:
(1)发热 (腋温≥37.6℃);(2)局部红肿(直径≥15mm)、局部硬结、无菌性脓肿;(3)过敏反应:过敏性皮疹(荨麻疹、大疱型多形红斑、麻疹猩红热样皮疹)、过敏性休克、过敏性紫癜、血小板减少性紫癜、阿瑟氏(Arthus)反应等;(4)神经系统反应: 热性惊厥、癫痫、多发性神经炎、臂丛神经炎、脑病、脑炎和脑膜炎、疫苗相关麻痹型脊髓灰质炎等;(5)卡介苗接种反应:淋巴结炎或淋巴管炎、骨髓炎、全身播散性卡介苗感染;(6)晕厥、癔症;(7)局部化脓性感染:局部脓肿、淋巴管炎和淋巴结炎、蜂窝织炎;(8)全身化脓性感染:毒血症、败血症、脓毒血症;(9)除上述情形外其它的不明原因死亡、严重残疾或组织器官损伤、群体性反应、公众高度关注事件等。
AEFI报告内容包括姓名、性别、出生日期、监护人、现住址、接种疫苗名称、接种日期、反应发生日期和人数、主要临床经过、就诊日期、就诊单位、初步临床诊断、报告单位、报告日期、报告人等。
3、报告程序与时限
AEFI报告实行属地化管理。责任报告人发现AEFI后应填写“AEFI登记表”(附件1),符合报告要求的AEFI应在48小时内向所在地的县级疾病预防控制机构报告。
怀疑与预防接种有关的死亡、群体性反应、公众高度关注事件在2小时内逐级向县、市、省级和国家疾病预防控制机构报告;各级疾病预防控制机构及时向同级卫生行政部门报告;各级卫生行政部门及时向上一级卫生行政部门报告。
(三)AEFI调查
1、核实报告
2
县级疾病预防控制机构接到AEFI报告后,根据报告内容,核实AEFI的基本信息、发生时间和人数、临床表现、初步诊断、疫苗接种等情况,完善相关资料,做好深入调查的准备工作。经核实为需要报告的AEFI,应进行个案调查。
2、调查的组织
县、设区的市和省级疾病预防控制机构应当成立预防接种异常反应调查诊断专家组,负责AEFI的调查诊断。调查诊断专家组由流行病学、临床医学、药学等专家组成。
AEFI由县级疾病预防控制机构组织专家进行调查诊断;死亡、严重残疾、群体性反应、对社会有重大影响的AEFI,由设区的市或省级疾病预防控制机构组织专家进行调查诊断。
3、现场调查和资料收集
县级疾病预防控制机构应在接到AEFI报告后48小时内组织专家开展现场调查,调查内容包括:(1)现场访视病人,了解病人基本情况,进行临床检查,收集临床资料;(2)疫苗的基本情况;(3)预防接种组织实施情况;(4)同批次疫苗接种情况及反应发生情况;(5)同品种疫苗既往应用及反应发生情况;(6)当地类似疾病发生情况。各地可以根据AEFI的具体情况增加调查内容。
AEFI个案、群体性AEFI个案需要报告的,应填写“AEFI个案调查表”(附件2)。单纯的发热 (腋温≥37.6℃)、局部红肿(直径≥15mm)、局部硬结等AEFI个案可以明确诊断的,不必赴现场调查。
县级疾病预防控制机构应将“AEFI个案调查表”、“群体性AEFI登记表”的信息在调查后3天内通过国家网络报告系统录入上报;根据调查进展,及时对录入上报资料进行订正和补充。市、省级疾病预防控制机构应及时通过国家网络报告系统,对辖区AEFI报告信息进 3
行审核。
4、标本采集和实验室检查
当怀疑AEFI与疫苗或注射器材质量有关时,接种单位需保存相应的样本,以便后期对疫苗、稀释液或注射器材进行采样,送相应检验检定机构进行检测。
当现有实验室资料不能满足AEFI分类诊断要求时,应根据调查诊断专家组的意见采集相关标本,送相关实验室进行检测。对于死亡病例,建议进行尸体解剖检查,并按照有关规定进行。
5、初步结果与建议
调查诊断专家组应对调查和收集的资料进行充分讨论和分析,判断反应是否与预防接种有关、可能的发生原因,得出初步调查结果,并提出相应建议。
6、调查报告
对于死亡、严重残疾或组织器官损伤、群体性反应、公众高度关注事件,调查诊断专家组需在调查结束后3天内撰写调查报告,并向组织调查的部门或机构报告。
调查报告包括以下内容:AEFI基本情况;AEFI临床经过、诊断、治疗情况及实验室检查结果;疫苗流通和预防接种组织实施情况;AEFI发生后所采取的措施;AEFI发生原因分析;AEFI初步分类诊断结果及判定依据;撰写调查报告的人员、时间等。
三、AEFI分类诊断
AEFI按发生原因分为:(1)一般反应:在预防接种后发生的,由疫苗本身所固有的特性引起的,对机体只会造成一过性生理功能障碍的反应,主要有发热、局部红肿、硬结,同时可能伴有全身不适、倦怠、食欲不振、乏力等综合症状。(2)异常反应:合格的疫苗在实 4
施规范接种过程中或接种后造成受种者机体组织器官、功能损害,相关各方均无过错的药品不良反应。(3)疫苗质量事故:由于疫苗在生产过程中质量不合格,接种后造成受种者机体组织器官、功能损害。
(4)实施差错事故:由于在预防接种实施过程中违反预防接种工作规范、免疫程序、疫苗使用指导原则、接种方案造成受种者机体组织器官、功能损害。(5)偶合症:受种者在接种时正处于某种疾病的潜伏期或者前驱期,接种后偶合发病。(6)心因性反应:在预防接种实施过程中或接种后因受种者心理因素发生的个体或者群体性反应。
(7)不明原因反应:经过调查、分析,发生原因仍不能明确的反应。
AEFI的最终分类诊断由预防接种异常反应调查诊断专家组在调查结束后30天内尽快作出,AEFI分类诊断流程见附件3。调查诊断专家组在作出诊断后,及时将调查诊断结论向同级卫生行政部门报告,以适宜的方式通知当事人,并做好解释工作。
四、评价与质量控制
(一)资料分析
县级以上疾病预防控制机构应按月分析AEFI监测数据,发现异常情况及时进行调查处理。资料分析内容包括AEFI发生率、分类、临床诊断;AEFI地区、时间、年龄分布;AEFI聚集性(同一时间、同一接种地点、接种同品种和/或同批号疫苗发生2例及以上相同临床损害的AEFI);AEFI报告单位比例等。
(二)信息反馈
省、市、县级疾病预防控制机构定期以公文或简报等形式,向同级卫生行政部门、上级疾病预防控制机构报告AEFI监测分析与评价结果,并向下级疾病预防控制机构、医疗机构和接种单位通报。 5
(三)监测指标
1、AEFI发现后在48小时内报告率≥80%;
2、AEFI报告后调查率≥90%;
3、AEFI报告后在48小时内调查率≥80%;
4、AEFI个案调查表填写完整率≥80%;
5、AEFI个案调查表在3天内报告率≥80%;
6、死亡、严重残疾或组织器官损伤、群体性反应、公众高度关注事件在调查结束后3天内完成调查报告达到100%;
7、AEFI分类诊断率≥90%。
五、处理原则
(一)发现AEFI,按照《预防接种工作规范》的要求积极诊治。
(二)当受种方、接种单位、疫苗生产企业对AEFI调查诊断结果有争议时,按照《预防接种异常反应鉴定办法》有关规定开展鉴定工作。
(三)因预防接种异常反应造成受种者死亡、严重残疾或者器官组织损伤的,按照《疫苗流通和预防接种管理条例》有关规定给予受种者一次性补偿。
(四)发生死亡、群体性反应、公众高度关注事件,按照应急条例有关规定开展AEFI知识宣传,做好媒体、受种者或监护人、公众等沟通工作。
(五)因疫苗质量、接种实施差错给受种者造成损害的,依照《中华人民共和国药品管理法》、《医疗事故处理条例》等有关规定处理。
六、机构与职责
(一)卫生行政部门
各级卫生行政部门负责组织开展本辖区内AEFI监测工作,并提 6
供所需监测经费,保证监测工作的顺利开展。
(二)疾病预防控制机构
协助卫生行政部门制定AEFI监测方案并具体实施,负责AEFI的报告、调查、分类诊断等工作;开展AEFI知识宣传;对疾病控制人员、医务人员和接种人员进行培训;对下级疾病预防控制机构、医疗机构和接种单位的监测工作进行督导。
(三)疫苗质量检定部门
对导致AEFI的可疑疫苗、稀释液或注射器材等进行采样和相关实验室检查,定期开展疫苗质量抽检。
(四)疫苗生产企业、疫苗经营企业
向所在地的县级疾病预防控制机构报告所发现的AEFI;向AEFI调查组提供所需要的疫苗相关信息。
(五)医疗机构、接种单位
向所在地的县级疾病预防控制机构报告所发现的AEFI;向AEFI调查组提供所需要的AEFI临床资料和疫苗接种等情况;对AEFI进行积极诊治。
7
附件1 AEFI登记表
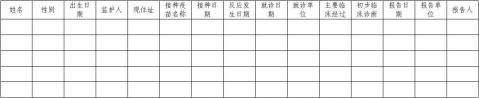
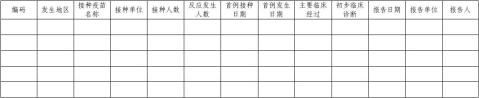
填写说明:此表用于医疗机构、接种单位、疾病预防控制机构的AEFI登记或报告记录。
8
附件2 AEFI个案调查表
一、基本情况
1. 编码 □□□□□□□□□□□□□□
2. 姓名 3. 性别 1男 2女
4. 出生日期 日
5. 监护人
6. 现住址
7. 报告日期 日
8. 报告类型 1主动监测 2被动监测
9. 调查日期 日
二、可疑疫苗情况(按最可疑的疫苗顺序填写)
疫苗1 疫苗2
1. 疫苗名称 2. 规格(剂/支或粒) 3. 生产企业 4. 批号 5. 有效日期 年 年月
6. 接种日期 年 年月
7. 接种剂次 8. 接种剂量(ml或粒) 9. 接种途径 1肌内 2皮下 3皮内 1肌内 2皮下 3皮内
4口服 5其它 4口服 5其它
10. 接种部位 1左臂 2右臂 3左臀 1左臂 2右臂 3左臀
4右臀 5其它 4右臀 5其它
1医院/卫生院 1医院/卫生院
11. 接种地点 2村卫生室 3学校 2村卫生室 3学校
4家中 5其它 4家中 5其它
三、反应发生情况
1. 反应发生日期 月
2. 发现/就诊日期 月
9 □ □□□□/□□/□□ □□□□/□□/□□ □ □□□□/□□/□□ 疫苗3 月 月 1肌内 2皮下 3皮内 4口服 5其它 1左臂 2右臂 3左臀 4右臀 5其它 1医院/卫生院 2村卫生室 3学校 4家中 5其它 □□□□/□□/□□ □□□□/□□/□□
3. 临床症状
发热(腋温℃) 局部红肿(直径mm) 局部硬结(直径mm) 其它症状
1轻(37.1-37.5) 2中(37.6-39.0) 3重(>39.0) 4无 1轻(<15) 2中 (15-30) 3重(>30) 4无 1轻(<15) 2中 (15-30) 3重(>30) 4无
□全身不适 □倦怠 □乏力 □头痛 □头晕 □寒战 □食欲不振 □恶心 □呕吐 □腹痛 □腹泻 □皮疹 □局部疼痛 □其它
□ □ □
4. 初步临床诊断 5. 是否住院
如住院,住院日期
出院日期
6. 病人转归
如死亡,死亡日期 是否进行尸体解剖 尸体解剖结论 四、结论
1. 诊断或鉴定组织 2. 诊断或鉴定级别 3. 反应分类
1是 2否
年 月 日 年 月 日 1痊愈 2好转 3 后遗症 4死亡 年 月 日 1是 2否
□□ □
□□□□/□□/□□ □□□□/□□/□□
□
□□□□/□□/□□
□
1 调查诊断专家组 2鉴定机构 1县级 2市级 3省级 1一般反应 2异常反应 3疫苗质量事故 4实施差错事故 5偶合症 6心因性反应 7不明原因反应
□ □
□
4. 最终临床诊断 5. 是否群体性AEFI
群体性AEFI编码
1是 2否
□□ □
□□□□□□□□□□□□
填写说明:AEFI个案调查表由县级疾病预防控制机构录入上报国家信息管理平台;死亡、严重残疾或组织器官损伤、群体性反应、公众高度关注事件,应附详细调查报告。
10
附件3 AEFI分类诊断流程

11
-
监测数据分析报告
888888基坑水平位移观测及相邻建筑物沉降观测第五观测周期20xx92监测报告有限公司二零一0年九月二日888888基坑水平位移…
-
某水利枢纽工程大坝安全监测资料分析报告
万家寨水利枢纽工程大坝安全监测资料分析报告建设单位黄河万家寨水利枢纽有限公司编制单位水利部天津水利水电勘测设计研究院二二年五月总目…
-
医院感染监测信息分析报告
20xx年元月份医院感染监测信息分析报告一医院感染病例的监测1元月份全院出院人数283人上报医院感染病例7例上呼吸道感染6例泌尿系…
-
AEFI监测分析报告
苍溪县20xx年13月疑似预防接种异常反应监测分析为加强疫苗使用的安全性监测进一步做好疑似预防接种异常反应AEFI监测和处置现将我…
-
20xx年死因监测报告年度分析
东阿县死因监测分析报告20xx东阿县疾病预防控制中心1东阿县20xx年度死因监测分析报告20xx年东阿县死因监测系统共收到来自各级…
-
小学教学质量监测分析报告--范例1
小学教学质量监测分析报告为了取得质量检测真实的、可信的效果,为学校进行质量分析提供客观、全面、原始的理论数据,上学期期末质量检测我…
-
小学数学期末试卷质量监测分析报告
小学数学期末试卷质量监测分析报告一、参考学生的基本情况分析全班参加考试的学生为23人。平均分90.83,及格人数为23人,及格率为…
-
监测数据分析报告
888888基坑水平位移观测及相邻建筑物沉降观测第五观测周期20xx92监测报告有限公司二零一0年九月二日888888基坑水平位移…
-
死因监测分析报告模板
20xx年死因监测分析报告开篇经济文化背景人口学特征死因监测工作的意义与重要性第一部分总死亡模式分析粗死亡率20xx年常住人口21…
-
20xx-20xx年中国松花粉市场监测及投资前景分析报告
20xx20xx年中国松花粉市场监测及投资前景分析报告艾凯咨询网艾凯咨询网什么是行业研究报告行业研究是通过深入研究某一行业发展动态…