盐酸普鲁卡因注射液中对氨基苯甲酸检查
实验项目名称:盐酸普鲁卡因注射液中对氨基苯甲酸检查
实验计划学时:6
一、实验目的
1.掌握TLC法测定有关物质的原理与测定方法。
2.熟悉粘合薄层板的制备与活化。
二、实验内容和要求
(一).薄层色谱法
(1)玻板 用5cm×20cm或l0cm×20cm的规格,要求光滑、平整,洗净后不附水珠,晾干。
(2)固定相 常用固定相有硅胶G、硅胶GF254、硅胶H、硅胶HF254等。其颗粒大小.一般要求直径为10-40 ?m,取各品种项下规定的固定项一定量,按“薄层板制备”法制备薄层板。
(3)薄层涂布 一般可分无粘合剂和含粘合剂两种;前者系固定相直接涂布于玻板上,后者系在固定相中加入一定量的粘合剂,一般常用10%-15%煅石膏(CaSO4.2H2O 在140oC加热4h), 混匀后加水适量使用,或用羧甲基纤维素钠水溶液(0.5%-0.7%)适量调成糊状,均匀涂布于玻板上。
(4)展开室 应使用适合薄层板大小的玻璃制薄层色谱展开缸, 并有严密的盖子,底部应平整光滑,便于观察。
薄层板制备 根据各品种项下规定,取1份固定相和3份水(或粘合剂)在研钵中向一方向研磨混合,去除表面的气泡后,用倾注法或平铺法或涂布器法,在玻板上涂布厚度为0.2-0.3 mm的薄层板。将涂
好薄层的玻板置水平台上,于室温下晾干后在110oC烘30min;置有干燥剂的干燥箱中备用。使用前检查其均匀度(可通过透射光和反射光检视).
点样 用微量注射器或微量吸管吸取规定量样品溶液,点样于薄层板上,—般为圆点,点样基线距底边2.0 cm,样点直径为2-4 mm,点间距离约为1.5-2.0 cm,点样时必须注意勿损伤薄层表面。
展开 展开缸如需预先用展开剂饱和,可在缸个加入足够量的展开剂,并在壁上贴两条与缸一样高、宽的滤纸条,一端浸入展开剂中,一端浸入展开剂中,密封缸顶的盖,使系统平衡.将点好样品的薄层板放人展开缸的展开剂中,浸入展开剂的深度为距薄层板底0.5-1.0 cm(切勿将样点浸入展开刑中),密封缸盖,待展开至规定距离(一般为10-15cm),取出薄层板,晾干,按各品种项下的规定检测。
三、实验主要仪器设备和材料
层析缸,玻板,喷雾器,点样用微量注射器或微量吸管。硅胶H,硅胶GF254,对二甲氨基苯甲醛,盐酸普鲁卡因注射液.
四、实验方法、步骤及结果测试
盐酸普鲁卡因注射液中对氨基苯甲酸检查
精密量取本品,加乙醇制成每1mL中含盐酸普鲁卡因2.5mg的溶液,作为供试品溶液。另取对氨基苯甲酸对照品,加乙醇制成每1mL中含30 ug的溶液,作为对照品溶液。照薄层色谱法(附录A)试验,吸取上述两种溶液各10 uL,分别点于含有羧甲基纤维素钠为粘合剂的硅胶H薄层板上,用苯-冰醋酸-丙酮-甲醇(14:1:l:4)为展
开剂,展开后,取出晾干,用对二甲氨基苯甲醛溶液(2%对二甲氨基苯甲醛乙醇溶液100 mL,加冰醋酸5 mL制成)喷雾显色。供试品溶液如显与对照品溶液相应的杂质斑点,其颜色与对照品溶液的主斑点比较,不得更深。
五、实验报告要求
记录实验详细步骤及分析结果。
六、思考题
1.TLC分析定性定量方面的应用?
七、实验说明及注意事项
1.薄层色谱分析中为使斑点集中,点样应分次点加,每次点加后,候其自然干燥、低温烘干或经温热气流吠干。
2.荡层板故入层析缸时,薄板底边应水平浸入展开剂中,待展开至溶剂前沿距玻板顶端2-3cm时,取出薄层板。
3.展开缸必须密封,为使缸内展开剂饱和,薄层板故人前可在层析缸内壁贴滤纸条,让滤纸条一端浸入展开剂中,密封层析缸,待系统平衡后再将薄层板故入,展开。
第二篇:对氨基苯甲酸乙酯(苯佐卡因)的合成
设计性实验
对氨基苯甲酸乙酯(苯佐卡因)的合成
实验大纲
(1)查阅资料,掌握以对硝基甲苯为原料合成苯佐卡因的工艺路线和反应条件。
(2)初步拟写出采用的实验方案。
(3)根据工艺路线,查出所用的试剂、合成的中间体和最终产物的理化性质。
(4)根据有关化合物的理化性质,结合掌握的化学知识,判断工艺路线和反应条件是否有可以改进或优化的可能。(在参考所查资料的基础上,运用已掌握的知识设计出合成的操作步骤以及各步反应的条件,包括物料比、反应时间和反应温度。)
(5)与老师一起讨论、修正提出的实验方案,制定出以对硝基甲苯为起始原料合成苯佐卡因的最佳工艺路线。
(6)按照修正过的方案开展合成工作。在实验过程中要特别注意一些问题,比如在氧化对硝基甲苯时硫酸的加入方式,酯化反应时所用的试剂和仪器必须干燥等。
(7)对实验进行总结和讨论,找出实验过程中发现的问题并提出改进的方法。
(8)按要求完成实验报告。
实验目的
1.设计从对硝基甲苯合成对氨基苯甲酸乙酯的不同路线,从中选择相应路线;
2.掌握有机化学实验相关资料的查找和整理及实验报告的制订;
3.通过苯佐卡因的合成,了解药物合成的基本过程;
4.掌握氧化、酯化和还原反应的原理及基本操作;
5.练习多步骤合成的实验操作技术;
6.巩固回流、过滤和结晶等基本操作技术。
实验原理
苯佐卡因有多种合成方法,若以对硝基甲苯为原料可有三种不同的合成路线:
(1)
CH3 还原CH3乙酯化CH3氧化COOH酯化
COOC2H5
.(2) NO2NH2NHCOCH3NHCOCH3NH2
CH3
COOHCOOH酯化COOC2H5
NO2NO2NH2NH2
(3)
CH3
氧化COOH酯化COOC2H5还原COOC2H5
第一条路线步骤多,产率较低;第二、第三条路线步骤少,产率较高。
参考文献
[1]马俊林,刘栓柱.苯佐卡因的合成研究[J].十堰职业技术学院学报,2001,14(2):74~77. [2]丁常泽.苯佐卡因的实验室合成方法研究[J].当代化工,2009,38(3):228,229,271.
[3]朱卫国,罗虹.有机化学实验[M].湘潭:湘潭大学出版社,2010:312~314.
[4]刘太泽.苯佐卡因的合成研究[D].南昌:南昌大学化学与环境工程学院,2010.
[5]于丽颖.苯佐卡因的合成[J].广州化工,2012,40(24):112~113.
[6]卢忠.苯佐卡因的制备方法[J].数理医药学杂志,2000,13(5):445~446. NO2NO2NO2NH2
方法(一)
主反应:
3
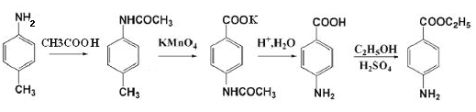
3
NO2NH2
副反应: COOK COOH
3+ H2O+H2SO43+ KHSO43 3
实验步骤:
(1)对甲基苯胺的制备
在250mL三口烧瓶上装配电动搅拌器、回流冷凝管和温度计。向三口瓶中加入10g细铁屑和90mL水。在微微加热和搅拌下,加入浓盐酸(比重1.19)0.9mL。然后将9.2g对硝基甲苯分批加入瓶中,并使反应在90℃进行回流1.5h[1]。还原反应完成后,加入0.9g碳酸钠使呈碱性。然后用水蒸汽蒸馏法[2]蒸出对甲苯胺,后者在充分冷却后结晶析出[3]。产量:约5g。纯对甲苯胺为白色片状结
晶,熔点44~45℃。
(2)对甲基乙酰苯胺的制备
在100mL圆底烧瓶中加入5g对甲苯胺和2.7mL冰醋酸,微热使其溶解。然后慢慢加入片刻后装上回流冷凝管,将反应物在水浴上加热回流0.5小时。将此温热的反应液倒入100mL冷水中,不时搅拌并微热以分解残余的醋酐。冷却,抽滤,滤饼用10mL冷水洗涤后抽干。产品如不纯,可用乙醇-水重结晶[4]。产量:约6g。纯对甲基乙酰苯胺为单斜晶体,熔点148.5℃。
(3)对乙酰氨基苯甲酸的制备
在大烧杯中将12g高锰酸钾和9g硫酸镁[5]溶解于350mL水中。在500mL圆底烧瓶中放入4.5g对甲基乙酰苯胺,并加入约三分之一[6]上述已配制的高锰酸钾水溶液,投入沸石后装上回流冷凝管,在不断振荡下用石棉网回流煮沸1~2h[7],期间分批加完其余的高锰酸钾水溶液。氧化作用完成后[8],加10~15mL10%氢氧化钠使反应液呈碱性,然后趁热抽滤[9]。将无色透明的滤液用稀硫酸酸化至弱酸性,对乙酰氨基苯甲酸呈白色粉状固体析出[10]。抽滤,滤饼用少量水[11]洗涤后压干,再用红外灯烘干。产量:约4.5g。纯对乙酰氨基苯甲酸为针状结晶,熔点256.5℃。
(4)对氨基苯甲酸乙酯的制备[12]
在干燥洁净的100mL圆底烧瓶中,溶解干燥的4.5g对乙酰氨基苯甲酸于13mL95%乙醇中,再加入2mL浓硫酸(比重1.84),投入沸石后装上回流冷凝管,将反应物用水浴加热回流1~1.5h。冷却,加水60mL,再在搅拌下分批加碳酸固体至呈中性,滤集析出的沉淀。晾干后测其熔点。必要时再用50%乙醇重结晶[13]。产量:1~2g。纯对氨基苯甲酸乙酯为白色针状晶体,熔点92℃。 注意事项:
[1]若还原时间延长(例如放置过夜),产率可明显提高。
[2]水蒸汽蒸馏时,对甲苯胺易在冷凝管中凝结而堵塞通道,遇此情况可暂停通入冷凝水。 [3]如果产品颜色较深或呈油状物,可用蒸馏法精制,收集195~200℃馏分即为产品。
[4]对甲基乙酰苯胺难溶于水(0.09g/100mL),可溶于醇(8.05g/100mL),易溶于热醇。
[5]高锰酸钾系一氧化剂,在碱性或酸性介质中的变化分别为:
2KMnO4+H22KOH+2MnO2+3[O]
2KMnO4+3H2SO4K2SO4+2MnSO4+3H2O+5[O]
由于乙酰氨基在碱性介质中会有被水解成氨基的可能,而芳香族伯胺又可进一步被氧化。故在氧化反应中加入适量的硫酸镁,可使大部份生成的氢氧化钾转变为中性的硫酸钾和氢氧化镁沉淀,上述副作用便可避免。
[6]由于反应较激烈及沉淀的生成反应时易发生暴沸现象,帮分批加入氧化剂。
[7]也可在回流约45分钟后放置过夜使反应完全。
[8]氧化作用完全时,反应液呈棕色,但若有稍过量的高锰酸钾存在,反应液也可能呈紫色。 [9]反应生成的二氧化锰易成水合物(2MnO2·H2O)析出,使抽滤较困难。加碱使对乙酰氨基苯甲酸转变成水溶性的盐类,可使抽滤较方便。
[10]滤液中的对乙酰氨基苯甲酸盐遇硫酸后转变成难溶于水的对乙酰氨基苯甲酸以沉淀析出。 [11]水洗的目的是去除夹杂在产品中的硫酸盐。
[12]在本合成方法的4步反应中,本步(水解与酯化作用)产率最低,故操作中须注意。 [13]也可用稀醇重结晶。
方法(二)
(1)对硝基苯甲酸的制备
氧化:
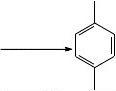
CH3+ Na2Cr2O7 + 4H2SO4
2+Cr2(SO4)3 + Na2SO4 +5H2O
步骤:本实验步骤采用机械搅拌装置[1]
向该装置的250mL三口烧瓶中加入6g研碎的对硝基甲苯、18g重铬酸钠和22mL水,开启搅拌器。在滴液漏斗[2]中放30mL浓硫酸,然后慢慢滴加入浇瓶。随着浓硫酸的加入,氧化反应随之开始,反应温度迅速上升,料液颜色逐渐变深。注意要严格控制滴加浓硫酸的速度,严防反应混合物高于沸腾温度(滴加时间约20~30分钟[3])。硫酸加完后,稍冷后再将烧瓶放在石棉网用小火加热[4],使反应混合物微微沸腾半小时[5]。停止加热。冷却后,慢慢加入76mL冷水[6],然后关闭搅拌器。将混合物抽滤,压碎粗产物,用20mL水分两次洗涤,粗制的对硝基苯甲酸呈深黄色固体。将固体放入100mL烧杯中暂存。第一次实验到此为止。
为了除去粗产物夹杂的铬盐,向烧杯中加入76mL5%氢氧化钠溶液,温热(不超过60℃)使粗产物溶解[7]。冷却后抽滤。在玻璃棒搅拌下将滤液慢慢倒入盛有60mL15%硫酸的另一大烧杯中,浅黄色沉淀立即析出。用试纸检验溶液是否呈酸性。呈酸性后抽滤,固体用少量水洗至中性,抽干后放置晾干、而后称重。必要时再用50%乙醇重结晶[8],可得到浅黄色小针状晶体。
产量:约4g。纯对硝基苯甲酸为浅黄色单斜叶片状晶体,熔点242℃。
注意事项:
[1]本氧化反应十分激烈。采用机械搅拌和滴加硫酸的方法可使反应较平稳、安全。装置安装完毕后应经教师检查无误后再加料使用。
[2]滴液漏斗在使用前要检查其考克的密封性是否完好。
[3]若滴加硫酸时烧瓶内有较多白色烟雾或火花出现,则应迅速减慢或暂停滴加,必要时用冷水浴冷却烧瓶。
[4]反应温度过高,一部分对硝基苯甲酸会挥发,冷结于冷凝管内壁上。此时可适当关小冷凝水,让其熔融滴入。
[5]观察沸腾情况时,可将搅拌器暂停片刻,当看到反应物在微微起泡则可继续搅拌反应。若因故无法搅拌,也可以采用分批加硫酸、不断振荡烧瓶的方法进行实验。
[6]也可将反应混合物在玻棒搅拌下倒入水中。但由于反应物较干粘而难以倒净,反之加入水时可以充分利用搅拌器。
[7]反应式为:Cr2(SO4)3+3+3Na2SO4而Cr(OH)3是两性物质,在温度较高
时又会溶于碱中:2Cr(OH)3+NaCrO2+2H2O,故加热溶解时温度须在60℃以下。 [8]本产品也可用升华法精制。
(2)对硝基苯甲酸先还原后酯化
还原:
HOOC
COOH
NO2HOOCCOOHNHHClSnCl4 COONH4+ CH3COONH4
NH2NH2HClNH2
步骤:在100mL圆底烧瓶中放置4g对硝基苯甲酸,9g锡粉和20mL浓盐酸,装上回流冷凝管,小火加热至还原反应发生,移去热源,不断振荡烧瓶,必要时可再微热片刻以保持正常反应。
约20~30分钟后,大部分锡粉均已参与反应,反应液呈透明状,稍冷,将反应液倾入烧杯中,加入浓氨水,直至溶液对pH纸刚好呈碱性。滤去析出的氢氧化锡沉淀[1],沉淀用少许水洗涤,合并滤液和洗液(若总体积超过55mL,在水浴上加热浓缩至45~55mL,浓缩过程中若有固体析出,应滤去)。向滤液中小心地滴加冰乙酸,至对蓝色石蕊试纸恰好呈酸性[2]乃有白色晶体析出为止。在冷水浴中冷却,滤集产品[3],在空气中晾干后称重。
产量:约2g。纯对氨基苯甲酸为无色针状晶体,在空气中或光照下变为浅黄色。m.p.为184~186℃,于186℃熔融并分解。
注意事项:
[1]还原反应后锡生成四氯化锡也溶于水,反应完毕,加入浓氨水至碱性,生成的氢氧化锡沉淀可被滤去:SnCl4+4NH3·H2Sn(OH)4↓+4NH4Cl
[2]产品对氨基苯甲酸为两性物质,故酸化或碱化时都须小心控制酸碱用量,否则严重影响产品与质量。
[3]为使产品少受损失,可采用分步抽滤的方法。即在有产品析出后,先滤集之,再将滤液加酸,如此反复抽滤,至无沉淀析出为止。
酯化:
COOH
CHCHOH
24
NH2COOC2H5COOC2H5NH22SO4NH2
步骤:在干燥的250mL圆底烧瓶中放置2g对氨基苯甲酸,20mL无水乙醇,2.5mL浓硫酸[1],混匀后投入沸石,水浴加热回流1~1.5h。将反应液趁热倒入装有85mL冷水的250mL烧杯中,得一透明溶液。在不断搅拌下加入碳酸钠固体粉末至液面有少许白色沉淀出现时[2],慢慢加入10%碳酸钠
溶液,使溶液对pH试纸呈中性,滤集沉淀,少量水洗涤,抽干,空气中晾干。必要时可用50%乙醇重结晶。产量:1~2g。
注意事项:
[1]加浓硫酸时要慢,且不断振荡烧瓶使之在反应液中分散均匀,以防加热后引起碳化。 [2]加碳酸钠粉末时要少量多次,每次加入后必须等反应完全后再可补加,切忌过量。
方法(三)
(1)对硝基苯甲酸的制备:同方法(二)
(2)对硝基苯甲酸先酯化后还原
酯化:
2H5
步骤:在250mL圆底烧瓶中依次加入4g对硝基苯甲酸,20mL95%乙醇和1.5mL浓硫酸,加热回流
1.5h。用小火蒸出一部分乙醇(约9mL),趁热将残液倒入50mL冷水中并随加搅拌[1],滤集析出的白色沉淀,用少量水洗,再将沉淀转移至研钵内[2],加5%碳酸钠5mL,研磨以除去未酯化的对硝基苯甲酸,抽滤,用少量水洗涤滤饼,抽干,得白色颗粒晶体。必要时可用乙醇重结晶。
产量:2~3g。纯对硝基苯甲酸乙酯为无色结晶,熔点57℃。
注意事项:
[1]必须随时搅拌,这样析出的固体粒子比较细,便于以后处理。
[2]如粒子很细,可不在研钵内研磨,只要在烧杯中用5%碳酸钠溶液洗涤就可以了。
还原:
2H5
NO2NO2 2H5
步骤:在100mL三颈烧瓶中,放5.6g铁屑,18mL水,1mL冰醋酸,搅拌回流煮沸10分钟使铁屑活化,放冷,加入2g对硝基苯甲酸乙酯和18mL95%乙醇[1],搅拌下慢慢回流1.5~2小时[2],将13mL温热的10%碳酸钠溶液慢慢加入热的反应物中,并随加随搅拌,迅速抽滤,滤液加水至结晶产品完全析出,冷却,滤集产品[3],必要时可用50%乙醇重结晶。
注意事项:
[1]用95%乙醇作溶剂,既可溶解对硝基本甲酸乙酯,使还原反应容易进行,又可使反应物控制在80度以下搅拌回流,以免产物在沸水中分解。
[2]在加热回流过程中,先有红棕色氢氧化铁生成,最后反应物呈深棕色偏黑,这是因为有Fe3O4 NO2 NH2
存在所致。
[3]滤集Fe3O4残渣中可能夹杂着少量产品,大量制备时可用热水或稀醇洗一次,以减少损失。 思考题
1.试提出其它合成苯佐卡因的路线并比较它们的优缺点。
2.酯化反应为何先用Na2CO3粉末中和,再用10% Na2CO3溶液中和反应液?
3.如何以对氨基苯甲酸为原料合成普鲁卡因(Procaine)。
普鲁卡因(4-氨基苯甲酸-2-(二乙氨基)乙酯)有两种合成方法。第一种是从对氨基苯甲酸乙酯出发与N,N'-二甲基-2-氨基乙醇在乙醇钠的催化下发生酯交换反应。第二种方法是通过先用氯化亚砜将对硝基苯甲酸转化成对硝基苯甲酰氯,接着将酰氯与N,N'-二甲基-2-氨基乙醇得到对硝基苯甲酸酯,最后用Rany镍将硝基还原成氨基得到产物。
4.氧化反应完毕,将对硝基苯甲酸从混合物中分离出来的原理是什么?
5.酯化反应为什么需要无水操作?
6.铁酸还原反应的机理是什么?
7.试比较“先还原后酯化”与“先酯化后还原“的特点。
实验报告
包括实验目的,实验方案步骤,实验结果并讨论分析在实验中出现的问题,实验中的特殊现象、实验操作的成败、实验的关键点等内容进行整理、解释、分析总结,回答思考题,提出实验结论或提出自己的看法等。
-
对氨基苯甲酸乙酯的制备大实验报告
前言对氨基苯甲酸乙酯别名苯佐卡因白色晶体状粉末无嗅无味分子量16519熔点9192易溶于醇醚氯仿能溶于杏仁油橄榄油稀酸难溶于水其作…
-
对氨基苯甲酸乙酯的实验报告
对氨基苯甲酸乙酯编辑词条编辑摘要摘要别名苯佐卡因无色斜方形结晶无嗅无味分子量16519熔点8890易溶于醇醚氯仿能溶于杏仁油橄榄油…
-
对氨基苯甲酸乙酯合成及表征实验报告
对氨基苯甲酸乙酯苯佐卡因的制备一实验目的1了解多步反应合成思路2进一步了解氨基的保护苯甲基的氧化和酯化反应二实验原理对氨基苯甲酸乙…
-
苯佐卡因实验报告三:对氨基苯甲酸乙酯的制备(还原)
苯佐卡因实验报告三对氨基苯甲酸乙酯的制备还原对氨基苯甲酸乙酯的制备还原实验目的1通过苯佐卡因的合成了解药物合成的基本过程2掌握氧化…
-
对硝基苯甲酸的还原实验操作报告
实验操作报告对硝基苯甲酸制对氨基苯甲酸一实验目的1通过对硝基苯甲酸的还原了解有机合成的基本过程2掌握还原反应的原理及基本操作3由对…
-
收银员课长(领班)个人年度工作总结
收银员课长(领班)个人年度工作总结天顺师宗明辉店阳光收藏室该年度中,在企业领导及同事们的指导和帮助下,我严格要求自己,认真履行一名…
-
施工员项目管理工作总结感受及心得
施工员项目管理工作总结感受及心得在兰大项目部一年多的时间里,我跟随项目部参与了此工程从前期的施工准备到目前正在进行的后期装饰等一系…
-
设备安全专项大检查工作总结汇报
根据中国中铁股份有限公司和中国中铁大桥局集团第六工程有限公司通知安排和要求,在所有工点开展一次设备安全专项大检查活动。我梁场接通知…
-
党课结业考试总结
一计划党课培训结业总结活动目的党课培训的目的是,使同学们学习到一些党的纪律,党纪是组织和全体党员必须遵守的行为规则,是维护全党的团…
-
测量员年终工作总结
工作总结时光飞逝,转眼间20xx年又到尾声了。测量是工程的眼睛,作为测量人员,我本着实事求是、一切以数据说话的原则从事测量工作。我…