辅酶催化法合成安息香--溶液pH值对合成安息香产率的影响
辅酶催化法合成安息香
--溶液pH值对合成安息香产率的影响
实验人员学号:
姓名 :笑天
专业班级:高分子 10-1班
指导老师姓名:黑晓明
目录
摘要………………………………………………………………3
关键词……………………………………………………………3
第一章 前言……………………………………………………3
1.1安息香的结构与性质…………………………………………………3
1.2安息香的用途…………………………………………………3
1.3安息香的合成方法…………………………………………………3
第二章 实验部分……………………………………………4
2.1实验仪器与药品………………………………4
2.2实验装置…………………………………………………4
2.3实验步骤………………………………………………5
2.4实验注意事项………………………………………………6
第三章 数据处理……………………………………………………7
3.1理论产率………………………………………………………7
3.2 pH对产率的影响……………………………………………7
3.3安息香的熔点测定……………………………………………8
3.4晶体的I-R图……………………………………………9
第四章 结果与讨论…………………………………………………9
4.1 pH对产率的影响…………………………………………………9
4.2熔点分析…………………………………………………10
4.3晶体的I-R图分析…………………………………………………11
参考文献…………………………………………………12
摘要
以苯甲醛为原料,辅酶 VB1 为催化剂,利用缩和反应制备安息香,实验采用单因素法,寻找不同催化剂用量对安息香合成的产率的影响,得出了最佳反应条件: 碱性环境 pH =9~10 ,苯甲醛用量为15ml, VB1的用量为1.8g,反应时间为75min,反应温度为60~75℃。在此反应条件下,反应产率可达到 22%~24%,测得熔点在133~136℃之间,符合安息香的熔点范围,而且的得到I-R图和安息香的标准I-R图基本上相近。
关键词:苯甲醛,安息香缩合反应,安息香,催化剂VB1,碱性条件。
第一章 前言
1.1安息香的结构与性质
结构:C6H5-CO-CHOH-C6H5
性质:安息香(英文:Benzoin) 又称苯偶姻、二苯乙醇酮、2-羟基-2-苯基苯乙酮或2-羟基-1,2-二苯基乙酮,是一种无色或白色晶体。
1.2安息香的用途
安息香可用于配制止咳药和感冒药还可制成局部用药。等级较好的安息香提取后用于生产香皂、香波、护肤霜、浴油、气溶胶、爽身粉、液体皂、空气清新剂、织物柔顺剂、洗衣粉和洗涤剂等日用化学品。安息香配剂用作吸人剂, 可减轻粘膜炎、支气管炎等上呼吸道病症。安息香还是一种主要的食用香精。
安息香是一种重要的化工原料,广泛用作感光性树脂的光敏剂、染料中间体和粉末涂料的防缩孔剂,也是一种重要的药物合成中间体,如抗癫痫药物二苯基乙内酰脲的合成以及二苯基乙二酮、二苯基乙二酮肟、乙酸安息香类化合物的。
1.3安息香的合成方法
安息香缩合是人们用氰化钠催化生成安息香,芳香醛在氰化钠(钾)催化下,分子间发生缩合生成二苯羟乙酮或称安息香的反应,称为安息香缩合。这是一个碳负离子对羰基的亲核加成反应。其它取代芳醛如甲基苯甲醛、对甲氧基苯甲醛和呋喃甲醛等也可发生类似的缩合,生成相应的对称性二芳基羟乙酮。这种方法的优点是效果好,不过氰化钠有毒和反应产率低。 20世纪70年代后,开始采用具有生物活性的辅酶维生素B1 代替氰化物作催化剂进行缩合反应。以维生素B1作催化剂具有操作简单,节省原料,耗时短,污染轻等特点。但是反应需要在冰水浴中操作,而且反应收率往往比较低。
本实验以苯甲醛为原料,VB1为催化剂,利用缩合反应合成安息香。采用单因素实验法,寻找体系在不同pH时对产率的影响。
第二章 实验部分
2.1 实验仪器与药品
1)仪器:100ml圆底烧瓶(2个),天平(称量纸),量筒,玻璃棒,烧杯(300ml两个、50ml一个),电热套,温度计,冷凝管(乳胶管),抽滤瓶,布氏漏斗,滴管,热过滤漏斗,pH试纸,滤纸,毛细管若干,长玻璃管一个,橡皮圈一个,酒精灯,提勒熔点测定管,铁夹、架圈一套,。
2)装置:加热回流装置,抽滤装置,热过滤装置,熔点测定装置,红外测定装置
3)药品:VB1,固体氢氧化钠,95%乙醇,苯甲醛,沸石,活性炭,冰块。
2.2实验装置


1,加热回流装置 2. 热过滤装置


3.抽滤装置 4.熔点测定
2.2实验装置
1.NaOH溶液的配制
用天平称取氢氧化钠固体7.5g,然后向烧杯中加入50ml水溶解,搅拌,摇匀待用。
2.配制反应液:在室温下,在100ml圆底烧瓶中,加入1.8gVB1,6ml水,15ml工业乙醇和15ml苯甲醛。
3.调节pH:用上面配置的氢氧化钠溶液,慢慢滴加到混合溶液,并充分摇匀混合液,将pH调到8,并三分钟内不变褪色为止。
4.加热回流
按照由下往上,自左向右的顺序将回流装置安装好,打开水龙头,让冷凝水由球形冷凝管的下部流入,上部流出。启动电热套,用水浴加热,并且保持温度在60~75℃之间,加热75min。反应混合物呈桔黄(红)色均相溶液。
5.冰浴
回流完毕,取出蒸馏瓶,将蒸馏烧瓶置于空气中冷却片刻,再将蒸馏瓶放在装有冰块的烧杯中冷却,直到有晶体全部析出。
6.抽滤
将布氏漏斗洗净,并放入两张小的圆形滤纸,启动水泵,向滤纸上滴加几滴水,然后将冰浴得到的物质倒入漏斗中进行抽滤,并用冷水分两次洗涤结晶,等到没有滤液滴出时停止抽滤。注意,一定要先拿来开布氏漏斗才能关闭水泵。
7.粗称
用托盘天平称量抽虑所得的粗产品,并记录数据。
8.重结晶
将抽虑所得的粗产品放入圆底烧瓶中,加入适量95%乙醇(1克粗产品对应6ml乙醇),将液体加热沸腾至溶解,如产物为黄色,可稍微冷却加入活性炭脱色,加热约5分钟,同时加热准备好的热过滤漏斗趁热过滤。过滤过程中继续加热圆底烧瓶以免晶体析出造成浪费。 热过滤装置如图所示:
9.结晶抽滤
将过滤得到的滤液冷却结晶,按步骤6抽滤,得到纯产品。
10.称量
称量所得产品的质量,并记录。
11.测熔点
将准备好的毛细管一端放在酒精灯。火焰边缘,慢慢旋转加热,毛细管因玻璃熔融而封口。注意,转速要均匀,使封口严密且厚薄均匀,要避免毛细管烧弯或溶化为小球。
填装样品时,一定要把样品填装均匀,密实,使样品的填装高度为2~3mm。
安装装置时,倒入的导热油液面位于提勒管叉口处,温度计的水银球位于提勒管上下叉管中间,而试样位于水银球的中部,且橡皮圈要在导热液以上。
安装完成后,开始加热,记下药品开始坍塌时和完全熔化时的温度即可。再重复两次, 且相隔温度不应超过1℃。
12. 重复上述实验,不过要将步骤三中的pH调至9、10、11。再做三次实验。
13.测量该晶体的I-R图。
2.4 实验注意事项
(1)VB1酸性条件下稳定,易吸水,在水溶液中已被氧化失效,且在滴加氢氧化钠时,要冷却的氢氧化钠,以防止VB1开环失效
(2)调节pH时,溶液一定要摇匀,并且三分钟内不退色 。
(3)在加热回流过程中,温度不能超过75℃,温度过高会使维生素分解,影响产率,所以在回流过程中应严格控制温度。
(4)加入活性炭之前,一定要冷却,以防引起暴沸。
(5)热过滤一定要迅速,防止冷却,热过滤时一定要将酒精灯移走防止失火。
(6)在不到保温时间就有产物析出,属正常现象。
(7)测准熔点必须注意的问题:
1、仪器因素:温度计要校正;熔点管要干净,管壁要薄。
2、操作因素:样品必须干燥并研磨细、装填紧密;严格控制升温速度观察准确。
第三章 数据处理
3.1 理论产量
计算安息香的理论产量:
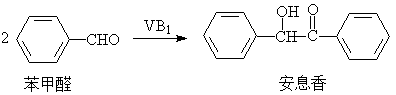
由反应式可得:
安息香理论产量15ml×1.0415g/ml÷106.12 ÷2×212.25 = 15.62g
3.2pH对产率的影响

3.3 安息香的熔点测定

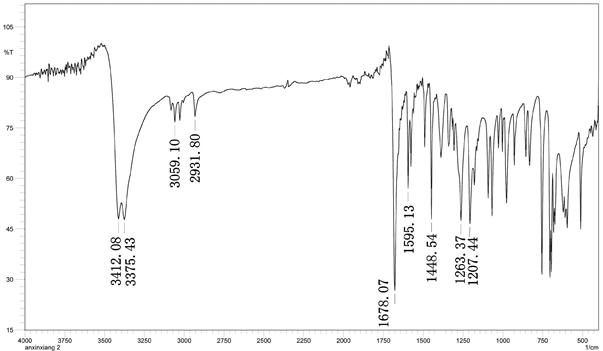
3.4测量得到的该晶体的I-R图
第四章 结果与讨论
4.1pH对产率影响
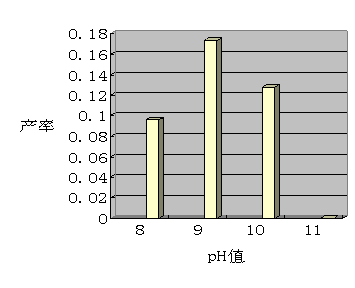
1.整体概述:
通过所得的柱形图显示,pH在8~9 间时安息香的产率呈现上升趋势,在9~10间安息香的产率呈现下降趋势。当溶液的pH在9 时,产量最大。当调节溶液的pH达到10时,产量减少并且当调节溶液的pH到11时,没有得到安息香,产率为零。
可以得出结论:溶液的pH值对安息香产率有影响
2.催化机理:
绝大多数生化过程都是在特殊条件下进行的化学反应,酶的参与可以使反应更巧妙、更有效及在更温和的条件下进行。维生素B1在生化过程中可对形成偶姻(如α-羟基酮)反应发挥辅酶作用。VB1分子最主要的部分是噻唑环,其C2上的质子由于受氮和硫原子的影响,有明显的酸性,在碱作用下,质子容易解离下去,产生碳负离子反应中心,形成苯偶姻。碱性在 9~10 间,VB1在1.8g时催化效率最高(碱性在9~10 时,辅酶活性最好)。
3.实验偏差分析
在实验操作过程中,由于对操作过程不熟悉,造成了浪费,而且抽滤也有些不完全,也出现了热过滤时析出大量结晶的现象,导致以后的产量忽高忽低,并不能得到安息香的产率随pH的变化而呈现的较为准确的变化趋势。
总之本次实验以15ml苯甲醛为基准,在9~10 的碱性环境下,当VB1的用量为1.8g,反应时间为75min,反应温度为60~75℃时反应产率达到最高。
4.2 熔点分析:
安息香的标准熔点是137℃,本实验所测得的物质的熔点在133—135℃之间,两者之间相差比较小,可以初步判断此合成物质为安息香。详细来看,合成的安息香的熔程在133-135之间,符合安息香在浓度范围内对标准熔点的偏差,因此,我们可以得出结论,合成的物质即为安息香。
有很多原因会导致合成的安息香的熔点偏小,如晶体干燥补充不充分,装的固体多了,重结晶损耗太多,操作规范性与读数误差等都会造成熔点的偏差。
4.3晶体的I-R图分析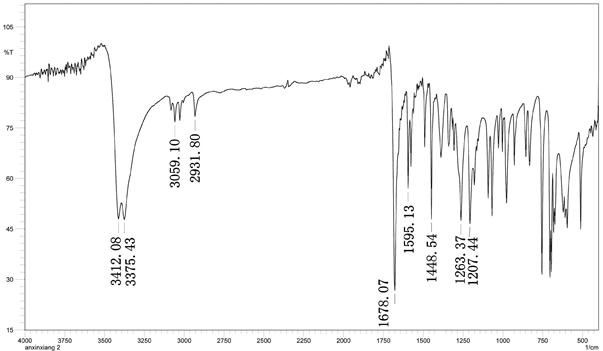
1.安息香的特征结构:-OH,-CH,C=O,苯环,C-O
2.图形分析
由安息香的标准IR谱图1和样品IR谱图6知,通过对比,可以看出这两幅图的非常相似,但也有不同之处,从样品IR谱图知,在3412.08和3375.43处有强吸收峰可知样品中有-OH,在3059.10和2931.80处有吸收峰知样品中有-CH,在样品IR谱图1678.07处有吸收知样品中有C=O键,在1595.13和1448.54处有吸收说明有苯环,在1263.37和1207.44处有吸收说明有C-O键。
通过以上分析,所测物质的特征结构与标准的安息香的特征结构的数据范围相当接近,可以认为晶体为安息香。但在实验过程中可能会有杂质,有点误差是难免的,所以得到最终结论:该晶体就是安息香。
实验过程及结果总结
以苯甲醛为原料,VB1为催化剂,利用缩合反应合成安息香。采用单因素实验法,寻找体系在不同pH时对产率的影响。得出了最佳反应条件: 碱性环境 pH =9~10 ,苯甲醛用量为15ml, VB1的用量为1.8g,反应时间为75min,反应温度为60~75℃。在此反应条件下,反应产率可达到 22%~24%,测得熔点在133~136℃之间,符合安息香的熔点范围,而且的得到I-R图和安息香的标准I-R图基本上相近,很容易推出此晶体就是安息香的结论。
用辅酶(维生素B1)作催化剂,价廉易得,操作安全,效果良好,但实验中产率较低或有时得不到产品,影响后续实验的进行,因此在实验中可以采用四丁基溴化铵作为相转移催化剂,通过控制反应体系的pH和反应温度,安息香产率可以进一步提高,实验成功率也大大提高。
参考文献
[1] 杜登学、马万勇等.基础化学实验简明教程.化学工业出版社,2007.8
[2] 张国升、程俊等.安息香缩合反应的改进[J].安徽中医学院学报.2003.22(6)46-47
[3] 何强芳,伍光仲,朱洁民. 安息香缩合反应的影响因素[J]. 大学化学. 20##年03期
[4] 李中华,白亦穷. 辅酶催化安息香缩合反应的实验探讨[J]. 大学化学. 20##年02期
[5] 张康华,曹小华,陶春元,全民强. 安息香缩合与应用研究进展[J]. 安徽农业科学. 20##年30期
第二篇:安息香
辅酶催化法合成安息香
——辅酶用量对合成安息香产率的影响
姓名:
专业班级:
指导教师:
目 录
摘要 ...................................................................................................................................................... 1
关键词 .................................................................................................................................................. 1
第一章 前言 ...................................................................................................................................... 2
第二章 实验部分 .............................................................................................................................. 3
2.1 实验设备、装置、仪器和试剂、材料 ................................................................................ 3
2.2实验方法和过程..................................................................................................................... 4
2.2.1安息香的制备 .............................................................................................................. 4
2.2.2 安息香的提纯(重结晶方法) ................................................................................. 5
2.2.3 安息香熔点测定 ......................................................................................................... 5
2.2.4 其它组操作 ................................................................................................................. 6
2.3 实验注意事项........................................................................................................................ 7
第三章 数据处理 .............................................................................................................................. 8
3.1 相关信息查找........................................................................................................................ 8
3.2 实验数据记录及处理 ............................................................................................................ 8
3.2.1 产率计算..................................................................................................................... 8
3.2.2 绘制产率—VB1用量曲线 ........................................................................................ 9
第四章 结果与讨论 ........................................................................................................................ 10
4.1 维生素B1用量对产率的影响分析 ................................................................................... 10
4.2 安息香纯度分析.................................................................................................................. 10
4.3 安息香结构分析.................................................................................................................. 10
4.4 心得体会 ............................................................................................................................. 12
参考文献 ............................................................................................................................................ 13
基础化学综合试验
摘要
以苯甲醛为原料,在辅酶维生素B1的催化作用下,分子间发生缩合生成了安息香。本实验采用单因素法,得出了辅酶用量对反应产率的影响。以15ml苯甲醛、6ml水、15ml无水乙醇和适量150g/LnaOH使PH达9-10为基准,得维生素B1的最佳用量为1.30g。反应产率达6.47%。适量维生素B1提高了反应产率。
关键词:苯甲醛维生素B1 安息香产率
1
基础化学综合试验
第一章 前言
安息香缩合反应一般采用氰化钾(钠)作催化剂,是在碳负离子作用下,两分子苯甲醛缩合生成二苯羟乙酮。但氰化物是剧毒品,易对人体危害,操作困难,且“三废”处理困难。20世纪70年代后,开始采用具有生物活性的辅酶维生素B1代替氰化物作催化剂进行缩合反应。 以维生素B1作催化剂具有操作简单,节省原料,耗时短,污染轻等特点。
本实验目的是在维生素B1的催化下合成安息香,并且通过单因素法研究维生素B1用量对反应产率的影响,最后测定产品熔点确定其纯度,测IR谱图确定其结构。
安息香用途广泛,即可用作医药中间体,也可用于染料生产及感光性树脂的光增感剂、照相凹版油墨、光固化型涂料 。作为药物时,其可治疗中风痰劂;惊痫昏迷,产后血晕;心腹疼痛;风痹肢节痛。开窍醒神;豁痰辟秽;行气活血;止痛。
安息香有很好的发展前景,就近些年其市场需求量逐年增多,再加上其用途被广泛开发,其价值在不断提升。此项研究可用于工业大规模生产,提高安息香产品的产率。
2
基础化学综合试验
第二章 实验部分
2.1 实验设备、装置、仪器和试剂、材料
1.仪器:烧杯(1000ml、l各一个),量筒(10 ml、100ml各一个),锥形瓶一个,广口瓶一个,小滴管一个,玻璃棒一个,PH试纸一包,托盘天平一个,电子天平一个,大小滤纸若干
2.设备和装置:
(1).加热回流装置:KDM型电热套
一个, 100ml圆底烧瓶一个,400ml
烧杯一个, 19×2球形冷凝管一个,
100℃温度计一支, 铁架台一个

(2).抽滤装置:SHB-ⅢA循环、水
式多用真空泵,布氏漏斗一个,抽滤瓶
一个
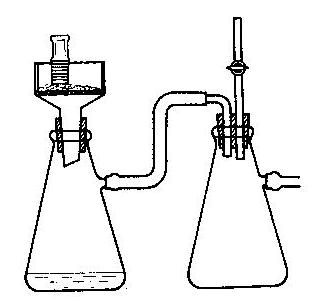
(3).热过滤装置:铁架台一个(带
铁圈),保温漏斗一个,普通漏斗一个,
酒精灯一个
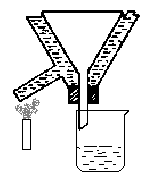
3 图 2-1 加热回流装置 图 2-2 抽滤装置 图 2-3 热过滤装置
基础化学综合试验
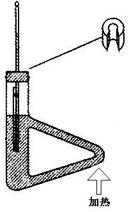
(4).熔点测定装置:提勒熔点测定管一个,酒精灯一个,表面皿一个,毛细管若干, 150℃温度计一支,30~50cm玻璃管一根,橡皮圈
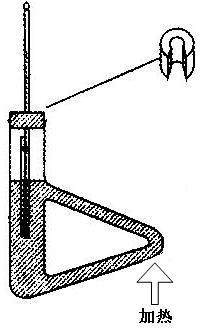
图 2-4 提勒熔点测定管
3.试剂、材料:
维生素B1,水,无水乙醇,苯甲醛,冰,NaOH固体,甘油。 2.2实验方法和过程 2.2.1安息香的制备
将实验所用到的所有仪器洗刷干净摆放整齐待用。然后,按照从下到上,从左到右的顺序安装好热回流装置。
表2-1 试剂及其用量
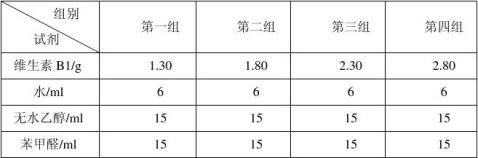
注:称取维生素B1用电子天平,水用10ml量筒,无水乙醇用100ml量筒,苯甲醛用250ml恒压滴液漏斗。
1.配制反应液:检查无误后,按表2-1第一组数据量取试剂、材料,加入到100ml圆底烧瓶中,混合均匀。然后用托盘天平称取3gNaOH固体(NaOH易潮解,为防止其腐蚀天平托盘,用小烧杯盛装),稀释到20ml,搅拌均匀,即得150g/LNaOH溶液。然后用胶头滴管慢慢向混合液中滴加刚刚配制好的NaOH溶液,不断摇晃圆底烧瓶使溶液均匀混合,并随时用玻璃棒蘸取少量混合液于PH试纸上检验其是
4
基础化学综合试验
否达到9-10范围内,最后滴加到15滴时PH值达到要求,并且溶液的橙黄色在3分钟内不褪去,停止滴加NaOH溶液。
2.加热回流:在此之前已经提前在400ml烧杯中加入适量的水,放于电热套上加热待用,使其水浴温度保持在60-75℃(且不可加热至沸腾)。然后将反应液放入水浴中加热回流了80min,期间时刻注意温度值,没有超出允许范围,而且由于固体太多,摇晃反应液两次,以加速固体溶解。最后反应混合物呈桔黄色。
3.结晶:将反应后液体转入50ml小烧杯中,冷却至室温,析出浅黄色固体。然后将小烧杯放入盛有适量冰块的1000ml大烧杯中冰浴,使其结晶完全。
4.抽滤:把滤纸放入布氏漏斗内,用少量水润湿。然后,把漏斗安于抽滤瓶上(注意漏斗端的斜口应对着抽滤瓶的吸气嘴),打开开关,滤纸紧贴在布氏漏斗的瓷板上,说明其气密性良好。然后将烧杯中液体倒入漏斗内,注意使固体铺展开,用50ml 冷水分两次洗涤结晶。抽滤完成后为防止倒吸,先拿下布氏漏斗,然后关闭开关。取下晶体,即得安息香粗产品,称其质量为3.08g。
2.2.2 安息香的提纯(重结晶方法)
将粗产品置于100锥形瓶中,加入0.09g活性炭(计算量)脱色,22ml无水乙醇(计算量),放于电热套内加热至沸腾。与此同时,保温漏斗内注满水,普通漏斗放入其中,酒精灯加热至较高温度。然后,将叠好的滤纸放入普通漏斗内,用水润湿,使滤纸紧贴漏斗内壁,滤纸也有一定温度后,趁热过滤,由于产品在滤纸上残留太多,又用无水乙醇溶解,趁热过滤一次。然后,将滤液冰浴一段时间使其重结晶,结晶完全后按上述方法抽滤,将产品置于桌面上,盖上小滤纸使其自然干燥,即得安息香精产品,称其质量为1.01g。
2.2.3 安息香熔点测定
1.毛细管封口:将准备好的三根毛细管一端放在酒精灯火焰边缘,慢慢转动加热,毛细管因玻璃熔融而封口。操作时转速要均匀,避免毛细管烧弯或熔化成小球。
2.样品填装:将少量产品置于研钵中研细,放在干净的表面皿上,聚成小堆,将毛细管开口的一端插入其中,使产品挤入毛细管中。然后,毛细管开口一端朝上,投入竖直放在表面皿上的玻璃管内,反复几次,使产品填装均匀、密实,高
5
基础化学综合试验
度约为2~3mm。
3.仪器安装:按照熔点测定装置图
安装好实验装置,注意导热油液面位于
提勒管的叉管处,毛细管中试样位于温
度计水银球中部,如图2-1所示。温度
计水银球位于提勒管上下叉管中间,因
此处对流循环好,温度均匀。
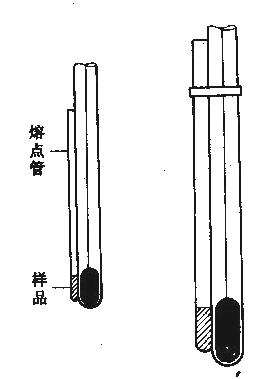
图 2-5 毛细管与温度计相对
4.熔点测定:酒精灯在提勒管支管下端加热,时刻注意温度计所示温度,并仔细观察毛细管中样品熔化情况。当出现塌落时,产品开始熔化,记下此时始熔温度为130℃,当其呈透明溶液时,熔化完全,记下此时全熔温度为135℃。固体熔化过程如图2-2所示。
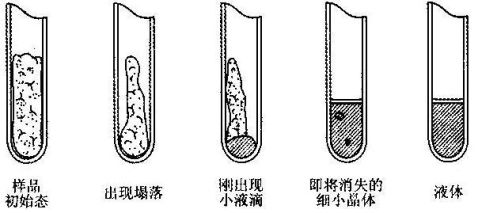
图 2-6 固体熔化过程
按照上述方法测量其它两根毛细管中样品的熔点,记录数据,以两个误差较小的数据作为实验数据。
2.2.4 其它组操作
与第二组实验大致相同,分别进行加热回流,抽滤,重结晶,熔点测定过程。不同点列于如下:
第一组:按照表2-1第一组数据添加,150g/LNaOH溶液15滴,加热回流了80 min。
6
基础化学综合试验
第二组:按照表2-1第二组数据添加,150g/LNaOH溶液15滴,加热回流了83 min。
第三组:按照表2-1第三组数据添加,150g/LNaOH溶液19滴,加热回流了80min。
第四组:按照表2-1第四组数据添加,150g/LNaOH溶液20滴,加热回流了77min。
2.2.5 安息香结构测定
由老师取样,测定安息香IR谱图,用于分析其结构。谱图见图4-1。
2.3 实验注意事项
1.维生素B1在酸性条件下是稳定的,但易吸水,在水溶液中易被氧化失效,光及Cu、Fe、Mn等金属离子均可加速氧化;在NaOH溶液中噻环 易开环失效。
2.安息香在沸腾的无水乙醇中的溶解度为100ml12-14g。
3.在使用活性炭时,切记不可将其直接加入沸腾的溶液中,待溶液冷却后再加入,其用量为有机物的1%—5%。
4. 热过滤前一定要先将酒精灯熄灭,并且远离明火进行操作,以免引起火灾;及时开窗通风,降低室内乙醇浓度,以免达爆炸极限,引起事故。
7
基础化学综合试验
第三章 数据处理
3.1 相关信息查找
查阅相关资料,得出以下两种有机物的部分物理性质,用于数据处理。
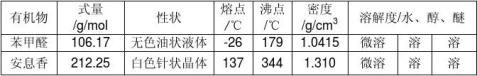
3.2 实验数据记录及处理
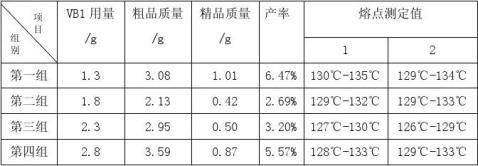
3.2.1 产率计算
2苯甲醛
安息香
由反应方程式以及表3-1所给数据计算出安息香的理论产值15.616g,再由表3-2所记录精产品质量得出各组安息香产率,填入表3-2。
8
基础化学综合试验
3.2.2 绘制产率—VB1用量曲线
以VB1用量为横坐标,产率为纵坐标,作出以下二维柱状图。
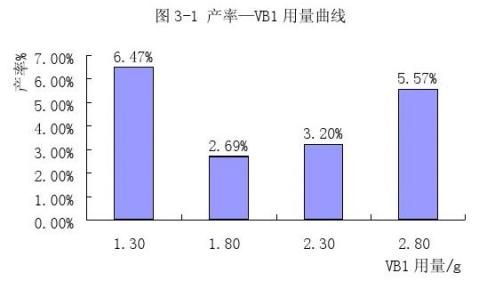
9
基础化学综合试验
第四章 结果与讨论
对第三章数据处理部分的相关图、表进行综合比较,从一下三个方面对安息香产品进行分析。
4.1 维生素B1用量对产率的影响分析
由图3-1 分析知,四组实验安息香产率都不高。维生素B1用量为1.3g时,产率最大,依次为2.8g,2.3g,1.8g。此结果与实际情况1.8g产率最高不符,有很多原因影响:
1. 用150g/LNaOH溶液调节反应液PH时,碱性不够,不宜析出晶体。我们在进行第二组实验时,由于只加了5滴NaOH溶液,最后导致晶体没有析出,向小烧杯中加入少量晶种,并用玻璃棒摩擦瓶壁,析出晶体量增加,但是仍达不到理想值,于是重新进行此组实验。改进后的第二次实验结果仍不是很理想。
2. 加热回流过程中圆底烧瓶中固体太多,阻碍了反应进行,生成产物少。
3. 热过滤过程中,由于保温漏斗温度不够,热过滤损失很多,导致产率偏低。
4.2 安息香纯度分析
安息香文献提供其熔点为137℃,纯的有机物熔程很窄,一般不超过0.5~1℃。此数值与表3-2四组产品的熔点及熔程进行对比可知,四组产品熔点都偏低,熔程较宽,说明产品中含有杂质,都不是纯的有机物。导致此种情况原因:
1. 苯甲醛与安息香在乙醇中都溶解,热过滤过程中不易除去未反应的苯甲醛杂质。
2. 精产品没有干燥充分或是研钵、表面皿不干燥,少量水混入产品。
3. 熔点测定过程中温度升高太快,给实验结果带来一定影响。
4.研钵本身不干净,将原来少量的杂质混入其中。
5.抽虑过程中,洗涤效果不好。
4.3 安息香结构分析
比较分析产品IR谱和标准IR谱。
10
基础化学综合试验 35003250300017501500
图2 IR谱图图 4-1 安息香产品安息香产品IR谱图
吸
收100强
度
50
4000300020001500
-11000300 图1 安息香标准 IR谱图(波数cm) 图 4-2 安息香标准IR谱图
分析知:
1.O—H基伸缩振动出现在3650~3200cm-1,产品谱图在3412.08和3375.43处出现峰值,由此可知,安息香结构中有-OH存在。
2.C=O伸缩振动出现在1900~1650cm-1,而且吸收峰很强,产品在1678.07处
11
基础化学综合试验
出现一强吸收峰,说明安息香结构中存在C=O。
3.单核芳烃的C=C伸缩振动出现在1600和1500cm-1附近,有2~4个峰,产品在1595.3和1448.54附近出现四个峰,所以可证明有苯环存在。
4.—CH基的吸收峰出现在2890cm-1附近,但强度较弱,产品在2931.80处出现一弱峰,说明有—CH存在。
5.C—O的伸缩振动在1300~1000cm-1,产品在1207.44和1263.37处出现峰值,说明有C—O键存在。
与标准谱图相比,产品谱图有些差别,说明我们的产品不是很纯,应该混有其它杂质。
4.4 心得体会
一个周的实验让我感悟到了许多,不仅学到了一些相关实验的知识以及操作方法,综合运用了以前的基础化学实验理论和实践知识,,而且,自己独立思考了很多问题,加深了对相关知识的印象,对抽象的课本知识有了更加具体的理性认识。整个实验我们很努力的去做,遇到很多问题,比如说,第一次冷却结晶时,别人的都有很多晶体,而我们的几乎没有,当时真的很失落,感觉自己的努力没有得到回报,不过经老师指点,我们采取一些措施,晶体量增加,我们仔细分析这些方法的原因,理论知识得以加固,感觉学到了更多的东西,因此,失败是成功之母这话言之有理,而且,失败会让我们成功的更加心安理得,更加有价值。以后几天的实验,我们不再害怕失败!
在实验过程中,我体会到的合作的重要性,没有同伴的努力,没有我们默契的合作,没有我们一次与一次的探讨,我们甚至不能将实验完成,虽然,实验中有很多漏洞,有很多不满意的地方还要我们在以后的学习中继续努力克服,但是我们的合作很愉快。因为我们都努力了,没有座位可以坐一会儿,没有午睡,一站就是六七个小时,每天累得腿疼,下午回到宿舍倒头就睡,这一切我都觉得很充实。
最后,还得感谢赵老师的指引,没有这根强有力指挥棒,我们甚至不知从何做起。
12
基础化学综合试验
参考文献
[1] 杜登学,马万勇.基础化学实验简明教程.化学工业出版社,2007.8
[2] 关烨第,李翠娟,葛树丰修订.有机化学实验第二版.北京大学出版社,2002.11
[3] 叶宪曾,张新祥.仪器分析教程第二版.北京大学出版社,2007.1
13
-
安息香的辅酶合成(完整版)
南昌大学有机化学实验报告学生姓名小田田学号专业班级实验类型验证综合设计创新实验日期20xx年4月28日实验地点同组学生姓名指导教师…
-
安息香的辅酶合成
安息香的辅酶合成一实验目的1学习安息香辅酶合成的制备原理和方法进一步掌握回流冷凝抽滤等基本操作2了解酶催化的特点二实验原理安息香又…
-
安息香的辅酶合成及氧化
安息香的辅酶合成及氧化一实验目的1掌握安息香的辅酶合成和氧化路线及实验方法2熟练掌握重结晶的实验方法3熟知利用薄层层析法检测反应进…
-
安息香的辅酶合成及转化
安息香的辅酶合成及转化实验目的学习安息香辅酶合成及转化的制备原理和方法了解多步骤有机合成的方法进一步掌握回流冷却抽滤等基本操作实验…
-
安息香辅酶合成法 开题报告
论文开题报告课题名称安息香的辅酶合成法姓名高珊学号院系所湘雅医学院专业临床八年制指导教师李洁选题时间20xx年09月22日1论文选…
-
安息香的辅酶合成(完整版)
南昌大学有机化学实验报告学生姓名小田田学号专业班级实验类型验证综合设计创新实验日期20xx年4月28日实验地点同组学生姓名指导教师…
-
安息香的辅酶合成及氧化
安息香的辅酶合成及氧化一实验目的1掌握安息香的辅酶合成和氧化路线及实验方法2熟练掌握重结晶的实验方法3熟知利用薄层层析法检测反应进…
-
安息香辅酶合成法 开题报告
论文开题报告课题名称安息香的辅酶合成法姓名高珊学号院系所湘雅医学院专业临床八年制指导教师李洁选题时间20xx年09月22日1论文选…
-
安息香的辅酶合成及转化
安息香的辅酶合成及转化实验目的学习安息香辅酶合成及转化的制备原理和方法了解多步骤有机合成的方法进一步掌握回流冷却抽滤等基本操作实验…
-
安息香的辅酶合成
安息香的辅酶合成一实验目的1学习安息香辅酶合成的制备原理和方法进一步掌握回流冷凝抽滤等基本操作2了解酶催化的特点二实验原理安息香又…