安息香的辅酶合成(完整版)
实验三:安息香的辅酶合成
一:实验目的
1、 学习安息香辅酶合成的制备原理和方法。
2、 进一步掌握回流、冷却、抽滤等基本操作。
3、了解酶催化的特点
二:实验基本原理(或主、副反应式)
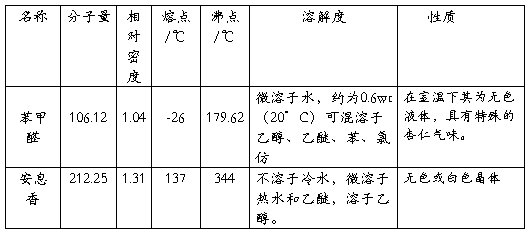
三:主要试剂及主要主副产物的物理常数
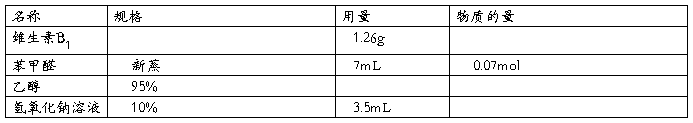
四、主要试剂规格及用量
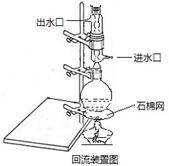
五、实验装置图
主要仪器:圆底烧瓶,试管,冷凝管,烧杯,抽滤装置,玻璃棒等。
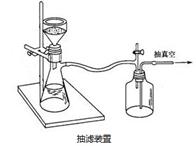
六、实验步骤及现象


七、实验结果及分析
实验中用去0.07mol苯甲醛,理论上应得到0.035mol安息香,得到的理论产量为:
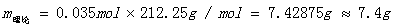
实际产量为: m实际=0.5g
产率:
本次实验产量很低,其可能的原因有以下几点:
1、滴加氢氧化钠溶液过快,导致局部温度升高而使部分维生素B1催化活性失效,致使产量较低;
2、在实验中可能滴加了过多了氢氧化钠,而使部分维生素B1分解;
3、在抽滤时,由于结晶不完全等因素会造成产量进一步降低。
八、实验思考
1、本实验中有哪些特别注意事项?
答:a、调节PH时,溶液一定要摇匀,且PH要调到9—10;
b、维生素B1在酸性条件下稳定,易吸收水,在水溶液中易被空气氧化,且再滴加氢氧化钠时,要冷却的氢氧化钠,防止维生素B1开环失效;
c、再水浴加热时,温度一定要保持在60-75摄氏度,不可加热至沸腾;
d、加热回流时一定要加入沸石,防止暴沸。
e、若产物呈油状物析出,应重新加热使呈均相,再慢慢冷却重新结晶。必要时可用玻璃棒摩擦瓶壁或投入晶种。
2、为什么加入苯甲酸后,反应混合物的ph要保持在9-10?
答:在碱性环境下,VB1形成碳负离子,催化亲核加成反应。pH一低,酸性强了,VB1就无法形成C-离子了(结合H+变回成VB1了)。pH值过高的话,也就是碱性太强的话,原料苯甲醛就会发生歧化反应生成苯甲醇和苯甲酸,不但导致合成安息香的收率大大下降,还使反应体系多了两个副产物,增加分离难度。
这反应叫做Cannizzaro反应,定义如下:无α-活泼氢原子的醛,在强碱作用下,发生分子间氧化-还原反应,一个分子的醛基氢以氢负离子的形式转移给另一分子,结果一分子被氧化成酸,而另一分子则被还原为醇,故又称为歧化反应。
苯甲醛合成安息香一般用氢氧化钠,pH太高,就是NaOH加太多,这时候,氢氧根HO-就会去进攻苯甲醛的醛基碳,碳氧双键其中一对电子先转移到氧原子上,这时候整个分子电子过于富裕,原来的醛基碳变得很排斥电子,于是原来醛基上的那个氢带着一对电子奔向另一个苯甲醛的羰基碳而去形成苯甲醇负离子,这个苯甲醇负离子很容易就从氢氧化钠溶液的H2O中夺取一个氢成了苯甲醇,而第一分子醛上原来转移到氧原子上的那对电子看到失去一个氢的醛基碳带了正电,于是便向它奔来,又形成碳氧双键,苯甲酸就形成了。
第二篇:安息香的辅酶合成










-
安息香的辅酶合成(完整版)
南昌大学有机化学实验报告学生姓名小田田学号专业班级实验类型验证综合设计创新实验日期20xx年4月28日实验地点同组学生姓名指导教师…
-
安息香的辅酶合成
安息香的辅酶合成一实验目的1学习安息香辅酶合成的制备原理和方法进一步掌握回流冷凝抽滤等基本操作2了解酶催化的特点二实验原理安息香又…
-
安息香的辅酶合成及氧化
安息香的辅酶合成及氧化一实验目的1掌握安息香的辅酶合成和氧化路线及实验方法2熟练掌握重结晶的实验方法3熟知利用薄层层析法检测反应进…
-
安息香的辅酶合成及转化
安息香的辅酶合成及转化实验目的学习安息香辅酶合成及转化的制备原理和方法了解多步骤有机合成的方法进一步掌握回流冷却抽滤等基本操作实验…
-
安息香辅酶合成法 开题报告
论文开题报告课题名称安息香的辅酶合成法姓名高珊学号院系所湘雅医学院专业临床八年制指导教师李洁选题时间20xx年09月22日1论文选…
-
安息香的辅酶合成及氧化
安息香的辅酶合成及氧化一实验目的1掌握安息香的辅酶合成和氧化路线及实验方法2熟练掌握重结晶的实验方法3熟知利用薄层层析法检测反应进…
-
安息香辅酶合成法 开题报告
论文开题报告课题名称安息香的辅酶合成法姓名高珊学号院系所湘雅医学院专业临床八年制指导教师李洁选题时间20xx年09月22日1论文选…
-
辅酶催化法合成安息香--溶液pH值对合成安息香产率的影响
辅酶催化法合成安息香溶液pH值对合成安息香产率的影响实验人员学号姓名笑天专业班级高分子101班指导老师姓名黑晓明目录摘要3关键词3…
-
安息香的辅酶合成及转化
安息香的辅酶合成及转化实验目的学习安息香辅酶合成及转化的制备原理和方法了解多步骤有机合成的方法进一步掌握回流冷却抽滤等基本操作实验…
-
安息香的辅酶合成
安息香的辅酶合成一实验目的1学习安息香辅酶合成的制备原理和方法进一步掌握回流冷凝抽滤等基本操作2了解酶催化的特点二实验原理安息香又…