ʵ��ʮ�� ����������ֽ�
2.3 ����ѧ����
ʵ��ʮ�� ����������ֽ⪤
1 Ŀ��Ҫ��
(1) �ⶨ��������ֽ�ķ�Ӧ�ٶȳ����� ��
(2) �˽���������о�����ѧ�Ļ���ԭ������
(3) �˽�ʵ��ⶨ���E��ԭ���ͷ�������
2 ����ԭ����
����������û�д���ʱ���ֽⷴӦ���еú������������ʱ�ܴٽ���ֽ⡣��������ֽ�Ļ�ѧ����ʽ���£�
H2O2��H2O+1/2O2��
�ܶ����ʶ��ܶ���һ��Ӧ������ã��粬������Ǧ���������̡����Ȼ����Լ����Ȼ������Ȼ�ͭ�Ļ����ȡ���ʵ���������Ȼ������Ȼ�ͭ��������������о�H2O2�ֽⷴӦ�Ķ���ѧ������CuCl2��������������ʹ�����������ܴ��÷�Ӧ��
�ڱ�ʵ�������£���������ķֽ���һ����Ӧ���� �� a ��ʾH2O2����ʼŨ�ȣ�x��ʾ��ʱ�� t ʱ�Ѿ��ֽ����H2O2��Ũ�ȣ�����ʣ���H2O2��Ũ��Ϊ(a-x)�������У�

������ʽ���� ln(a-x)= -k1t + lna
ʽ��k1Ϊ��Ӧ���ʳ��������Ĵ�С�����ŷ�Ӧ���ʵĿ�����lnaΪ���ֳ���������t=0��x=0����һ�߽������ó���
����H2O2�Ĵ��ֽ��У�t ʱ��H2O2��Ũ��Ct ��ͨ����������Ӧ��ʱ���ڷֽ�ų�������������ó�����ֽ�����зų������������ֽ��˵�H2O2��Ũ�ȳ����ȣ����������Ϊ��ֵ��.��V�� ��ʾH2O2ȫ���ֽ�ų������������Vt ��ʾH2O2�� t ʱ�̷ֽ�ų����������������
��C0 ��V���� Ct��(V��-Vt��)��
ʽ�У�C0��Ct���ֱ����H2O2��t = 0 �� t =t ʱ��Ũ�ȡ��������ϵʽ����һ����Ӧ���ʷ��̵Ķ����ֱ���ʽ�����У�
��
���ߪ� lg(V��-Vt) = - k1t/2.303 + lgV������,
������ʽ�������lg(V��-Vt)��t��ͼ��һֱ�ߣ�������֤�÷�Ӧ��һ����Ӧ����ʱ��ֱ�ߵ�б�ʿ������Ӧ���ʳ���k1����
��V���������ַ����ó�����
(1)ʵ��ó���
(2)��ʽ�������
���㹫ʽ���£���H2O2�ֽⷴӦ�Ļ�ѧ����ʽ��1mol H2O2�ų�1/2molO2����������Һ����KMnO4����Һ�ζ�H2O2��Һ��V������ڣ�
V�� =MH2O2·��VH2O2·��RT/p�� (m3)��
ʽ�У�MH2O2·������H2O2����ʼĦ��Ũ��mol·L-1��
���� ��V H2O2������H2O2��Һ�����(m 3)��
����p�����������ķ�ѹ��������ѹ��ȥʵ���¶���ˮ�ı�������ѹ(Pa)��
����T ����ʵ�������ѧ�¶�(K)��
����R���������峣����ȡ8.314J·K-1·mol-1��
�������ַ�������KMnO4�ζ�H2O2��Ũ�ȣ��Ƚ��鷳������һ�㶼��ʵ�鷨ֱ�ӻ�á��� ������Ǹı�ֽⷴӦ���¶ȣ���ò�ͬ�¶��µķ�Ӧ���ʳ���k1������ݰ�������˹��ʽ���У�

���ֺ��֪������lnk��1/T��ͼ����б���������ڸ÷�Ӧ�¶ȷ�Χ�ڵ�ƽ����ܡ�
�� ��������о���ѧ��Ӧ����ѧ�Ļ�������֮һ��ֻҪ��Ӧ��������ϵ������������Եı仯��һ�㶼�������ַ����о��÷�Ӧ�Ķ���ѧ����
3 �����Լ�
�� ���²� 1�ף������ 1ֻ��
���Һ 0.05mol·L-1��FeCl3-0.005mol·L-1CuCl2-0.4mol·L-1HCl��0.2mol ·L-1��H2O2��
4 ʵ�鲽�誥
(1) ʵ��װ��ͼ��ͼ2.15.1��ʾ��
ʵ��ǰ�������ϵͳ�Ƿ�©����Ϊ�ˣ�����A���ο�����B�����ˮƿC��ʹ������D�ڵ�ˮ�������ϲ����رջ���A����ˮƿ���������ϡ���������B������A����ˮ���������䣬������ijһλ�ñ��־�ֹ����֤��ϵͳ��©�������ɿ�ʼʵ�顣
(2) �ο�����B������A�����ˮƿC��ʹD���ڵ�ˮƽ������������0�̶����ϣ� �ر�A���ٵ���A��ʹD���ڵ�ˮ��ǡ�ڿ̶�0��λ�á���ȡ20mL H2O2��Һע��B������ 10mL���Һ���漴��������������ʱH2O2�ѿ�ʼ�ֽ⣬���ϵ��ڻ���A��ʹ�����������ڵ�ˮ�汣����ͬ��������ų��ٶ������ȶ���(Լ10min)������D����ˮƽ��Ŀ̶ȣ�ͬʱ�������ÿ5min��¼һ��D����ˮ���λ�á���¼8����10�����ݡ�
Ϊ�õ�H2O2ȫ���ֽ������V���������8����10��Vt ����Թ�ƿ����80��ˮԡ�м��ȣ�������ҡ��������Ӧ���ڲ��������ݷų�Ϊֹ��ȡ����Ӧ�ܣ��ԷŻ�ԭ���²��ں��º�ȡ��������ˮ��̶ȣ���V����ֵ��������������������������������

ͼ2.15.1 ��������ֽ�װ�ê���
��ʵ���������H2O2�ֽⷴӦ�Ļ�ܣ��ı䷴Ӧ�¶ȣ��ֱ�ⶨ25�桢30�桢35�桢40����¶��µ����ʳ���������ͬ�ϡ� ��
5 ���ݴ�����
(1)�ɰ����и�ʽ��¼ʵ�����ݡ�
���£� ����ѹ���� ���²��¶��� V����=��

��2����lg(V��-Vt)Ϊ�����꣬ʱ��t Ϊ��������lg(V��-Vt) �� t��ͼ����ֱ��б�ʼ���ֽⷴӦ�����ʳ�����k��min-1������
6 ע�����
(1) �����������¶Ⱥ�ѹ��Ӱ��ϴ���ʵ����Ҫ��֤����õ�Vt��V����������ͬ���¶Ⱥ�ѹ���µ����ݡ���
(2 )Ҫ�������������ѧ������Vt��V���ĺ��壬�������ڽ������ݴ���ʱ�Ͳ�����ִ���
�����ɱ��������ֳ�http://bmh88.com��������
�ڶ�ƪ��ʵ��ʮ�� ����������ֽ�
2.3 ����ѧ����
ʵ��ʮ�� ����������ֽ⪤
1 Ŀ��Ҫ��
(1) �ⶨ��������ֽ�ķ�Ӧ�ٶȳ����� ��
(2) �˽���������о�����ѧ�Ļ���ԭ������
(3) �˽�ʵ��ⶨ���E��ԭ���ͷ�������
2 ����ԭ����
����������û�д���ʱ���ֽⷴӦ���еú������������ʱ�ܴٽ���ֽ⡣��������ֽ�Ļ�ѧ����ʽ���£�
H2O2��H2O+1/2O2��
�ܶ����ʶ��ܶ���һ��Ӧ������ã��粬������Ǧ���������̡����Ȼ����Լ����Ȼ������Ȼ�ͭ�Ļ����ȡ���ʵ���������Ȼ������Ȼ�ͭ��������������о�H2O2�ֽⷴӦ�Ķ���ѧ������CuCl2��������������ʹ�����������ܴ��÷�Ӧ��
�ڱ�ʵ�������£���������ķֽ���һ����Ӧ���� �� a ��ʾH2O2����ʼŨ�ȣ�x��ʾ��ʱ�� t ʱ�Ѿ��ֽ����H2O2��Ũ�ȣ�����ʣ���H2O2��Ũ��Ϊ(a-x)�������У�
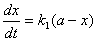
������ʽ���� ln(a-x)= -k1t + lna
ʽ��k1Ϊ��Ӧ���ʳ��������Ĵ�С�����ŷ�Ӧ���ʵĿ�����lnaΪ���ֳ���������t=0��x=0����һ�߽������ó���
����H2O2�Ĵ��ֽ��У�t ʱ��H2O2��Ũ��Ct ��ͨ����������Ӧ��ʱ���ڷֽ�ų�������������ó�����ֽ�����зų������������ֽ��˵�H2O2��Ũ�ȳ����ȣ����������Ϊ��ֵ��.��V�� ��ʾH2O2ȫ���ֽ�ų������������Vt ��ʾH2O2�� t ʱ�̷ֽ�ų����������������
��C0 ��V���� Ct��(V��-Vt��)��
ʽ�У�C0��Ct���ֱ����H2O2��t = 0 �� t =t ʱ��Ũ�ȡ��������ϵʽ����һ����Ӧ���ʷ��̵Ķ����ֱ���ʽ�����У�
��
���ߪ� lg(V��-Vt) = - k1t/2.303 + lgV������,
������ʽ�������lg(V��-Vt)��t��ͼ��һֱ�ߣ�������֤�÷�Ӧ��һ����Ӧ����ʱ��ֱ�ߵ�б�ʿ������Ӧ���ʳ���k1����
��V���������ַ����ó�����
(1)ʵ��ó���
(2)��ʽ�������
���㹫ʽ���£���H2O2�ֽⷴӦ�Ļ�ѧ����ʽ��1mol H2O2�ų�1/2molO2����������Һ����KMnO4����Һ�ζ�H2O2��Һ��V������ڣ�
V�� =MH2O2·��VH2O2·��RT/p�� (m3)��
ʽ�У�MH2O2·������H2O2����ʼĦ��Ũ��mol·L-1��
���� ��V H2O2������H2O2��Һ�����(m 3)��
����p�����������ķ�ѹ��������ѹ��ȥʵ���¶���ˮ�ı�������ѹ(Pa)��
����T ����ʵ�������ѧ�¶�(K)��
����R���������峣����ȡ8.314J·K-1·mol-1��
�������ַ�������KMnO4�ζ�H2O2��Ũ�ȣ��Ƚ��鷳������һ�㶼��ʵ�鷨ֱ�ӻ�á��� ������Ǹı�ֽⷴӦ���¶ȣ���ò�ͬ�¶��µķ�Ӧ���ʳ���k1������ݰ�������˹��ʽ���У�
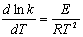
���ֺ��֪������lnk��1/T��ͼ����б���������ڸ÷�Ӧ�¶ȷ�Χ�ڵ�ƽ����ܡ�
�� ��������о���ѧ��Ӧ����ѧ�Ļ�������֮һ��ֻҪ��Ӧ��������ϵ������������Եı仯��һ�㶼�������ַ����о��÷�Ӧ�Ķ���ѧ����
3 �����Լ�
�� ���²� 1�ף������ 1ֻ��
���Һ 0.05mol·L-1��FeCl3-0.005mol·L-1CuCl2-0.4mol·L-1HCl��0.2mol ·L-1��H2O2��
4 ʵ�鲽�誥
(1) ʵ��װ��ͼ��ͼ2.15.1��ʾ��
ʵ��ǰ�������ϵͳ�Ƿ�©����Ϊ�ˣ�����A���ο�����B�����ˮƿC��ʹ������D�ڵ�ˮ�������ϲ����رջ���A����ˮƿ���������ϡ���������B������A����ˮ���������䣬������ijһλ�ñ��־�ֹ����֤��ϵͳ��©�������ɿ�ʼʵ�顣
(2) �ο�����B������A�����ˮƿC��ʹD���ڵ�ˮƽ������������0�̶����ϣ� �ر�A���ٵ���A��ʹD���ڵ�ˮ��ǡ�ڿ̶�0��λ�á���ȡ20mL H2O2��Һע��B������ 10mL���Һ���漴��������������ʱH2O2�ѿ�ʼ�ֽ⣬���ϵ��ڻ���A��ʹ�����������ڵ�ˮ�汣����ͬ��������ų��ٶ������ȶ���(Լ10min)������D����ˮƽ��Ŀ̶ȣ�ͬʱ�������ÿ5min��¼һ��D����ˮ���λ�á���¼8����10�����ݡ�
Ϊ�õ�H2O2ȫ���ֽ������V���������8����10��Vt ����Թ�ƿ����80��ˮԡ�м��ȣ�������ҡ��������Ӧ���ڲ��������ݷų�Ϊֹ��ȡ����Ӧ�ܣ��ԷŻ�ԭ���²��ں��º�ȡ��������ˮ��̶ȣ���V����ֵ��������������������������������

ͼ2.15.1 ��������ֽ�װ�ê���
��ʵ���������H2O2�ֽⷴӦ�Ļ�ܣ��ı䷴Ӧ�¶ȣ��ֱ�ⶨ25�桢30�桢35�桢40����¶��µ����ʳ���������ͬ�ϡ� ��
5 ���ݴ�����
(1)�ɰ����и�ʽ��¼ʵ�����ݡ�
���£� ����ѹ���� ���²��¶��� V����=��

��2����lg(V��-Vt)Ϊ�����꣬ʱ��t Ϊ��������lg(V��-Vt) �� t��ͼ����ֱ��б�ʼ���ֽⷴӦ�����ʳ�����k��min-1������
6 ע�����
(1) �����������¶Ⱥ�ѹ��Ӱ��ϴ���ʵ����Ҫ��֤����õ�Vt��V����������ͬ���¶Ⱥ�ѹ���µ����ݡ���
(2 )Ҫ�������������ѧ������Vt��V���ĺ��壬�������ڽ������ݴ���ʱ�Ͳ�����ִ���
7˼���⪥
��Ӧ���ʳ�������Щ�����й�?��Ϊʲô��ÿ�ζ�ȡVt��V��ʱ��һ��Ҫ�������������ڵ�ˮ����ƽ��
-
��������Ĵ��ֽ�ʵ�鱨��
��������Ĵ��ֽ�һʵ��Ŀ��1�þ�̬���ⶨH2O2�ֽⷴӦ���ٶȳ����Ͱ�˥��2��Ϥһ����Ӧ�ص��˽ⷴӦ��Ũ���¶ȴ��������ض�һ����
-
ʵ��14 ����������ֽⷴӦ���ʳ����IJⶨ
�ӱ��Ƽ���ѧ�̰���ֽ�ڴο�4ѧʱ��1ҳ�ӱ��Ƽ���ѧ�̰���ֽʵ��14����������ֽⷴӦ���ʳ����IJⶨһʵ��Ŀ��1�ⶨ����������֡�
- ��������������о� ʵ�鱨��
-
��������Ĵ��ֽ�ʵ��
��������Ĵ��ֽ�һʵ��Ŀ��1��Ϥһ����Ӧ�ص��˽ⷴӦŨ���¶Ⱥʹ��������ض�һ����Ӧ�ٶȵ�Ӱ��2�þ�̬����H2O2�ֽⷴӦ�ķ�Ӧ��
- ��������Ĵ��ֽ�
-
��������Ĵ��ֽ�ʵ�鱨��
��������Ĵ��ֽ�һʵ��Ŀ��1�þ�̬���ⶨH2O2�ֽⷴӦ���ٶȳ����Ͱ�˥��2��Ϥһ����Ӧ�ص��˽ⷴӦ��Ũ���¶ȴ��������ض�һ����
-
ʵ��14 ����������ֽⷴӦ���ʳ����IJⶨ
�ӱ��Ƽ���ѧ�̰���ֽ�ڴο�4ѧʱ��1ҳ�ӱ��Ƽ���ѧ�̰���ֽʵ��14����������ֽⷴӦ���ʳ����IJⶨһʵ��Ŀ��1�ⶨ����������֡�
- ��������������о� ʵ�鱨��
-
����������ֽⷴӦ���ʳ����IJⶨ
����������ֽⷴӦ���ʳ����IJⶨ��ǩ��ѧʵ�鱨��������ⷴӦ���ʳ�����������ҩѧ����һʵ��Ŀ��1�˽����������ֽⷴӦ���ʳ�����
-
̽����ͬ�����Թ�������ֽⷴӦ���ʵ�Ӱ�� �̰�
����̽����ͬ�����Թ�������ֽⷴӦ���ʵ�Ӱ��һ�̲����ݽ̲İ汾�ս̰���ͨ���пγ̱�ʵ��̿���ʵ�黯ѧѡ��������42�����Թ���
- ʵ�鱨��̽����ͬ�����¹�������ķֽ�