实验2 蛋白质含量测定(考马斯亮蓝G-250法)
实验三 蛋白质含量测定(考马斯亮蓝G-250法)
一、目的
1.学习一种蛋白质染色测定的方法
2.掌握考马斯亮蓝法测定蛋白质含量的基本原理和方法
二、原理
蛋白质的存在影响酸碱滴定中所用某些指示剂的颜色变化,从而改变这些染料的光吸收。在些基础上发展了蛋白质染色测定方法。涉及的指示剂有甲基橙、考马斯亮蓝、溴甲酚绿和溴甲酚紫。目前广泛使用的染料是考马斯亮蓝。
考马斯亮蓝G-250在酸性溶液中为棕红色,当它与蛋白质通过范德华键结合后,变为蓝色,且在蛋白质一定浓度范围内符合比尔定律,可在595nm处比色测定。2~5分钟即呈最大光吸收,至少稳定1小时。在0.01~1.0 mg蛋白质/ml范围内均可。该法操作简便迅速,消耗样品量少,但不同蛋白质之间差异大,且标准曲线线性差。高浓度的Tris、EDTA、尿素、甘油、蔗糖、丙酮、硫酸铵和去污剂时测定有干扰。缓冲液浓度过高时,改变测定液pH值会影响显色。考马斯亮蓝染色能力强,比色杯不洗干净会影响光吸收值,不可用石英怀测定。
三、器材与试剂
1.仪器
(1)分析天平;(2)具塞刻度试管10ml×8;(3)吸管 0.lml×I,lml×Z,5ml×I;(4)研钵;(5)漏斗;
(6)离心管10ml;(7)容量瓶10ml;(8)离心机;(9)721型分光光度计
2.试剂
(1)标准蛋白质溶液 称取10mg牛血清白蛋白,溶于蒸馏水并定容至100ml,制成 100 pg/ml的原液。
(2)考马斯亮蓝G-250蛋白试剂 称取100mg考马斯亮蓝G-250,溶于50ml 90%乙醇中,加入 85%(m/v)的磷酸 100ml,最后用蒸馏水定容到 1000ml。
此溶液在常温下可放置一个月。
3.材料
植物种子
四、操作步骤
1.标准曲线的制作 取6支具塞试管,编号后,按下表加入试剂。
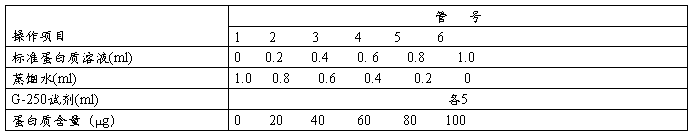
盖上塞子,摇匀。放置2min后在595 nm波长下比色测定(比色应在 l h内完成)。以牛血清白蛋白含量(μg)为横坐标,以吸光度为纵坐标,绘出标准曲线。
2.样品中蛋白质含量的测定
(1)准确称取约200mg绿豆芽下胚轴,放入研钵中,加入5ml蒸馏水在冰浴中研成匀浆,离心(4000r/min,10min),将上清液倒入10ml容量瓶,再向残渣中加入2ml蒸馏水,悬浮后再离心10min,合并上清液,定至刻度。
(2)另取1支具塞试管,准确加入0.l ml样品提取液,再加入0.9 ml蒸馏水,5ml考马斯亮蓝G-250试剂,充分混合,放置2min后,以标准曲线1号试管做参比,在595 nm波长下比色,记录吸光度。
3.结果处理
根据所测样品提取液的吸光度,在标准曲线上查得相应的蛋白质含量(μg),按下式计算:
样品蛋白质含量(μg/g鲜重)=(查得的蛋白质含量(μg)×提取液总体积(ml))/(样品鲜重(g)×测定时取用提取液的体积(ml))
六、注意事项
1.由于染料本身的两种颜色形式的光谱有重叠,试剂背景值会因与蛋白质结合的染料增加而不断降低,因而当蛋白质浓度较大时,标准曲线稍有弯曲,但直线弯曲程度很轻,不致影响测定
2.测定工作应在蛋白质染料混合后2min开始,力争1hr内完成,否则会因蛋白质一染料复合物发生凝集沉淀而影响测定结果。
3.样品中的Tris、乙酸、2-巯基乙醇、EDTA等物质对实验结果有少量颜色干扰,可以在做标准曲线时可以用缓冲液代替蒸馏水,就可以将干扰扣除,
七、思考题
1.考马斯亮蓝G-250法测定蛋白质含量的原理是什么?还有哪些蛋白质定量法?
2.如何正确使用分光光度计?
八、参考文献
鲁子贤.蛋白质化学.北京:科学出版社,1981
文树基.基础生物化学实验指导.西安:陕西科学技术出版社,1994
张龙翔.生物化学实验技术.北京:人民教育出版社,1981
第二篇:考马斯亮蓝
标准曲线制作—考马斯亮蓝法测蛋白质含量
一、 标准曲线
一般用分光光度法测物质的含量,先要制作标准曲线,然后根据标准曲线查出所测物质的含量。因此,制作标准曲线是生物检测分析的一项基本技术。
二、 蛋白质含量测定方法
1、 凯氏定氮法
2、 双缩脲法
3、 Folin-酚试剂法
4、 紫外吸收法
5、 考马斯亮蓝法
三、 考马斯亮蓝法测定蛋白质含量—标准曲线制作
(一)、试剂:
1、 考马斯亮蓝试剂:
考马斯亮蓝G—250 100mg溶于50ml 95%乙醇,加入100ml 85% H3PO4,雍蒸馏水稀释至1000ml,滤纸过滤。最终试剂中含0.01%(W/V)考马斯亮蓝G—250,4.7%(W/V)乙醇,8.5%(W/V)H3PO4。
2、 标准蛋白质溶液:
纯的牛血清血蛋白,预先经微量凯氏定氮法测定蛋白氮含量,根据其纯度同0.15mol/LNaCl配制成100ug/ml蛋白溶液。
(二)、器材:
1、722S型分光光度计使用及原理()。
2、移液管使用()。
(三)、标准曲线制作:
试管编号 0 1 2 3 4 5 6
100ug/ml标准蛋白(ml) 0.0 0.1 0.2 0.3 0.4 0.5 0.6
0.15mol/L NaCl (ml) 1 0.9 0.8 0.7 0.6 0.5 0.4
考马斯亮蓝试剂 (ml) 5 5 5 5 5 5 5
摇匀,1h内以1号管为空白对照,在595nm处比色
2、以A595nm为纵坐标,标准蛋白含量为横坐标(六个点为10ug、20 ug、30 ug、40 ug、50 ug、60 ug),在坐标轴上绘制标准曲线。
1)、利用标准曲线查出回归方程。
2)、用公式计算回归方程。
3)、或用origin作图 ,测出回归线性方程。即A595nm=a×X( )+6
一般相关系数应过0.999以上,至少2个9以上。
4)、绘图时近两使点在一条直线上,在直线上的点应该在直线两侧。
(四)、蛋白质含量的测定:
样品即所测蛋白质含量样品(含量应处理在所测范围内),依照操作步骤1操作,测出样品的A595nm,然后利用标准曲线或回归方程求出样品蛋白质含量。
一般被测样品的A595nm值在0.1—0.05之间,所以上述样品如果A595nm值太大,可以稀释后再测A595nm值,然后再计算。
实验六 蛋白质含量测定(考马斯亮蓝G-250法)
一、目的
蛋白质是细胞中最重要的含氮生物大分子之一,承担着各种生物功能。蛋白质的定量分析是蛋白质构造分析的基础,也是农牧产品品质分析、食品营养价值比较、生化育种、临床诊断等的重要手段。根据蛋白质的理化性质,提出多种蛋白质定量方法。考马斯亮蓝G-250法是比色法与色素法相结合的复合方法,简便快捷,灵敏度高,稳定性好,是一种较好的常用方法。通过本实验学习考马斯亮蓝G-250法测定蛋白质含量的原理,了解分光光度计的结构、原理和在比色法中的应用。
二、原理
考马斯亮蓝G-250是一种染料,在游离状态下呈红色,当它与蛋白质结合后变为青色。蛋白质含量在0~1000μg范围内,蛋白质一色素结合物在 595nm下的吸光度与蛋白质含量成正比,故可用比色法测定。
三、仪器、试剂和材料
1.仪器
(1)分析天平
(2)具塞刻度试管 10ml× 8
(3)吸管 0.lml×I,lml×Z,5ml×I (4)研钵 (5)漏斗 (6)离心管 10ml
(7)容量瓶 10ml
(8)离心机
(9)721型分光光度计
2.试剂
(1)标准蛋白质溶液 称取10mg牛血清白蛋白,溶于蒸馏水并定容至100ml,制成 100 pg/ml的原液。
(2)考马斯亮蓝G-250蛋白试剂 称取100mg考马斯亮蓝G-250,溶于50ml 90%乙醇中,加入 85%(m/v)的磷酸 100ml,最后用蒸馏水定容到 1000ml。
此溶液在常温下可放置一个月。
3.材料
绿豆芽
四、操作步骤
1.标准曲线的制作 取6支具塞试管,编号后,按下表加入试剂。


盖上塞子,摇匀。放置2min后在595 nm波长下比色测定(比色应在 l h内完成)。以牛血清白蛋白含量(μg)为横坐标,以吸光度为纵坐标,绘出标准曲线。
2.样品中蛋白质含量的测定
(1)准确称取约200mg绿豆芽下胚轴,放入研钵中,加入5ml蒸馏水在冰浴中研成匀浆,离心(4000r/min,10min),将上清液倒入10ml容量瓶,再向残渣中加入2ml蒸馏水,悬浮后再离心10min,合并上清液,定客至刻度。
(2)另取1支具塞试管,准确加入0.l ml样品提取液,再加入0.9 ml蒸馏水,5ml考马斯亮蓝G-250试剂,充分混合,放置2min后,以标准曲线1号试管做参比,在595 nm波长下比色,记录吸光度。
五、结果处理
根据所测样品提取液的吸光度,在标准曲线上查得相应的蛋白质含量(μg),按下式计算:
样品蛋白质含量(μg/g鲜重)=(查得的蛋白质含量(μg)×提取液总体积(ml))/(样品鲜重(g)×测定时取用提取液的体积(ml))
六、注意事项
比色应在出现蓝色2 min~l h内完成。
七、思考题
1.考马斯亮蓝G-250法测定蛋白质含量的原理是什么?还有哪些蛋白质定量法?
2.如何正确使用分光光度计?
参考文献
鲁子贤。蛋白质化学。北京:科学出版社,1981
文树基。基础生物化学实验指导。西安:陕西科学技术出版社,1994
张龙翔.生物化学实验技术。北京:人民教育出版社,1981
-
实验考马斯亮蓝测蛋白质含量
实验7考马斯亮蓝考G250染色法测定蛋白质含量一目的1学习一种蛋白质染色测定的方法2掌握考马斯亮蓝法测定蛋白质含量的基本原理和方法…
-
实验七 考马斯亮蓝G250法测定的蛋白质含量
实验七考马斯亮蓝G250法测定的蛋白质含量一试验目的1学习分光光度计的原理及操作2学习利用染色方法提高蛋白质消光系数以提高分光光度…
-
蛋白质的定量测定---考马斯亮蓝法测定蛋白质浓度
实验名称蛋白质的定量测定考马斯亮蓝法测定蛋白质浓度实验原理考马斯亮蓝法测定蛋白质浓度是利用蛋白质燃料结合的原理考马斯亮蓝G250染…
-
蛋白质含量测定法考马斯亮蓝法
生物化学实验技术课程作业蛋白质含量测定法考马斯亮蓝法实验目的学习掌握考马斯亮蓝法Bradford法测定蛋白质含量的方法实验原理考马…
-
蛋白质浓度测定——考马斯亮蓝染色法(实验报告)
生物化学实验报告蛋白质浓度测定考马斯亮蓝染色法蛋白质浓度测定考马斯亮蓝染色法实验报告实验日期年月日实验温度室温实验地点生物化学与遗…
-
生化综合实验报告--测定蛋白质含量的三种方法及其比较
本科学生综合性实验报告学号姓名学院专业班级实验课程名称测定蛋白质含量的三种方法及其比较教师及职称开课学期月云南师范大学教务处编印一…
-
考马斯亮蓝法测定(实验报告)
考马斯亮蓝法测定苹果组织微量可溶性蛋白含量摘要本实验以苹果果肉为研究对象采取考马斯亮蓝比色法测定蛋白质的吸光度值通过对果实可溶性蛋…
-
蛋白质浓度测定——考马斯亮蓝染色法(实验报告)
生物化学实验报告蛋白质浓度测定考马斯亮蓝染色法蛋白质浓度测定考马斯亮蓝染色法实验报告实验日期年月日实验温度室温实验地点生物化学与遗…
-
实验考马斯亮蓝测蛋白质含量
实验7考马斯亮蓝考G250染色法测定蛋白质含量一目的1学习一种蛋白质染色测定的方法2掌握考马斯亮蓝法测定蛋白质含量的基本原理和方法…
-
实验七 考马斯亮蓝G250法测定的蛋白质含量
实验七考马斯亮蓝G250法测定的蛋白质含量一试验目的1学习分光光度计的原理及操作2学习利用染色方法提高蛋白质消光系数以提高分光光度…
-
实验7 考马斯亮蓝G-250染色法
实验7考马斯亮蓝G250染色法测定蛋白质含量一目的1学习一种蛋白质染色测定的方法2掌握考马斯亮蓝法测定蛋白质含量的基本原理和方法二…