浓缩果汁中维生素c含量的测定实验+++doc
浓缩果汁中维生素c含量的测定实验
本人郑重声明:
所呈交的毕业项目报告/论文《果汁饮料中维生素C含量的测定》是本人在指导老师的指导下,独立研究、写作的成果。论文中所引用是他人的无论以何种方式发布的文字、研究成果,均在论文中以明确方式标明。
本声明的法律结果由本人独自承担。
作者签名:
年 月 日
摘 要: 果汁饮料的主要原料就是水果,其中的主要营养成分是维生素C。维生素C又称为抗坏血酸,属于水溶性维生素,在水溶液中易被空气和其他氧化剂氧化,但在弱酸性条件下较稳定,所以本次用碘量法测定果汁中的维生素C的含量。本次方法简单,可靠,准确度较高,在实验室得到广泛应用。
关键词:果汁饮料;维生素C;碘量法
目 录
1 绪论............................................................................................................. 1
1.1 果汁饮料的概念....................................................................................... 1
1.2 果汁饮料的发展....................................................................................... 1
1.3 对果汁饮料中维生素C测定意义.......................................................... 1
2.实验部分................................................................................................... 3
2.1实验原理.................................................................................................... 3
2.2实验仪器与试剂........................................................................................ 3
2.3 实验步骤................................................................................................. 4
2.4数据处理.................................................................................................... 5
3.结果与分析.......................................................................................................................... 7
3.1数据变动原因............................................................................................ 7
3.2不同方法对比实验.............................................................................................7
3.3酸碱性对维生素C测定的影响.......................................................................
3.4含量影响因素...................................................................................................
4.结论........................................................................................................
参考文献...................................................................................................... 11
致 谢........................................................................................................... 12
果汁饮料中维生素C含量的测定
1 绪论
1.1果汁饮料的概念
果汁饮料是一种以水果为主要原料,经过如压榨、离心、萃取等得到的汁液产品。果汁(浆)及果汁饮料(品)类也可以细分为果汁、果浆、浓缩果浆、果肉饮料、果汁饮料、果粒果汁饮料、水果饮料浓浆、水果饮料等9种类型,其大都采用打浆工艺将水果或水果的可食部分加工制成未发酵但能发酵的浆液或在浓缩果浆中加入果浆在浓缩时失去的天然水分等量的水,制成的具有原水果果肉的色泽、风味和可溶性固形物含量的制品。
各种不同水果的果汁含有不同的维生素等营养,而被视为是一种对健康有益的饮料,但其缺乏水果所有的纤维素和过高的糖分有时被视为其缺点。
1.2 果汁饮料的发展
我国的果汁饮料发展始于上世纪70年代,在80年代处于缓步发展时期,进入90年代有了较快发展,在果汁饮料的品种上,打破了传统的单一桔子型格局,向着品种多样化的方向发展。诸如苹果汁,椰子汁,鲜橙汁等;在品种结构方面有浓缩汁、100%纯果汁、混合汁等;在果汁包装方面,也日趋多样化,有玻璃瓶包装、纸塑复合软包装、金属易拉罐包装等。随着人们生活水平的不断提高,果汁饮料在人们生活中越来越受到青睐,20##年,销售总量首次超越碳酸饮料,仅次于纯净水。从现在看,果汁饮料发展前景非常广阔,具备了非常好的投资优势。
1.3对果汁饮料中维生素C测定的意义
在果汁饮料不断发展的这几十年,已经深受人们的喜爱。人们对果汁的需求也日益不断的扩大,不仅因为它的口感好喝,而且里面所含的营养物质也是人们生活中所必需的,可以一定程度上保证人们的膳食平衡。虽然果汁饮料不断的被人们所喜爱,然而它的营养成分和水果不能相提并论。果汁饮料中所含的主要营养成分就是维生素C,捣碎和压榨的过程使水果中的易氧化的维生素C被破坏掉了。然维生素C是人体必须的微量营养元素,具有调节人体生命活动的作用。现在人们对果汁饮料的依赖,从而慢慢导致维生素C摄取量的缺失,也是对身体健康的一种损坏。摒弃人们对果汁饮料一种错误的传统观念,所以,对果汁饮料中维生素C的测定,具有重要意义。
2 实验部分
2.1实验原理
2.1.1 维生素C
维生素C是人体重要的维生素之一,缺乏时会产生坏血病,故维生素C又称抗坏血酸,属水溶性维生素。维生素C在空气中稳定,但它在水溶液中易被空气和其他氧化剂氧化,生成脱氢抗坏血酸;在碱性条件下易分解,见光加速分解;在弱酸条件中较稳定。
2.1.2 滴定原理
维生素C(C6H8O6, E=0.18),分子结构中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,抗坏血酸分子中的烯二醇基被I2完全氧化后,则I2与淀粉指示剂作用而使溶液变蓝,所以当滴定到溶液出现蓝色时即为终点。
由于维生素C的还原性很强,即使在弱酸性条件下,上述反应也进行得相当完全。维生素C在空气中极易被氧化,尤其在碱性介质中反应强烈,故该滴定反应在稀HAc中进行,以减少维生素C的副反应。
I2标准溶液采用间接配制法获得,用Na2S203标准溶液标定,反应如下:
2S2O32-+I2=S4O62-+2I-
2.2实验仪器与试剂
表1 实验仪器

表2 实验试剂

2.3 实验步骤
2.3.1 0.02mol·L-1 Na2S2O3标准溶液的配制
称取5g Na2S2O3·5H2O,溶于1000ml新煮沸并冷却的蒸馏水中,加入0.2gNa2CO3使溶液呈碱性,以防止Na2S2O3的分解,保存于棕色瓶中,待用。
2.3.2 K2Cr2O7标准溶液的配制
准确称取基准试剂K2Cr2O7 0.26—0.28g于小烧杯中,加入少量蒸馏水溶解后,移入200ml容量瓶中,用蒸馏水稀释至刻度,摇匀。
2.3.3 0.02mol·L-1 Na2S2O3标准溶液的标定
用移液管吸取上述标准溶液20.00ml于250碘量瓶中,加8ml 6mol·L-1 HCI,5-8ml 20%KI溶液,盖上表面皿,在暗处放5分钟后,加100ml水,立即以用待标定的Na2S2O3溶液滴定至淡黄色,再加入2ml0.5%淀粉溶液,继续滴至溶液呈亮绿色为终点,平行滴定3次。
2.3.4 I2标准溶液的配制与标定
(1)I2标准溶液的配制
称取1.3gI2和2.0gKI置于小烧杯中,加少量水,搅拌至I2全部溶解,转入250ml棕色瓶中,加水至250ml,混合均匀。
(2)0.05 mol·L-1I2标准溶液的标定
准确移取20.00ml Na2S2O3溶液标准于250ml锥形瓶中,加50ml蒸馏水、0.5%淀粉指示剂5ml,用I2滴定至稳定的蓝色,30S不褪色即为终点,平行标定三次。
2.3.5 0.5%淀粉溶液的配制
称取1g淀粉于小烧杯中,加少许水调成浆,搅拌下加到200ml沸水中,冷却后备用
2.3.6 2 mol·L-1HAc溶液的配制
取6.4ml冰醋酸(1.05g/ml),加水稀释到500ml,待用。
2.3.7 维生素C含量的测定
取20ml维生素C果汁,置250ml锥形瓶中,加100ml新煮沸过的冷蒸馏水,加入10ml 2mol·L-1HAc和5ml0.5%淀粉指示剂,立即用I2标准溶液滴定至稳定的蓝色,30S内不褪色即为终点。平行测定三份。
2.4数据处理
表3  (mol/L)的测定
(mol/L)的测定

表4 0.02 mol·L-1 Na2S2O3标准溶液的标定

Na2S2O3标准溶液C计算公式:

表5 I2标准溶液的标定
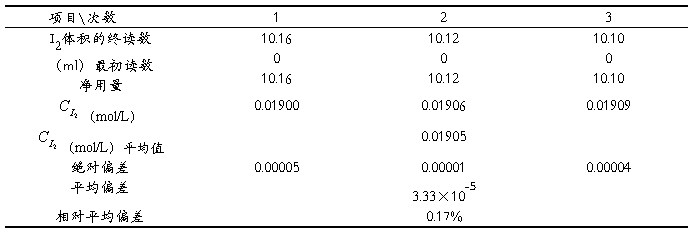
碘标溶液浓度计算:

表5碘量法测得Vc含量数据处理

根据滴定所消耗体积,按以下公式计算

3结果与分析
3.1 数据变动原因
用直接碘量法测维生素C含量时,存在一定的系统误差,使数据出现一定的波动;由于维生素C的强还原性,极易被氧化而使其含量减少,从而使I2的体积消耗减少。
3.2 不同方法对比实验
本次实验对果汁中维生素C的含量测定采用两种方法,比较直接碘量法和间接碘量法的结果,在同一实验条件下用间接碘量法获得的维生素C含量较大,且相对平均偏差也小得多。原因是:采用间接碘量法,减少了维生素C溶液与空气接触时间,并避免了碘的挥发对实验结果造成的影响。
3.3 酸碱性对维生素C测定的影响
抗坏血酸分子中的二烯醇基与I2的氧化反应,在碱性或酸性条件下均可进行,但在酸性介质中抗坏血酸表现稳定,且无副反应,所以反应在稀酸环境中进行更好。不过PH值不能太低。PH值太低,溶液中一些强还原性物质能与维生素C作用;PH值太高,空气中氧能与维生素C发生氧化还原反应,这些都使测定结果偏低,并且精密度不高。实验表明PH值应控制在3-5为宜。
3.4 含量影响因素
由于还原型维生素C的不稳定性,很容易被空气中的氧所氧化,因此,在测定果汁中的还原型维生素C含量时,应尽量缩短样品处理时间,获得检测液后,立即进行分析测试,不要放置过久,以便减少还原型维生素C的氧化损失,保证测定结果的稳定性,避免测定结果偏低。实验中获得的维生素C含量并不高,因为由于样品不足,该果汁是经过稀释的,故含量比新鲜果汁少得多。
4 结论
果汁饮料中含有人类所需的维生素C,还原糖,钾,钠等微量元素。其中主要的营养成分是维生素C。本次测定的方法是用实验室中常用的碘量法对维生素C的测定。这种方法简单,高效,能够较准确的测量出果汁中维生素C的含量。维生素C在人类生命活动中起到重要作用,所以对果汁中维生素C的测定,有利于人们对果汁饮料的充分认知。通过对果汁饮料中维生素C的研究,其含量远远低于水果中的维生素C。然而越来越多的人为了口感喜爱上了果汁饮料,希望通过本次试验研究,能够给那些用果汁饮料代替水果的人们,带来一些思想的转变。
参考文献
致 谢
感谢苏文莉老师对毕业项目进行指导。感谢您在忙碌的教学工作中挤出时间来审查、修改我的论文。导师渊博的专业知识,严谨的治学态度,精益求精的工作作风,诲人不倦的高尚师德,严以律己、宽以待人的崇高风范,朴实无华、平易近人的人格魅力对我影响深远。不仅使我树立了远大的学术目标、掌握了基本的研究方法,还使我明白了许多待人接物与为人处世的道理。
感谢我的母校,大学三年,是知识丰富了我的思想,使我的思想有了进一步的提升。
感谢江苏食品职业技术学院学院的所有专业老师,还有教过我的所有老师们,你们严谨细致、一丝不苟的作风一直是我工作、学习中的榜样;他们循循善诱的教导和不拘一格的思路给予我无尽的启迪。
最后,感谢论文答辩委员会的各位老师!
作者姓名
20##年5月10日
第二篇:学生实验9 维生素C的含量测定
学生实验9 维生素C的含量测定
实验日期:______年____月____日
班级:_____________ 姓名: 小组成员:______________
知识储备:
一、维生素C的基本性质
维生素C(Vitamin C ,Ascorbic Acid)又叫L-抗坏血酸,是一种水溶性维生素。食物中的维生素C被人体小肠上段吸收。一旦吸收,就分布到体内所有的水溶性结构中,正常成人体内的维生素C代谢活性池中约有1500mg维生素C,最高储存峰值为3000mg维生素C。正常情况下,维生素C绝大部分在体内经代谢分解成草酸或与硫酸结合生成抗坏血酸-2-硫酸由尿排出;另一部分可直接由尿排出体外。
物理性质:别名:抗坏血酸 分子式:C6H8O6 分子量:176.13
外观:无色晶体 熔点:190 - 192℃ 溶解性:水溶性维生素
化学性质:
酸性,具有较强的还原性,加热或在溶液中易氧化分解,在碱性条件下更易被氧化,为己糖衍生物。
二、维C泡腾片
维C泡腾片是以维生素C、柠檬酸、碳酸氢钠、葡萄糖为原料,经加工而成。
这种片剂加入水后,柠檬酸与碳酸氢钠反应,释放二氧化碳,因而会有许多气泡冒出水面。
3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3CO2↑
【用法与用量】将一片放入100ml热或凉开水中,每日一片。单片维C泡腾片含470mg维C。
【注意事项】1.本品不能直接吞服;2、严格按说明书要求掌握饮用;3、饭后服用。
【规格】1.8g/片
【保 质 期】24个月
【储藏方法】避光密封,在阴凉干燥处保存。
三、滴定管的使用方法
滴定管(Burette)分为碱式滴定管和酸式滴定管。前者用于量取对玻璃管有侵蚀作用的液态试剂;后者用于量取对橡皮有侵蚀作用的液体。滴定管容量一般为50mL,刻度的每一大格为1mL,每一大格又分为10小格,故每一小格为 0.1mL。可精确到0.01mL。滴定管为一细长的管状容器,一端具有活栓开关,其上具有刻度指示量度。一般在上部的刻度读数较小,靠底部的读数较大。
酸式滴定管使用方法:
1、使用时先检查是否漏液。
2、用滴定管取、滴液体时必须洗涤、润洗。
3、读数前要将管内的气泡赶尽、尖嘴内充满液体。
4、读数需有两次,第一次读数时必须先调整液面在0刻度或0刻度以下。
5、读数时,视线、刻度、液面的凹面最低点在同一水平线上。
6、读数时,边观察实验变化,边控制用量。
7、量取或滴定液体的体积=第二次的读数-第一次读数。
8、用于盛装酸性或强氧化性液体(如KMnO4溶液),不可装碱性溶液。
碱式滴定管使用方法:
1、使用时先检查是否漏液。
2、用滴定管取、滴液体时必须洗涤、润洗。
3、读数前要将管内的气泡赶尽、尖嘴内充满液体。
4、读数时,视线、刻度、液面的凹面最低点在同一水平线上。
5、量取或滴定液体的体积=第二次的读数-第一次读数。
6、绝对禁止用碱式滴定管装酸性及强氧化性溶液,以免腐蚀橡皮管。
7、用于盛装碱性溶液,不可盛装酸性和强氧化剂液体(如KMnO4溶液)
知识拓展:
一、维生素C的营养价值及药物作用
维生素c的主要作用是提高免疫力,预防癌症、心脏病、中风,保护牙齿和牙龈等。另外,坚持按时服用维生素c还可以使皮肤黑色素沉着减少,从而减少黑斑和雀斑,使皮肤白皙。富含维生素c的食物有花菜、青辣椒、橙子、葡萄汁、西红柿等,可以说,在所有的蔬菜、水果中,维生素c含量都不少。美国专家认为,每人每天维生素c的最佳用量应为200~300毫克,最低不少于60毫克,半杯(大约一百毫升)新鲜橙汁便可满足这个最低量。而中国营养学会建议的膳食参考摄入量,成年人为100mg/日,可耐受最高摄入量为1000mg/日。
维生素C在体内参与多种反应,如参与氧化还原过程,在生物氧化和还原作用以及细胞呼吸中起重要作用。从组织水平看,维生素C的主要作用是与细胞间质的合成有关。包括胶原、牙和骨的基质、毛细血管内皮细胞间的接合物。因此,当维生素C缺乏所引起的坏血病时,伴有胶原合成缺陷,表现为创伤难以愈合,牙齿形成障碍和毛细血管破损引起大量瘀血点,瘀血点融合形成瘀斑。
二、富含维生素C的食物(按含量高低排序)

实验目的:
1. 检测待测液中是否含有维生素C。
2. 测定待测液中维生素C的含量。
方法名称:
维生素C测定—氧化还原滴定法
该方法采用滴定法测定维生素C的含量。
实验原理:
1. 维生素C与碘液发生氧化还原反应,I2为氧化剂。
C6H8O6+I2→C6H6O6+2HI
在碘液中加淀粉试液,碘和淀粉试液混合会变蓝色。
当碘和VC反应完全时,蓝色消失,且振摇溶液半分钟不会再变蓝。
2. 维生素C有还原性,可以与高锰酸钾反应,使高锰酸根离子被还原为锰离子,紫红色高锰酸钾溶液褪色。
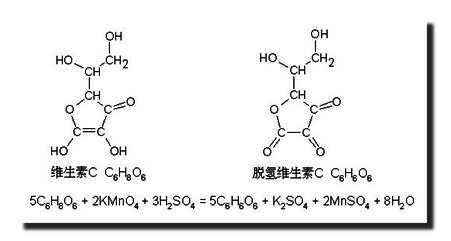
实验仪器及药品:
实验仪器:烧杯2只,三脚架,石棉网,酒精灯,滤纸,漏斗,玻璃棒,酸式滴定管,移液管,试管5只。
实验药品:淀粉指示液,蒸馏水,维生素C泡腾片1片,碘水( ),高锰酸钾(
),高锰酸钾( )溶液。
)溶液。
实验步骤及现象记录:
泡腾片溶液VC含量测定:
方法一:碘淀粉法
实验步骤:

方法二:高锰酸钾溶液法:
实验步骤:

水溶C100 VC含量测定:
方法一:碘淀粉法
实验步骤:

方法二:高锰酸钾溶液法:
实验步骤:
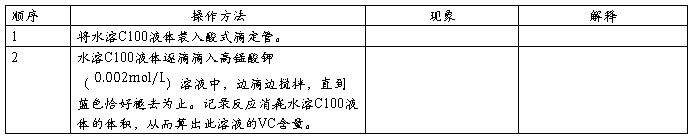
问题讨论
1. 已知重铬酸钾为强氧化剂,试推测VC能否与重铬酸钾发生反应。
2. 用高锰酸钾溶液法、碘淀粉法测得待测液的VC含量与实际值比较可能偏大,试解释原因。
3. 实验过程中,也可以采取将碘水滴加到加了淀粉溶液的待测液中,待待测液变蓝,根据所消耗碘水的浓度、体积推算待测液的VC含量。参考实验时所用药品浓度及实验数据,试比较两种方法优劣。
4. 根据实验结果,比较两种测定方法优劣。
-
维生素C的测定实验报告
附1学生实验报告格式浙江万里学院实验报告课程名称生化实验指导教师谭志文汪财生实验项目维生素C的定量测定26二氯酚靛酚法专业班级生物…
-
实验六 维生素C的定量测定
姓名:**年级专业:2012级生物科学同组者:**学号:***实验六维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、实验目的掌握…
-
维生素C的定量测定实验报告
生物化学实验报告维生素C的定量测定26二氯酚靛酚滴定法一实验目的掌握26二氯酚靛酚滴定法测定维生素C的原理和方法二实验原理维生素C…
-
实验三 维生素C的定量测定
实验三维生素C的定量测定一研究背景维生素C的主要作用是提高免疫力预防癌症心脏病中风保护牙齿和牙龈等另外坚持按时服用维生素C还可以使…
-
化学实验报告 实验__直接碘量法测定维生素C的含量
实验报告姓名班级同组人自评成绩项目直接碘量法测定维生素C的含量课程学号一实验目的1熟悉直接碘量法的操作步骤及注意事项2了解维生素C…
-
紫外光度法测定维生素C实验报告
紫外分光光度法测定维生素C片维生素C的含量一实验目的1学习利用紫外吸收光谱测定物质含量的原理和方法2熟练紫外可见分光光度计的操作二…
-
维生素C的测定实验报告
附1学生实验报告格式浙江万里学院实验报告课程名称生化实验指导教师谭志文汪财生实验项目维生素C的定量测定26二氯酚靛酚法专业班级生物…
-
分析化学设计实验报告单—水果中维生素C的测定
昌吉学院化学与应用化学系20xx20xx学年度第二学期分析化学设计实验化学与应用化学系B0901班做实验者马国民二零一一年六月十九…
-
化学实验报告 实验__直接碘量法测定维生素C的含量
实验报告姓名班级同组人自评成绩项目直接碘量法测定维生素C的含量课程学号一实验目的1熟悉直接碘量法的操作步骤及注意事项2了解维生素C…
-
实验六 维生素C的定量测定
姓名:**年级专业:2012级生物科学同组者:**学号:***实验六维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、实验目的掌握…
-
实验报告2荧光分光光度法测定维生素B2的含量
实验项目荧光分光光度法测定维生素B2的含量实验题目荧光分光光度法测定维生素B2的含量实验目的1掌握标准曲线法定量分析维生素B2的基…