电导的测定及应用实验报告
气温:24.3℃ 气压:70.28Kpa




以KCl溶液的Λm对 作图得一直线,其截距即为KCl的Λ∞m=
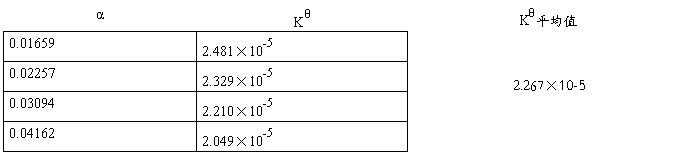
HAc溶液的各组数据

α=Λm/ Λ∞m Kθ=(CΛ∞m2)/ Λ∞mCθ(Λ∞m-Λm)
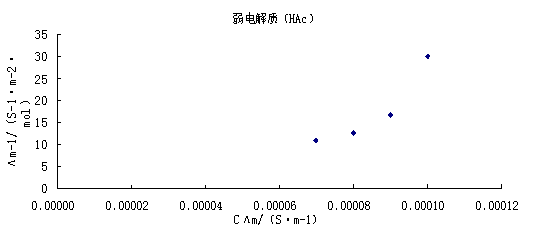
以CΛm对1/Λm作图
由图可知此直线的斜率为4.44727×10-5,所以(Λ∞m)2 KθCθ=4.44727×10-5,
又因为Λ∞m=3.907×10-2(S·m2·mol-1),Cθ=1mol/L;
所以Kθ=4.1963×10-5/((3.907×10-2)2×1×1000)=2.749×10-5
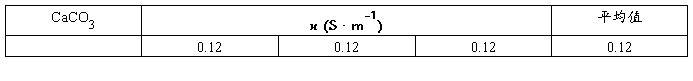
KCaCO3=0.12-0.093=0.027
Λm(1/2CaCO3)≈Λ∞m(1/2CaCO3) Λm(1/2CaCO3)=139.3×10-4
C(1/2CaCO3)= KCaCO3/Λ∞m(1/2CaCO3)
=1.94mol·m-3
C(CaCO3)=1/2 C(1/2CaCO3)
=0.97×10-3mol.L-1
第二篇:原电池电动势的测定及其应用实验报告
原电池电动势的测定及其应用实验报告
林传信 高分子101 1017051012
一、实验目的
1、理解电极、电极电势、电池电动势、可逆电池电动势的意义
2、掌握用对消法测定电池电动势的基本原理和数字式电子电位差计的使用方法
3、学会几种电极和盐桥的制备方法
二、对消法侧电动势的基本原理:
测量电动势只能在无电流通过电池的情况下进行,因此需要用对消法(补偿法)来测定电
动势。对消法测定电动势就是在所研究的电池的外电路上加一个方向相反的电压。当两者
相等时,电路的电流为零(通过检流计指示)。对消法测电动势常用的仪器为电位差计,
其简单原理如图所示
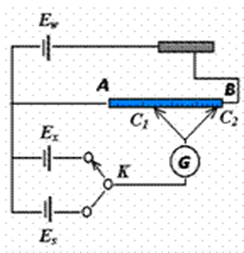

电极电势的测定原理:
原电池是化学能转变为电能的装置,在电池放电反应中,正极(右边)起还原反应,负极起
氧化反应。电池的电动势等于组成的电池的两个电极电位的差值。即:
E=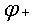 —
—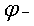 =
=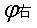 —
—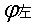
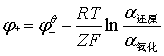
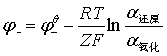 R=8.314J
R=8.314J
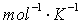
F=96500C 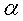 为参与电极反应的物质的活度。纯固体物质的活度为1。
为参与电极反应的物质的活度。纯固体物质的活度为1。
浓差电池:
一种物质从高浓度(或高压力)状态向低浓度(或低压力)状态转移,从而产生电动势,而
这种电池的标准电动势为零。
三、电池组合:
⑴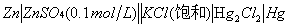
⑵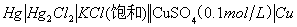
⑶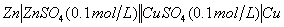
⑷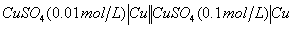
四、数据处理
实验室温度T=281.15 标准电动势Es=1000.03mV
电池电极电动势:
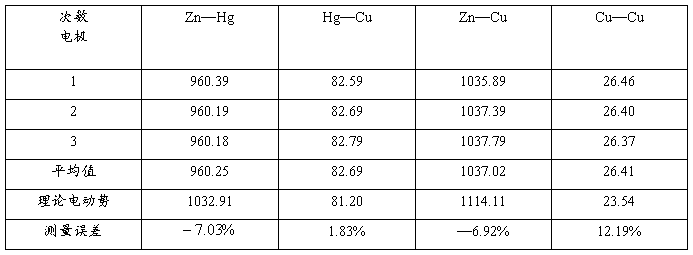
五、误差分析
在较长的电极电势测量过程中,工作回路中电流发生变化,导致测量误差
部分电解质溶液在测量过程中发生电解,浓度变化影响测量的结果
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
电导的测定及应用实验报告
实验名称一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
001520015000148YAxisTitle00146001440014200140XAxisTitle根据截距即为得154…
-
电导的测定及应用实验报告
实验名称一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
物化实验报告5-电导的测定及其应用
一实验目的1测量KCl水溶液的电导率求它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电导率仪的使…
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
大学物理化学实验报告-电导法测定水溶性表面活性剂的临界胶束浓度
物理化学实验报告院系化学化工学院班级学号姓名实验名称电导法测定水溶性表面活性剂的临界胶束浓度日期同组者姓名室温25气压1011kP…