实验四、药用硼砂含量的测定
实验四、药用硼砂含量的测定
一、实验目的
1.了解基准物质碳酸钠和硼砂的分子式和化学性质
2.掌握HCl标准溶液的配制、标定过程
3.掌握强酸滴定二元弱碱的滴定过程、突跃范围及指示剂的选择
4.掌握定量转移操作的基本要点
二、实验原理
1.硼砂的测定
Na2B4O7·10H2O(Mr381.37)是一个强碱弱酸盐,其滴定产物硼酸是一很弱的酸(K =7.3×10-10)。并不干扰盐酸标准溶液对硼砂的测定。在计量点前,酸度很弱,计量点后,盐酸稍过量时溶液pH值急剧下降,形成突跃。反应式如下:
Na2B4O7 + 2HCl + 5H2O → 2NaCl + 4H3BO3
计量点时pH=5.1,可选用甲基红为指示剂。按下式计算硼砂的质量分数。

ms为试样质量。
2. 0.1 mol·L-1 HCl溶液的标定
基准物质:无水Na2CO3或硼砂(Na2B4O7.10H2O)
①用无水Na2CO3标定:2HCl + Na2CO3 = 2NaCl + CO2 ↑+ H2O
指示剂:甲基橙;终点:黄色→橙色
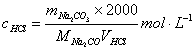

②用硼砂标定:Na2B4O7 + 5H2O + 2 HCl = 4H3BO3 + 2 NaCl
H3BO3 :Ka=5.8×10-10;
化学计量点时,溶液呈弱酸性(pH≈5.1),可选用甲基红作指示剂

三、主要试剂和仪器
0.1 mol·L-1 HCI溶液;无水Na2CO3基准物质,180℃干燥2~3h,置于干燥器中备用;0.2%甲基红指示剂(60%乙醇溶液);0.1%甲基橙指示剂;硼砂,置于含有NaCI和蔗糖的饱和液的干燥器内保存。
四、操作步骤
1. 0.1 mol·L-1 HCI溶液的配制和标定
(1)0.1 mol·L-1 HCI溶液的配制
配制0.1 mol·L-1 HCI溶液500mL(配制方法同实验二)
(2)0.1 mol·L-1 HCI溶液的标定(硼砂做基准物质)
用差减法准确称取0.4~0.6 克硼砂三份,分别放在250ml锥形瓶内,加水50毫升,微热溶解,冷却后,加2滴甲基红指示剂,然后用盐酸溶液滴定至溶液由黄色变为浅红色,即为终点,由硼砂的质量及实际消耗的盐酸体积,计算HCI溶液的浓度和测定结果的相对偏差。
(3)药用硼砂中硼砂含量的测定
准确称取药用硼砂0.5g(精确至小数点后4位),加50mL蒸馏水使溶解,加2滴甲基红指示剂,用0.1 mol·L-1HCl标准溶液滴定至溶液由黄变为橙色,平行三次,计算药用硼砂中硼砂的含量。
五、实验数据记录表格
表1 0.1 mol·L-1 HCl溶液的标定

表2 药用硼砂中硼砂含量的测定

六、思考题
1.用无水碳酸钠和硼砂标定盐酸标准溶液的操作方法有何不同,为什么?
第二篇:锡的测定
锌粉—氢氧化钠分解碘量法
原理:试样分解后,锡转化为金属锡、锌锡合金及其他可溶锡化合物。用盐酸溶解,以还原铁粉及铝片还原少量Sn(Ⅳ)成Sn(Ⅱ),最后以淀粉为指示剂,用碘酸钾标准溶液滴定完成测定。
硫化氢耗碘使结果偏高。焙烧过程硫被除去大部分,还原过程中产生的硫化氢,利用二氧化碳气流排除。砷在焙烧和分解过程中几乎除完,余下少量砷不干扰测定。锑含量不高时,经焙烧和分解排除后几乎不干扰测定。若含量高时,的按铍载—过氧化钠熔融碘量法处理。含钨较高的试样需按锌粉—硼砂—硼酸分解碘量法处理。
测定范围:大于0.1%锡的矿石。
试剂配制
盐酸 工业纯[不含锡,配成相当于市售AR浓盐酸(1+1)]
淀粉溶液3% 3g淀粉,溶于100mL沸水,冷却,加碳酸钠0.5g,碘化钾20g,摇匀备用。
锡标准溶液 称取纯金属锡(1.0000÷锡标准中锡的含量,置于250mL,加盐酸50mL盖表面,待锡溶解完全(必要时可稍加热)后,再加盐酸150mL移入1000mL容量瓶中,冷却至室温,以水稀释至刻度,摇匀备用,此溶液1mL=1.0000mgSn。
碘酸钾标准溶液(甲) 17.9g碘酸钾溶于含有3g氢氧化钾的500mL水中,加碘化钾89.5g。溶解完全后,水稀释至于10升。 滴定度的允许差为0.00001g/mL。
碘酸钾标准溶液(乙) 碘酸钾3g,溶于含有氢氧化钾2g的300mL毫升水中,加碘化钾11.7g,搅拌至溶解完全,以水稀释至10L。
标定 量取锡标准溶液20.00mL(相当于Sn=0.0200g)于300mL锥形瓶中,加工业盐酸100mL,加还原铁1g,以下按试样分析步骤进行还原、滴定,同时做空白试验。
分析步骤
试样0.2000g,置于5mL刚玉坩埚中,送入预先升温至500℃的马弗炉中,焙烧15min,取出冷却,加锌粉2g,用玻棒搅匀,用毛刷扫净玻棒,加氢氧化钠0.6~1g,加锌粉盖面(约1g),再加入氯化钠2g覆盖表面,送入750℃,的马弗炉中分解15min,取出冷却,放入预先装有盐酸(1+1)120mL,还原铁粉1g的300mL锥形瓶中。联接还原装置,加热至结块和铁粉溶解完全,取下冷却,加入铝片1g,在不断摇动下进行还原,待激烈作用停止后,移至电炉上加热至出现大气泡,置水槽冷却至室温,同时通以二氧化碳。取下,加入一颗小方解石,加淀粉指示剂2mL,以碘酸钾标准溶液滴定至浅蓝紫色为终点。同时做空白试验。
备注
①含锑在1%以上的试样需经分离,步骤按铍载—过氧化钠分解碘量法处理。
含钨在1~20%之间,其他干扰元素甚微时,可采用锌粉—硼砂—硼酸分解碘量法处理。步骤:将焙烧后的试样放入装有工业盐酸60mL的250mL烧杯中,加热浸出至出现大气泡,用工业盐酸洗净坩埚,以1%高锰酸钾溶液逐滴加入,直至溶液呈现黄色,搅拌1min,加热至微沸,保温10min,取下稍冷,用中速定性滤纸过滤,用工业盐酸洗三次烧杯,洗滤纸和深沉5~6次,滤液用300mL锥形瓶承接(控制总体积在120mL左右),然后加还原铁粉1g,加10%碘化钾溶液两滴,联接还原装置,加热使铁粉熔解,(若出现钨兰,则加磷酸10~15mL),加铝片1~1.5g还原。以下按分析步骤操作。
②若试样含锡较高时,采用碘酸钾标准溶液甲进行滴定,其淀粉指示剂可采用不加碘化钾的淀粉溶液5mL。若试样含锡较低(一般小于1%),采用碘酸钾标准溶液乙进行滴定,其淀粉指示剂采用本节配制的溶液2mL,以使待滴溶液中含有一定的碘化钾,提高终点灵敏度。
-
熏肉制品中亚硝酸盐含量的测定实验报告
熏肉制品中亚硝酸盐含量的测定华南师范大学09化一摘要肉制品是一类深受人民群众喜爱的食品在其生产过程中多采用亚硝酸盐作为发色剂它不仅…
-
实验报告 午餐肉中亚硝酸盐含量的测定
实验报告午餐肉中亚硝酸盐含量的测定一实验内容用盐酸萘乙二胺法测定午餐肉中亚硝酸盐的含量二实验目的与要求1熟悉掌握样品制备提取的基本…
-
实验三 药用硼砂的含量测定
实验三:药用硼砂的含量测定实验者:药学101李**合作者:倪**一、实验目的1掌握甲基红指示剂的滴定终点的判定。2巩固酸碱滴定中盐…
-
实验六 药用硼砂含量的测定
实验六药用硼砂含量的测定一实验目的1掌握药用硼砂含量的测定方法和原理的方法2掌握酸式滴定管的滴定操作和甲基红指示终点的判断二实验原…
-
化学实验报告 实验__硼砂的含量测定
实验报告姓名班级同组人自评成绩项目硼砂的含量测定课程学号一实验目的1掌握用酸碱滴定法直接测定硼砂含量的方法2掌握甲基红指示剂滴定终…