丙 烯 酰 胺 的 水 溶 液 聚 合-思考题
丙烯酰胺的水溶液聚合
一、 实验目的:
1、 掌握溶液聚合的方法及原理;
2、 学习如何正确的选择溶剂。
二、 实验原理:
与本体聚合相比,溶液聚合体系具有粘度低、搅拌和传热比较容易,不易产生局部过热、聚合反应容易控制等优点,但由于溶剂的引入,溶剂的回收和提纯使聚合过程复杂化;只有在直接使用聚合物溶液的场合,如涂料、胶粘剂、浸渍剂、合成纤维纺丝液等,使用溶液聚合才最有利。
进行溶液聚合时,由于溶液并非完全是惰性的,对反应要产生各种影响,选择溶剂时要注意其对引发剂分解的影响、链转移作用、对聚合物的溶解性能的影响,丙烯酰胺为水溶性单体,其聚合物也溶于水,在本实验采用水为溶剂进行溶液聚合,与有机物作溶剂的溶液聚合相比,只有廉价、无毒、链转移常数小、对单体和聚合物的溶解性能好的优点,聚丙烯酰胺是一种优良的絮凝剂、水溶性好,广泛应用于石油开采、选矿、化学工业及 污水处理等方面。
过硫酸铵是一种白色晶体,常作强氧化剂使用,也可以作单体聚合引发剂。它几乎不吸潮,由于能达很高的纯度而具有特别好的稳定性,便于储存。另外,它还具有使用方便、安全等优点。
三、 实验仪器和试剂:
三口瓶、球形冷凝管、温度计、丙烯酰胺(5g)、甲醇(25ml)、过硫酸铵(0.05g)
四、注意事项:
1、使用水浴锅时,水浴锅的外壳不能碰到谁,防止短路,破坏仪器;水浴锅底部不可与三口瓶接触;
2、甲醇为有毒的易挥发液体,在使用时注意尽量避免吸入鼻子中,使用后要进行回收处理。
3、沉淀剂的选择符合:①沉淀剂与聚合物完全不溶;②沉淀剂与溶剂要完全互溶;③沉淀剂一般为溶剂的4~5倍。
五、实验步骤、现象及其解释
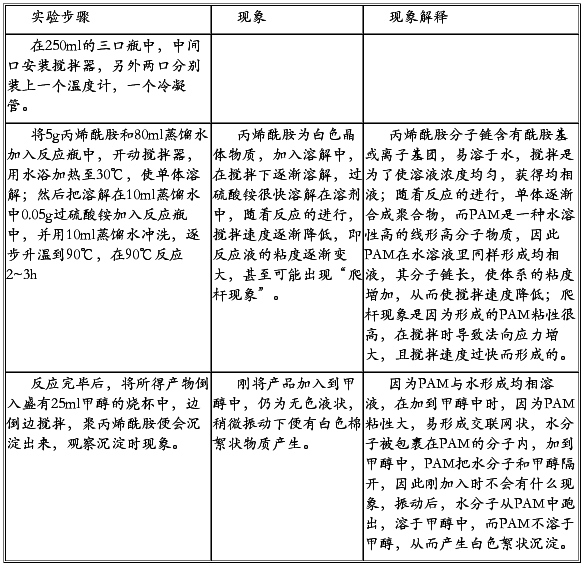
六、实验产品: 在三颈瓶中为无色均相溶液,滴加到25ml甲醇中,振动,得到棉絮状白色物质。
七、实验讨论与分析:在本次实验中,因不需要得到最终产品,因此对实验中各个因素对最终产率影响无法考究;因此在这只讨论可能对实验造成影响的因素:
1、溶剂:本实验选用水作为溶剂,水的极性很强,可能会与链自由基发生链转移,形成稳定自由基,就不能再引发单体聚合,从而使聚合物分子量降低;
2、温度的控制:升高温度将加速引发剂分解,从而提高聚合速率,但溶解单体时温度过高时丙烯酰胺会释放出强烈的腐蚀性气体和氮的氧化物类化合物,从而使单体浓度降低,使反应速率降低;在反应时温度过高,因引发剂为过氧化物具有强氧化性,氧化单体,从而使单体浓度降低,使反应速率降低;
3、引发剂的量:引发剂加入的浓度较多时,会引入更多的活性中心,反应速率增加,但得到的聚合物的分子量降低;且过硫酸铵是强氧化剂,在反应时可能会氧化单体,而使单体浓度降低,反应速率降低,引发剂自身也可能发生诱导分解,而使引发剂的量无故损耗;
4、单体浓度:在单体浓度较低的时候,聚合物分子量随着单体浓度增大而增大,但单体的浓度过大时,反应速率很快,反应产生热不能及时扩散,从而使局部温度较高,产生的聚合物自由基碰撞机率增加,加快反应的终止速率,可能使得到聚合物分子量较低。
实验改进:在实验步骤二时,可将少量水、引发剂、少量单体先溶解在烧杯中,然后将混合的均相溶液加入到反应液中反应。原因:在烧杯中形成的均相溶液,此时引发剂相对浓度较大,引发单体聚合形成较短聚合物,在将该溶液加入到反应液中后,在反应液中,一部分单体在引发剂引发下进行聚合,部分单体可直接与形成的低聚物链聚合(基本上可直接进入到链增长阶段),减短反应时间。
八、实验问题:
1、溶解丙烯酰胺时为何温度为30℃,温度过高会如何?
解:温度选择在30℃时,比较接近室温,而丙烯酰胺单体在室温很稳定,此时丙烯酰胺比较稳定的溶于水中,在温度过高时,丙烯酰胺会释放出强烈的腐蚀性气体和氮的氧化物类化合物;使单体浓度降低,而使反应速率降低,因接着往溶液中加入引发剂:过硫酸铵,其具有强氧化性,在高温时易将丙烯酰胺氧化,从而产生较多副产物;在反应时,温度较低时,聚合反应不完全,根据自由基聚合规律,温度升高有助于分子量的增大。当温度升高到一定程度后,若继续升温,自由基之间的碰撞机会增加,会使链终止速率比链增长反应速率增长更快,聚合产物分子量降低,且而温度过高时,引发剂分解加快,引发活性中心增多,反应时的聚合速率迅速增大,从而使反应不易控制,导致实验失败。
2、 在聚合反应时要反应2~3h,其中反应时间的控制是提高分子量还是转化率?
解:在聚合反应中,决定反应速率是反生在链引发中,引发剂的分解。引发剂的分解速率比较低,而引发剂产生的活性中心在接下来的链增长中聚合物的分子形成速度很快,在很短的时间内便会完成链的增长,因此对整个体系中,在较短的时间,引发剂分解产生的活性中心不可能使所有的单体均转化为聚合物,因而单体的转化率是随着反应时间的延长而增大的,表现在体系的平均分子量随着时间的增长而增大,但达到一定数值后,其分子量数值不再增加。因此反应时间的控制在前期既是提高转化率也是提高分子量,当分子量达到一定值时,反应时间的控制是在提高转化率。
3、实验中引发剂为何选用水溶性的,能否换成油溶性的?
解:本实验为溶液聚合,其要求单体和引发剂均要溶于溶剂中,实验采用以水作为反应的溶剂,因此需要采用水溶性的引发剂:过硫酸铵,其可以完全溶解在水中,形成均相体系,而丙烯酰胺同样溶解在水中,三者形成均相溶液体系,发生溶液聚合。在此实验中不能使用油溶性引发剂,因油溶性引发剂不能很好的溶解在溶剂水中引发反应,在反应液中很容易出现引发剂相互聚集,形成局部引发剂量较多,不能很好的引发聚合。
4、溶液聚合中,产品怎么处理,原理是什么?
解:水溶液聚合时,因加入溶剂的原因,在其聚合完成时,得到的产品中含有较多的溶剂,因此在得到产品后,应除去聚合物中的残留溶剂,将得到的产品重新溶解在另外一种溶剂中(如甲醇),该溶剂不能溶解聚合物,但可以溶解聚合物内部的溶剂,且挥发性好,且不与聚合物发生反应,这样最后便得到比较纯净的产品,其原理是根据聚合物在不同溶剂中溶解度不同而实行。
第二篇:丙 烯 酰 胺 的 水 溶 液 聚 合
丙 烯 酰 胺 的 水 溶 液 聚 合
一、 实验目的:
1、 掌握溶液聚合的方法及原理;
2、 学习如何正确的选择溶剂。
二、 实验原理:
与本体聚合相比,溶液聚合体系具有粘度低、搅拌和传热比较容易,不易产生局部过热、聚合反应容易控制等优点,但由于溶剂的引入,溶剂的回收和提纯使聚合过程复杂化;只有在直接使用聚合物溶液的场合,如涂料、胶粘剂、浸渍剂、合成纤维纺丝液等,使用溶液聚合才最有利。
进行溶液聚合时,由于溶液并非完全是惰性的,对反应要产生各种影响,选择溶剂时要注意其对引发剂分解的影响、链转移作用、对聚合物的溶解性能的影响,丙烯酰胺为水溶性单体,其聚合物也溶于水,在本实验采用水为溶剂进行溶液聚合,与有机物作溶剂的溶液聚合相比,只有廉价、无毒、链转移常数小、对单体和聚合物的溶解性能好的优点,聚丙烯酰胺是一种优良的絮凝剂、水溶性好,广泛应用于石油开采、选矿、化学工业及 污水处理等方面。
过硫酸铵是一种白色晶体,常作强氧化剂使用,也可以作单体聚合引发剂。它几乎不吸潮,由于能达很高的纯度而具有特别好的稳定性,便于储存。另外,它还具有使用方便、安全等优点。
三、 实验仪器和试剂:
三口瓶、球形冷凝管、温度计、丙烯酰胺(5g)、甲醇(25ml)、过硫酸铵(0.05g)
四、注意事项:
1、使用水浴锅时,水浴锅的外壳不能碰到谁,防止短路,破坏仪器;水浴锅底部不可与三口瓶接触;
2、甲醇为有毒的易挥发液体,在使用时注意尽量避免吸入鼻子中,使用后要进行回收处理。
3、沉淀剂的选择符合:①沉淀剂与聚合物完全不溶;②沉淀剂与溶剂要完全互溶;③沉淀剂一般为溶剂的4~5倍。
五、实验步骤、现象及其解释
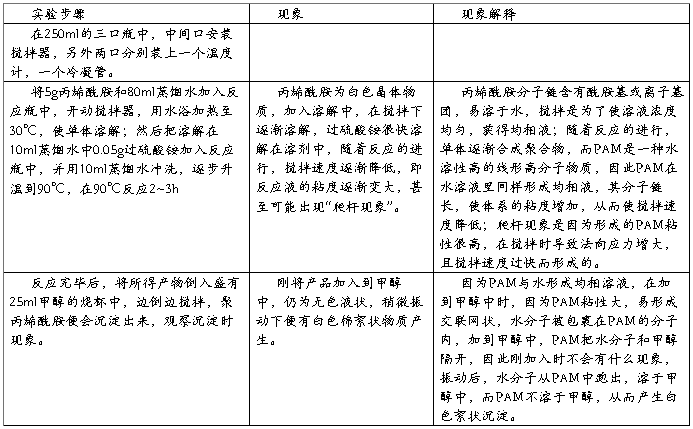
六、实验产品: 在三颈瓶中为无色均相溶液,滴加到25ml甲醇中,振动,得到棉絮状白色物质。
七、实验讨论与分析:在本次实验中,因不需要得到最终产品,因此对实验中各个因素对最终产率影响无法考究;因此在这只讨论可能对实验造成影响的因素:
1、溶剂:本实验选用水作为溶剂,水的极性很强,可能会与链自由基发生链转移,形成稳定自由基,就不能再引发单体聚合,从而使聚合物分子量降低;
2、温度的控制:升高温度将加速引发剂分解,从而提高聚合速率,但溶解单体时温度过高时丙烯酰胺会释放出强烈的腐蚀性气体和氮的氧化物类化合物,从而使单体浓度降低,使反应速率降低;在反应时温度过高,因引发剂为过氧化物具有强氧化性,氧化单体,从而使单体浓度降低,使反应速率降低;
3、引发剂的量:引发剂加入的浓度较多时,会引入更多的活性中心,反应速率增加,但得到的聚合物的分子量降低;且过硫酸铵是强氧化剂,在反应时可能会氧化单体,而使单体浓度降低,反应速率降低,引发剂自身也可能发生诱导分解,而使引发剂的量无故损耗;
4、单体浓度:在单体浓度较低的时候,聚合物分子量随着单体浓度增大而增大,但单体的浓度过大时,反应速率很快,反应产生热不能及时扩散,从而使局部温度较高,产生的聚合物自由基碰撞机率增加,加快反应的终止速率,可能使得到聚合物分子量较低。
实验改进:在实验步骤二时,可将少量水、引发剂、少量单体先溶解在烧杯中,然后将混合的均相溶液加入到反应液中反应。原因:在烧杯中形成的均相溶液,此时引发剂相对浓度较大,引发单体聚合形成较短聚合物,在将该溶液加入到反应液中后,在反应液中,一部分单体在引发剂引发下进行聚合,部分单体可直接与形成的低聚物链聚合(基本上可直接进入到链增长阶段),减短反应时间。
八、实验问题:
1、溶解丙烯酰胺时为何温度为30℃,温度过高会如何?
解:温度选择在30℃时,比较接近室温,而丙烯酰胺单体在室温很稳定,此时丙烯酰胺比较稳定的溶于水中,在温度过高时,丙烯酰胺会释放出强烈的腐蚀性气体和氮的氧化物类化合物;使单体浓度降低,而使反应速率降低,因接着往溶液中加入引发剂:过硫酸铵,其具有强氧化性,在高温时易将丙烯酰胺氧化,从而产生较多副产物;在反应时,温度较低时,聚合反应不完全,根据自由基聚合规律,温度升高有助于分子量的增大。当温度升高到一定程度后,若继续升温,自由基之间的碰撞机会增加,会使链终止速率比链增长反应速率增长更快,聚合产物分子量降低,且而温度过高时,引发剂分解加快,引发活性中心增多,反应时的聚合速率迅速增大,从而使反应不易控制,导致实验失败。
2、 在聚合反应时要反应2~3h,其中反应时间的控制是提高分子量还是转化率?
解:在聚合反应中,决定反应速率是反生在链引发中,引发剂的分解。引发剂的分解速率比较低,而引发剂产生的活性中心在接下来的链增长中聚合物的分子形成速度很快,在很短的时间内便会完成链的增长,因此对整个体系中,在较短的时间,引发剂分解产生的活性中心不可能使所有的单体均转化为聚合物,因而单体的转化率是随着反应时间的延长而增大的,表现在体系的平均分子量随着时间的增长而增大,但达到一定数值后,其分子量数值不再增加。因此反应时间的控制在前期既是提高转化率也是提高分子量,当分子量达到一定值时,反应时间的控制是在提高转化率。
3进行溶液聚合时,选择溶剂时应注意哪些问题?
解:在溶液聚合时根据溶液对聚合物的溶解性能与凝胶效应的影响分为良溶剂和沉淀剂,良溶剂在均相聚合中,如果单体的浓度不高,可能不会出现凝胶效应,而遵循自由基动力学规律,在沉淀聚合中,凝胶效应明显,从而发生自动加速效应,而导致实验失败;溶剂对聚合反应的影响:溶剂的加入降低了单体的浓度,使正反应进行的速率降低,使聚合物的分子量降低,溶剂也可能导致笼蔽效应使引发剂的效率降低,而且溶剂也可能与链自由基反生链转移反应等,因此在选择溶剂时,溶剂对凝胶效应的影响,避免或延长凝胶效应的时间,且要避免溶剂与引发剂、链自由基等作用。
4在加入引发剂进入溶液聚合中时,为什么选用滴加,?
解:在丙烯酰胺水溶液聚合时,引发剂过硫酸铵可以完全溶于水中,形成均相溶液,引发剂形成的溶液可以与单体形成的溶液形成均相,因为聚丙烯酰胺水溶性很好,在搅拌下形成均相的水溶液,而反应液在搅拌的作用下,滴加到反应液中,很容易使引发剂分散开来,不会出现引发剂在局部浓度过高的现象,从而减少引发剂分布不均匀而使水溶液只有局部反生溶液聚合反应,从而没有得到均相产品,所以在加入引发剂时用滴加而不要直接加入。
5在工业中,什么情况下采用溶液聚合?
解:在溶液聚合体系中,其在聚合时体系的粘度较低,搅拌和散热比较容易,反应温度容易控制,不易产生局部过热,溶液聚合多是直接以溶液的方式得到产品等,但是因为溶剂的引入,单体的浓度被稀释,聚合速率减慢,得到的最终产物分子量较低,且还要考虑加入的溶剂对引发剂、单体、聚合物等的影响,而且溶剂的回收和提纯使聚合过程复杂化,成本升高等,因此在直接使用溶液聚合时,只在使用涂料、浸渍剂、合成纤维纺丝液等。
6、实验中引发剂为何选用水溶性的,能否换成油溶性的?
解:本实验为溶液聚合,其要求单体和引发剂均要溶于溶剂中,实验采用以水作为反应的溶剂,因此需要采用水溶性的引发剂:过硫酸铵,其可以完全溶解在水中,形成均相体系,而丙烯酰胺同样溶解在水中,三者形成均相溶液体系,发生溶液聚合。在此实验中不能使用油溶性引发剂,因油溶性引发剂不能很好的溶解在溶剂水中引发反应,在反应液中很容易出现引发剂相互聚集,形成局部引发剂量较多,不能很好的引发聚合。
7、溶液聚合中,产品怎么处理,原理是什么?
解:水溶液聚合时,因加入溶剂的原因,在其聚合完成时,得到的产品中含有较多的溶剂,因此在得到产品后,应除去聚合物中的残留溶剂,将得到的产品重新溶解在另外一种溶剂中(如甲醇),该溶剂不能溶解聚合物,但可以溶解聚合物内部的溶剂,且挥发性好,且不与聚合物发生反应,这样最后便得到比较纯净的产品,其原理是根据聚合物在不同溶剂中溶解度不同而实行。
8、聚丙烯酰胺的用途?
解:聚丙烯酰胺为水溶性高分子聚合物,不溶于大多数有机物,其具有良好的絮凝性,降低液滴之间的摩擦阻力,广泛应用于石油开采、选矿、化学工业及污水处理等方面。在造纸过程中作为助流剂、补强剂;处理污水时作为助凝剂、絮凝剂、污泥脱水剂;石油钻采中作为降水剂;化学工业上主要应用于稳定胶体、粘结、成膜等方面
-
实验四 丙烯酰胺水溶液聚合
高实验四分子化学实验报告丙烯酰胺水溶液聚合丙烯酰胺水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂3掌握丙烯…
-
丙烯酰胺水溶液聚合
高分子化学实验报告09高分子1班实验四四丙烯酰胺水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验原理与…
-
实验四:丙烯酰胺水溶液的聚合
高分子实验四丙烯酰胺水溶液聚合化学实验报告一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验药品仪器及装置药品丙烯…
-
丙 烯 酰 胺 的 水 溶 液 聚 合-思考题
丙烯酰胺的水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验原理与本体聚合相比溶液聚合体系具有粘度低搅拌…
-
实验五_丙烯酰胺的水溶液聚合
实验五丙烯酰胺水溶液聚合一实验目的1掌握溶液聚合的方法和原理2学习如何选择溶液3掌握聚合物的处理方法二实验原理将单体溶于溶剂中而进…
-
实验报告2 SDS-聚丙烯酰胺凝胶电泳法
实验二SDS聚丙烯酰胺凝胶电泳法SDSPAGE测定蛋白质的分子量1原理11聚丙烯酰胺凝胶的性能及制备原理111性能聚丙烯酰胺凝胶的…
-
实验四 丙烯酰胺水溶液聚合
高实验四分子化学实验报告丙烯酰胺水溶液聚合丙烯酰胺水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂3掌握丙烯…
-
丙 烯 酰 胺 的 水 溶 液 聚 合
丙烯酰胺的水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验原理与本体聚合相比溶液聚合体系具有粘度低搅拌…
-
丙烯酰胺水溶液聚合
高分子化学实验报告09高分子1班实验四四丙烯酰胺水溶液聚合一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验原理与…
-
实验四:丙烯酰胺水溶液的聚合
高分子实验四丙烯酰胺水溶液聚合化学实验报告一实验目的1掌握溶液聚合的方法及原理2学习如何正确的选择溶剂二实验药品仪器及装置药品丙烯…