篇一 :医疗器械类安全风险分析报告
医疗器械类安全风险分析报告
医疗器械类安全风险分析报告
产品名称:(注册标准上的名称)
风险评价人员及背景:(项目组长、医学角度的大夫、技术角度的设计人员、应用角度的、市场角度的,并提供人员资格证明,如受过的培训资格、职称等级)
编 制: 日 期:
批 准: 日 期:
1. 编制依据
1.1 相关标准
1) YY0316-2003医疗器械——风险管理对医疗器械的应用
2) GB9706.1-1995医用电气设备 第一部分:通用安全要求;
3) IEC60601-1-4:1996医用电器设备——第徊糠郑和ㄓ冒踩蟆?:并行标准:医用可编程电气系统
4) 产品标准及其他
1.2 产品的有关资料
1)使用说明书
2)医院使用情况、维修记录、顾客投诉、意外事故记录等
3)专业文献中的文章和其他信息
2. 目的和适用范围
本文是对XXXX进行风险管理的报告,报告中对所有的可能危害以及每一个危害产生的原因进行了判定。对于每种危害可能产生损害的严重度和危害的发生概率进行了估计。在某一风险水平不可接受时,采取了降低见的控制措施,同时,对采取风险措施后的剩余风险进行了评价。最后,使所有的剩余风险的水平达到可以接受。
…… …… 余下全文
篇二 :医疗器械风险分析报告
安全风险分析报告
(依据YY0316-2003医疗器械——风险管理对医疗器械的应用)
单位名称:******医疗器械有限公司
产品名称: 医用纱棉块
申报日期: 20##年6月9日
风 险 分 析 报 告

1. 编制依据
相关标准
1) YY0316-2003医疗器械——风险管理对医疗器械的应用
2) 产品标准及其他
产品的有关资料
1) 使用说明书
2. 目的和适用范围
本文是对医用纱棉块产品进行风险管理的报告,报告中对所有的可能危害以及每一个危害产生的原因进行了判定。对于每种危害可能产生损害的严重度和危害的发生概率进行了估计。在某一风险水平不可接受时,采取了降低见的控制措施,同时,对采取风险措施后的剩余风险进行了评价。最后,使所有的剩余风险的水平达到可以接受。
…… …… 余下全文
篇三 :医疗器械产品风险分析报告范例
产品风险分析报告
广州市枫阳医疗器械有限公司
20##年6月
一、产品预期用途/预期目的和与安全性有关的特征的判定
按照《YY/T0316-2003 医疗器械 风险管理对医疗器械的应用》第4.2条的要求及附录A中有关医疗器械定性和定量特征的判定的提示清单,列出“一次性冲吸式无菌吸痰组合管”产品的所有可能影响其安全性的定性和定量特征的问题,并判定如下:
A.2.1 什么是预期用途/预期目的和怎样使用医疗器械?
——预期用途:该产品适用于医疗单位对临床病人口腔内痰液清理吸取和口腔清洁护理一次性用。
——怎样使用:由患者按照产品使用说明书在正常室内环境下由医护人员对患者使用。口腔过敏或行动不便的,医护人员使用时应进行相关培训。
A.2.2 医疗器械是否预期和患者或其他人员接触?
——是。治疗时理疗带与患者的病患区口腔粘膜接触。
A.2.3 在医疗器械中包含有何种材料和/或组分或与其共同使用、或与医疗器械接触?
——包含有下列材料:硅橡胶和PP材料以及ABS材料
A.2.4 是否有能量给予患者或从患者身上获取?
…… …… 余下全文
篇四 :医疗器械产品风险分析报告范例
××××理疗仪
产品风险分析报告
××××××有限公司
××××年×月
一、产品预期用途/预期目的和与安全性有关的特征的判定
按照《YY/T0316-2003 医疗器械 风险管理对医疗器械的应用》第4.2条的要求及附录A中有关医疗器械定性和定量特征的判定的提示清单,列出“××××理疗仪”产品的所有可能影响其安全性的定性和定量特征的问题,并判定如下:
A.2.1 什么是预期用途/预期目的和怎样使用医疗器械?
——预期用途:主要用于人体病患部位的急慢性扭挫伤、腰肌劳损、骨质增生、肩周炎等的康复治疗。
——怎样使用:由患者按照产品使用说明书在正常室内环境下自行使用。皮肤感觉差或行动不便的,使用时必须有医护人员或正常人员监护。
A.2.2 医疗器械是否预期和患者或其他人员接触?
——是。治疗时理疗带与患者的病患区表面皮肤接触,建议隔一件衣服为佳。
…… …… 余下全文
篇五 :医疗器械产品--安全风险分析报告
成人用品安全风险分析报告
1.总则
成人用品大多数都是体外用品,安全系数比较高,对一些体内服用产品,都是可以促进身体兴奋,所以不会对受检的患者或人员构成直接的风险。然而,在某些情况下,导致或促成错误的决定,可构成间接风险。另外,与使用有关的危害及其伴生风险也应给以考虑。本安全风险分析报告主要根据YY/T0316-2000《医疗器械一风险管理一第一部分风险分析的应用》要求中的附录A《用于判定医疗器械可能影响安全的特征问题》和附录B《体外诊断医疗器械风险分析指南》以及GB7826-87《系统可靠分析技术失效模式和效应分析(FMEA)程序》进行全面的安全风险分析。
2. 有关医疗器械定性和定量的判定
2.1 预期用途和目的
成人用品是一种体外诊断试剂,增加夫妻感情,促进人体新陈代谢,协调内分泌系统。
2.2 产品是否与患者或其他人员接触
成人用品为体外诊断试剂,与患者无接触,一般情况下也不与操作人员皮肤接触。
2.3 产品制造材料安全性
成人用品制造原料均为橡胶和高分子材料,均无毒性,因此在使用成人用品时应尽量失误吞服,不会风险。
2.4 是否有能量施加给患者或从患者身上获取
…… …… 余下全文
篇六 :医疗器械产品--安全风险分析报告
血清碱性磷酸酶测定试剂盒(ALP)安全风险分析报告
1. 总则
血清碱性磷酸酶测定试剂盒(以下简称ALP 测试盒)是一种临床检验体外诊断化学试剂中酶类试剂。因为检查并不在人体内或人体体表上进行,所以不会对受检的患者或人员构成直接的风险。然而,在某些情况下,由于体外诊断试剂有关的危害,导致或促成错误的决定,可构成间接风险。另外,与使用有关的危害及其伴生风险也应给以考虑。本安全风险分析报告主要根据YY/T0316-2000《医疗器械一风险管理一第一部分风险分析的应用》要求中的附录A《用于判定医疗器械可能影响安全的特征问题》和附录B《体外诊断医疗器械风险分析指南》以及GB7826-87《系统可靠分析技术失效模式和效应分析(FMEA)程序》进行全面的安全风险分析。
2. 有关医疗器械定性和定量的判定
2.1 预期用途和目的
ALP 测试盒是一种体外诊断试剂,是根据生物酶反应和光化学反应的原理,通过测定单位时间内吸光度的变化,实现对样品中ALP 的测定。ALP 测试盒预期用途为用于肝胆和骨骼系统疾病的诊断。
2.2 产品是否与患者或其他人员接触
ALP 测试盒为体外诊断试剂,与患者无接触,一般情况下也不与操作人员皮肤接触。
…… …… 余下全文
篇七 :医疗器械风险管理报告
医疗器械风险管理报告
(XXX型XX诊断仪)
文件编号:
批 准 人:
批准日期:
目 录
第一章 综述………………………………………………………………3
第二章 风险管理评审输入………………………………………………4
…… …… 余下全文
篇八 :医用手动病床安全风险分析报告
安全风险管理/分析报告

缩略词说明

用于判定可能影响安全性的医疗器械特征的问题
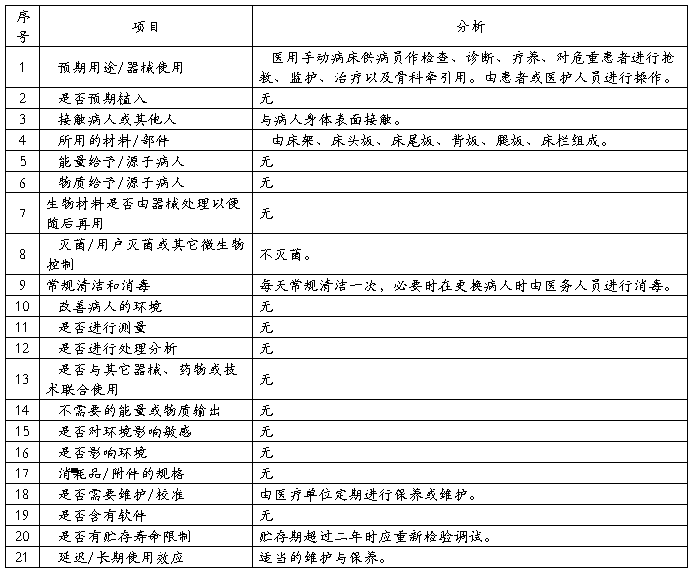
用于判定可能影响安全性的医疗器械特征的问题
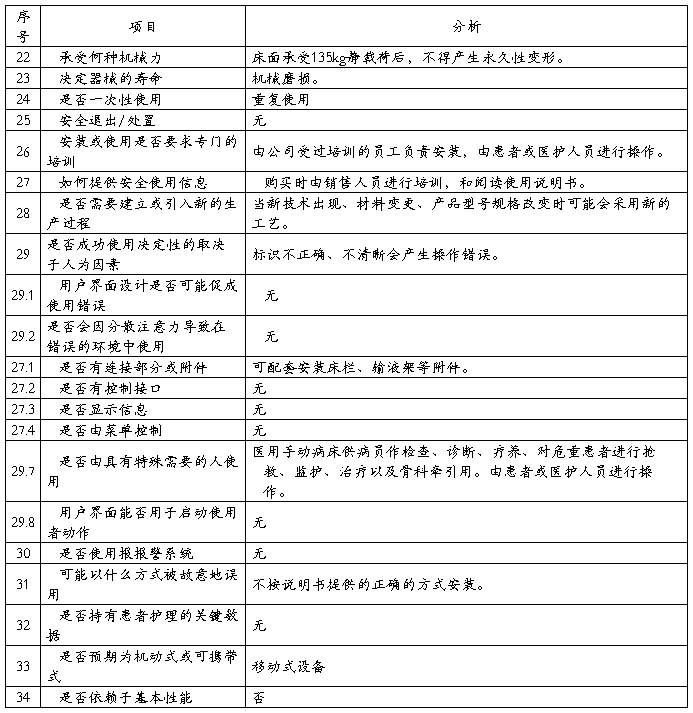
安全风险分析NO:01
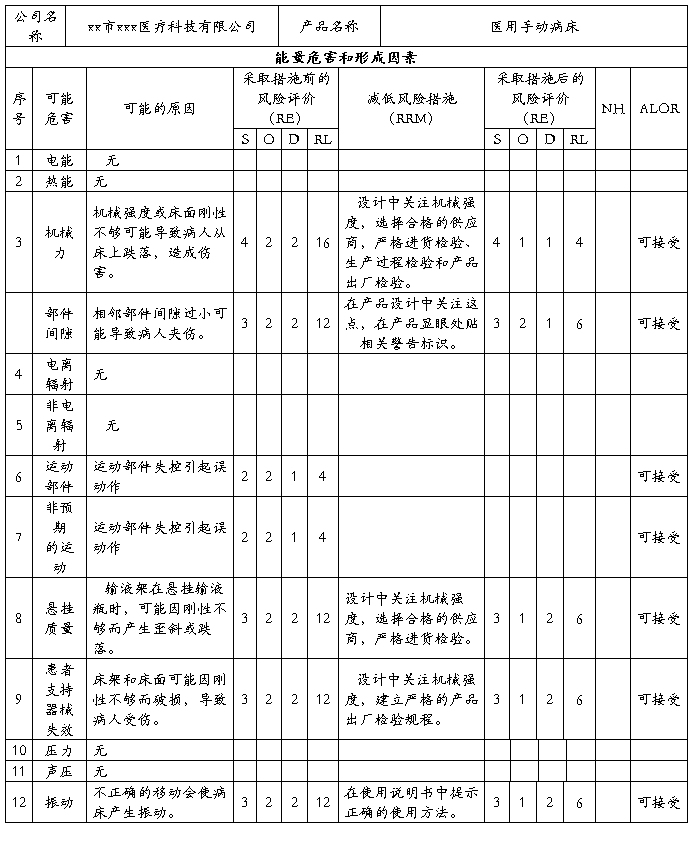
安全风险分析NO:02
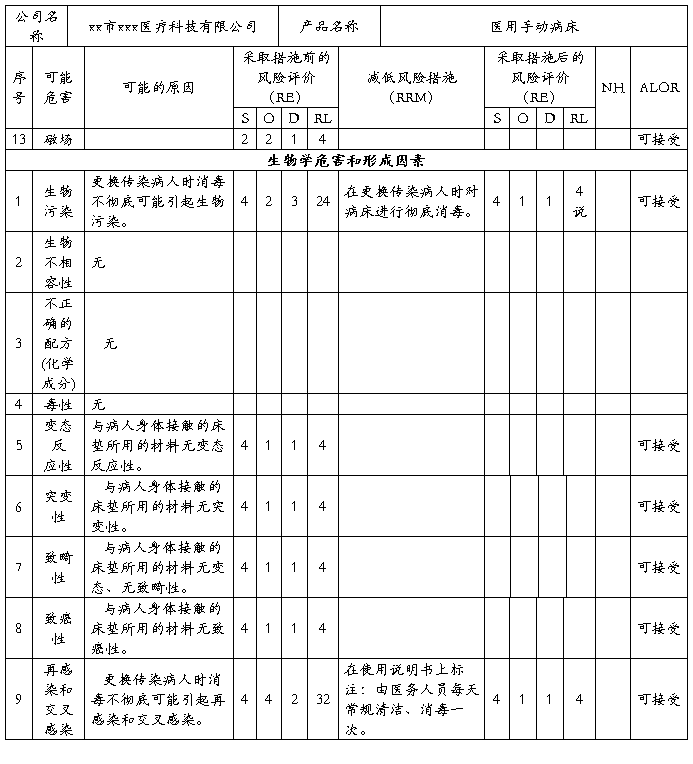
安全风险分析NO:03
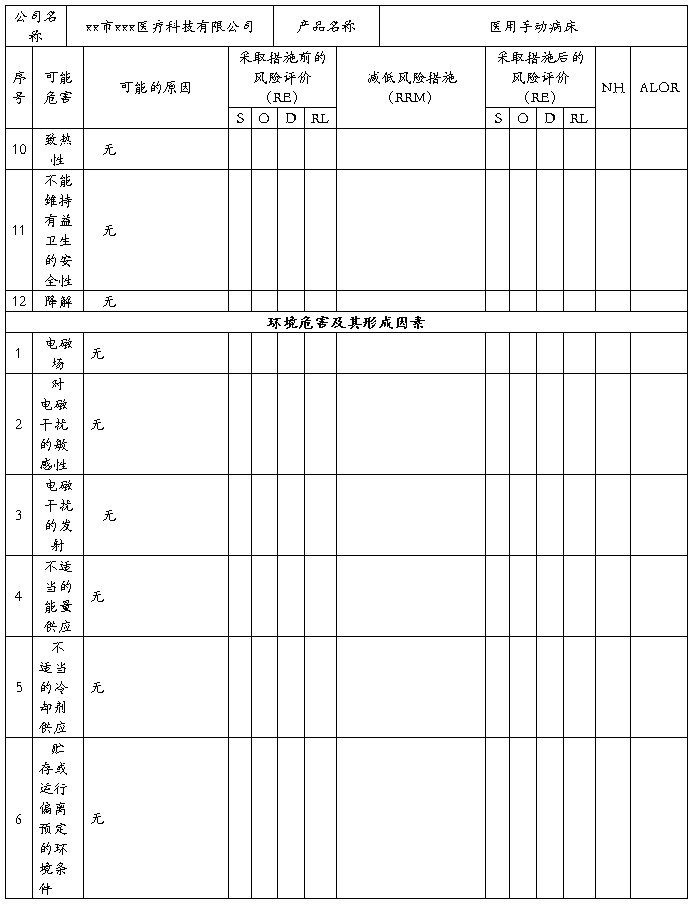
安全风险分析NO:04
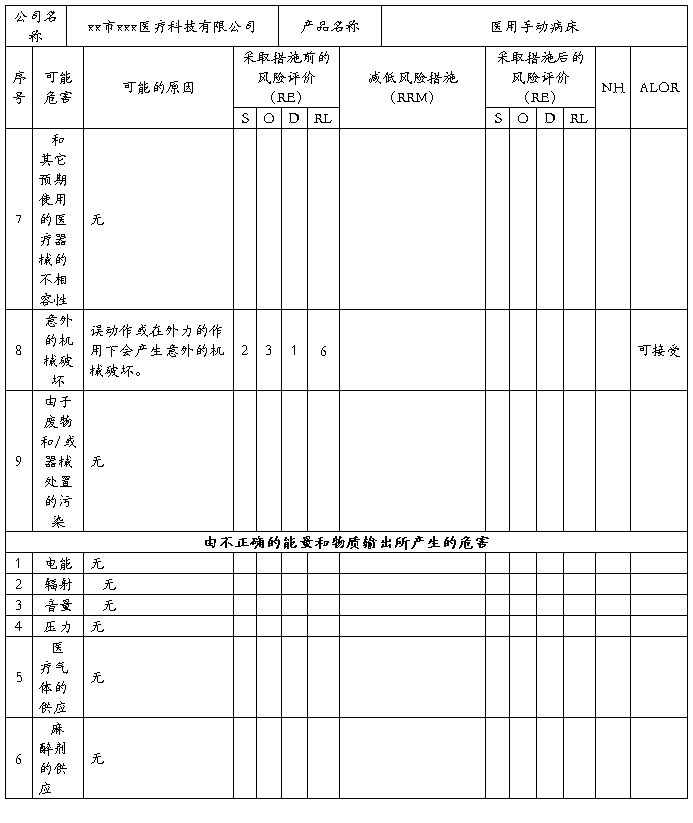
安全风险分析NO:05
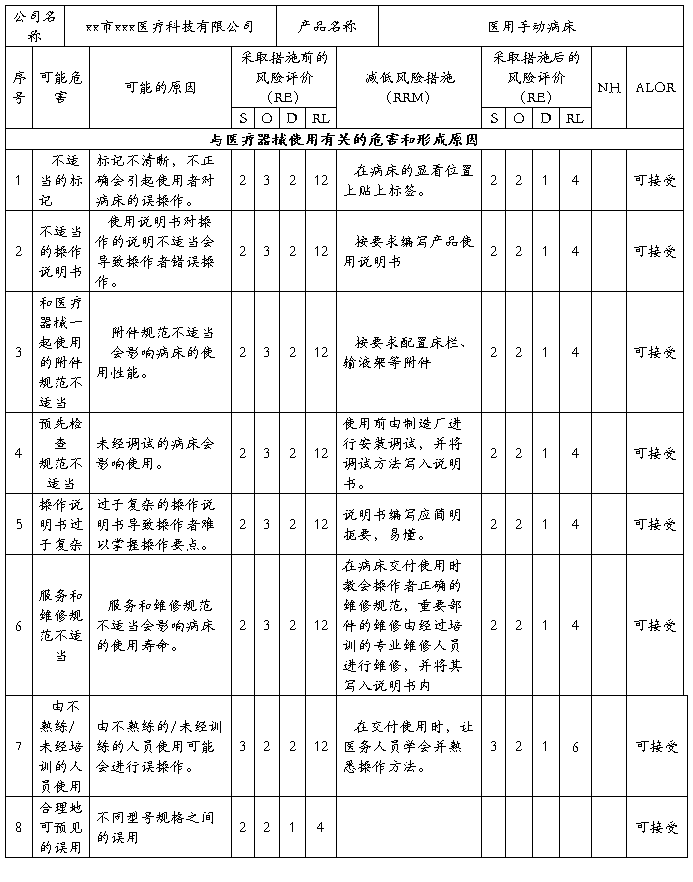
安全风险分析NO:06
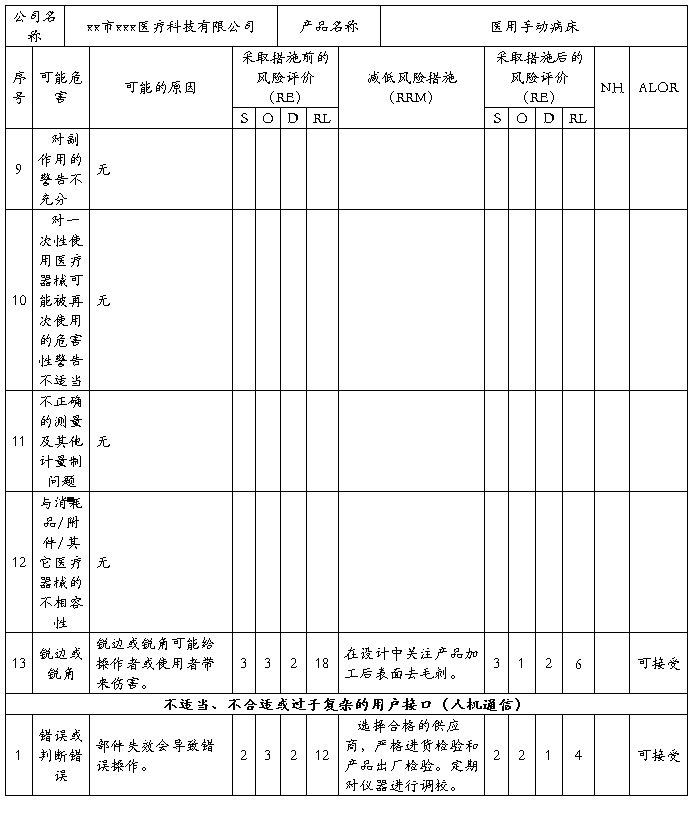
安全风险分析NO:07
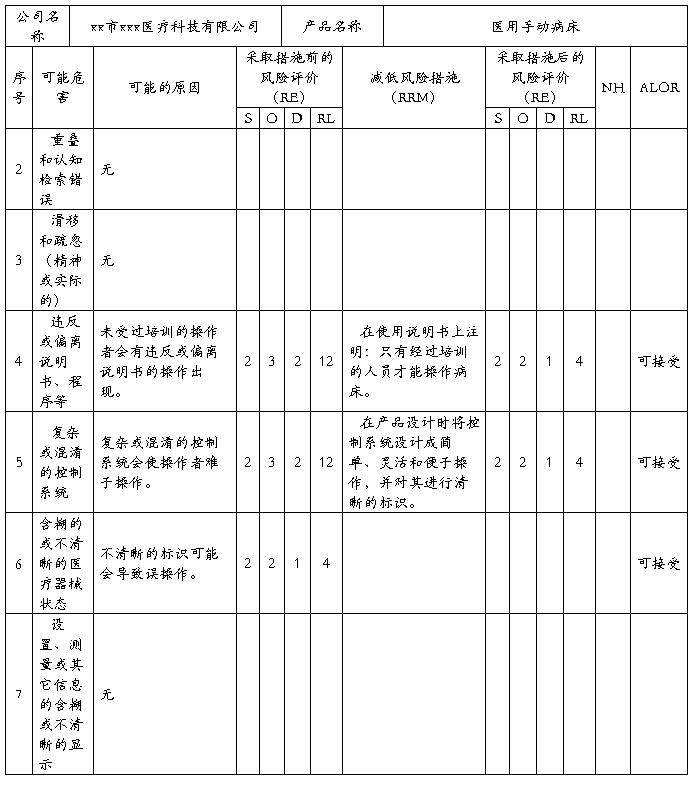
安全风险分析NO:08
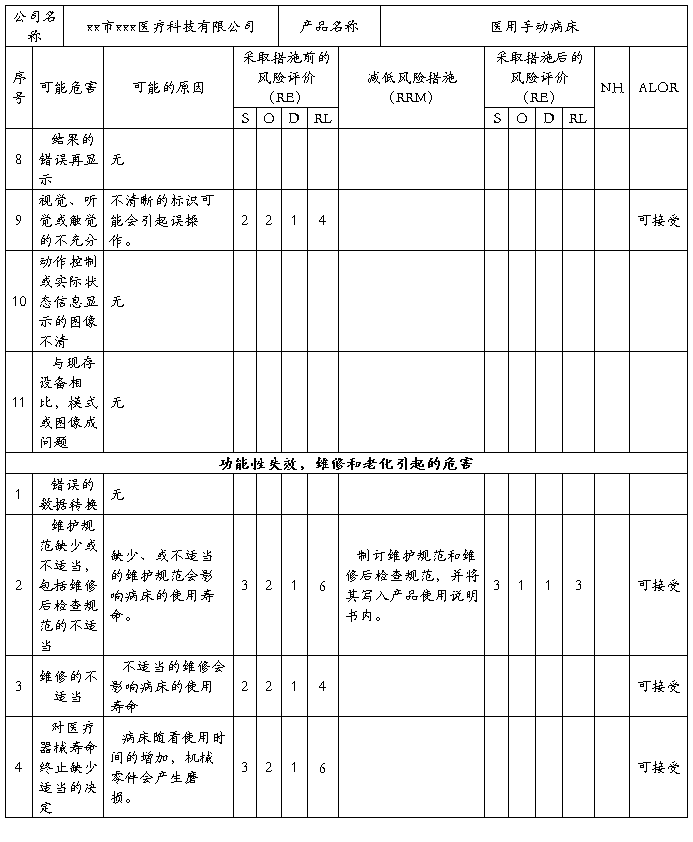
安全风险分析NO:09

…… …… 余下全文