篇一 :实验5 盐酸标准溶液的配制和标定
实验五 盐酸标准溶液的配制和标定
一、实验目的
1. 掌握减量法准确称取基准物的方法。
2. 掌握滴定操作并学会正确判断滴定终点的方法。
3. 学会配制和标定盐酸标准溶液的方法。
二、实验原理
由于浓盐酸容易挥发,不能用它们来直接配制具有准确浓度的标准溶液,因此,配制HCl标准溶液时,只能先配制成近似浓度的溶液,然后用基准物质标定它们的准确浓度,或者用另一已知准确浓度的标准溶液滴定该溶液,再根据它们的体积比计算该溶液的准确浓度。
标定HCl溶液的基准物质常用的是无水Na2CO3,其反应式如下:
Na2CO3 +2HCl=2NaCl+CO2 +H2O
滴定至反应完全时,溶液pH为3.89,通常选用溴甲酚绿-甲基红混合液或甲基橙作指示剂。
三、仪器及试剂
仪器:25ml酸式滴定管、烧杯、锥形瓶、玻璃棒、250ml容量瓶
试剂:浓盐酸(密度1.19)、无水Na2CO3、甲基橙或者溴甲酚绿-甲基红混合液指示剂:量取30mL溴甲酚绿乙醇溶液(2g/L),加入20mL甲基红乙醇溶液(1g/L),混匀。
四、实验内容
(一)0.1mol·L-1盐酸标准溶液的配制:
…… …… 余下全文
篇二 :盐酸标准溶液的配制与标定
盐酸标准溶液的配制与标定
一、【实验目的与要求】
1、掌握用无水碳酸钠作基准物质标定盐酸溶液的原理和方法。
2、正确判断甲基橙指示剂的滴定终点
二、【实验原理】
市售浓盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W,相对密度约为1.18。由于浓盐酸易挥发放出HCl气体,直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
标定盐酸的基准物质常用无水碳酸钠和硼砂等,本实验采用无水碳酸钠为基准物质,以甲基橙指示剂指示终点,终点颜色由黄色变为橙色。
用Na2CO3标定时反应为: 2HCl + Na2CO3 = 2NaCl + H2O + CO2↑
反应本身由于产生H2CO3会使滴定突跃不明显,致使指示剂颜色变化不够敏锐,因此,在接近滴定终点之前,最好把溶液加热煮沸,并摇动以赶走CO2,冷却后再滴定。
三、【仪器、材料与试剂】
1. 仪器和材料
2. 试剂
…… …… 余下全文
篇三 :盐酸标准溶液的配制与标定
一、考核目的
1. 学会直接法配制标准溶液的方法。
2. 学会盐酸溶液的标定方法。
3. 学会使用分析天平称取试样。
4. 练习容量瓶、移液管、滴定管的操作方法。
二、实验原理:
1. 用硼砂标定盐酸溶液的反应: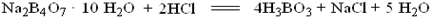
化学计量点时的pH=5.27, 可选甲基红作批示剂。
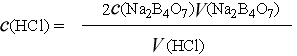
2. 硼砂标准溶液浓度计算: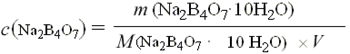
三、实验仪器及试剂:
仪器:万分之一分析天平,50ml酸碱滴定管各1支,20ml移液管1支,10ml量筒1支,表面皿1个,250ml锥形瓶2只,250ml容量瓶2只,250ml烧杯,洗耳球1只,玻璃棒1根,移液管架1个,药匙1个,滴定台。
…… …… 余下全文
篇四 :盐酸和氢氧化钠标准溶液浓度的标定实验报告
盐酸和氢氧化钠标准溶液浓度的标定实验报告
一、实验目的
1.掌握NaOH标准溶液的标定方法。
2.了解基准物质邻苯二甲酸氢钾的性质及应用。
3.进一步学习碱式滴定管的使用。
4.掌握强碱滴定弱酸的滴定过程、指示剂选择和终点的确定方法。
二、实验原理
溶液的配制方法主要分直接法和间接法两种。
(1)直接法:准确称取一定质量的基准物质,溶解后定量转移到容量瓶中,稀释至一定体积,根据称取物质的质量和容量瓶的体积即可计算出该标准溶液准确浓度。
例:配制0.017 mol/L K2Cr2O7标准溶液250mL。准确称取K2Cr2O7 1.2-1.3gK2Cr2O7于100mL小烧杯,加适量水溶解后定量转入250mL容量瓶中,用水稀释至刻度,摇匀。计算其准确浓度。
可直接配制标准溶液的物质应具备的条件:
①必须具备有足够的纯度 一般使用基准试剂或优级纯;
②物质的组成应与化学式完全相等 应避免:结晶水丢失;吸湿性物质潮解; ③稳定——见光不分解,不氧化 重铬酸钾可直接配制其标准溶液。
…… …… 余下全文
篇五 :实验报告_酸碱标准溶液的配制和标定
实验一酸碱标准溶液的配制和标定
实验目的
1. 掌握标准溶液的配制方法。
2. 掌握滴定法定量测定溶液浓度的原理,熟悉滴定管、移液管的准备、使用及滴定操作。
3. 熟悉甲基橙和酚酞指示剂的使用和终点的确定。
实验原理
酸碱滴定法是化学定量分析中最基本的分析方法。一般能与酸或碱直接(或间接)发生酸碱反应的物质大多可用酸碱滴定法测定他们的浓度。
按酸碱反应方程式中的化学计量系数之比,酸与碱完全中和时的pH值称为化学计量点,达到化学计量点时,应满足如下基本关系:
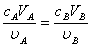
式中,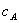 、
、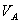 、
、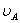 分别为酸的“物质的量”浓度、体积、化学计量系数;
分别为酸的“物质的量”浓度、体积、化学计量系数;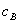 、
、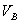 、
、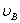 分别为碱的“物质的量”浓度、体积、化学计量系数。其中,酸、碱的化学计量系数由酸碱反应方程式决定。
分别为碱的“物质的量”浓度、体积、化学计量系数。其中,酸、碱的化学计量系数由酸碱反应方程式决定。
由于酸、碱的强弱程度不同,因此酸碱滴定的化学计量点不一定在pH=7处。通常,酸碱溶液为无色,酸碱中和是否完全,需用指示剂的变色来判断。指示剂往往是一些有机的弱酸或弱碱,它们在不同pH值条件下颜色不同。用作指示剂时,其变色点(在化学计量点附近)的pH值称为滴定终点。选用指示剂要注意:①变色点与化学计量点尽量一致;②颜色变化明显;③指示剂用量适当。
…… …… 余下全文
篇六 :盐酸标准溶液的配制与标定
盐酸标准溶液(0.1 mol·L-1)的配制与标定
一、原理
市售盐酸为无色透明的HCl水溶液,HCl含量为36%~38%(W/W)。由于浓盐酸易挥发出HCl气体,若直接配制准确度差,因此配制盐酸标准溶液时需用间接配制法。
采用无水碳酸钠为基准物质标定盐酸,以甲基红-溴甲酚绿混合指示剂指示终点。
用Na2CO3标定时反应为:2HCl + Na2CO3 → 2NaCl + H2O + CO2
执行标准:GB/T 601-2002 化学试剂标准滴定溶液的制备
二、实验用品
分析天平(感量0.1mg/分度),量筒,称量瓶,25mL酸式滴定管,250mL锥形瓶,工作基准试剂无水Na2CO3,浓HCl(浓或0.1mol/L),溴甲酚绿一甲基红指示液(变色点pH=5.1)。
三、实验步骤
(1)0.1mol.L-1盐酸溶液的配制:用小量筒取浓盐酸9ml,注入1000 ml,摇匀。
(2) 盐酸标准滴定溶液的标定
取在270~300℃干燥至恒重的基准无水碳酸钠约0.2g,精密称定3份,分别置于250ml锥形瓶中,加50ml蒸馏水溶解后,加甲基红-溴甲酚绿混合指示剂10滴,用盐酸溶液(0.1mol·L-1)滴定至溶液又由绿变暗红色,煮沸约2min。冷却至室温,继续滴定至暗红色,记下所消耗的标准溶液的体积, 同时做空白试验
…… …… 余下全文
篇七 :化学实验报告——盐酸溶液的标定
化学实验报告
(无机及分析化学)
题目:盐酸溶液的标定
学院班级: #####
姓名: ###
学号:###########
指导老师: #####
时间: ######
####年##月#日制
盐酸浓度的标定
一、实验目的
1. 练习酸碱标准溶液的标定方法。
2. 学习并掌握用酸碱滴定法测溶液浓度的方法。
3. 练习移液管、容量瓶的使用
二、实验原理
1.常用的标定NaOH溶液的基准物质是邻苯二甲酸氢钾(KHP),其结构式是: 。
。
标定时反应式:KHC8H4O4 + NaOOH = KNaC8H4O4 + H2O
2.用盐酸标定氢氧化钠,反应方程式:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
3.根据邻苯二甲酸氢钾的质量计算氢氧化钠的浓度,再根据氢氧化钠的浓度计算出盐酸的浓度。
三、实验步骤
1、0.1mol·L-1 NaOH溶液的标定
(1)检查、洗涤仪器
(2)称KHP 用差量法平行准确称量0.4—0.6 g KHP 三份,分别放入250ml的锥形瓶中(标号1、2、3)。
…… …… 余下全文
篇八 :盐酸溶液的配制与标定
实验五、盐酸溶液的配制与标定
一、实验目的
1、练习差减法称量;
2、学习酸式滴定管的使用
3、学习指示剂的原理和使用
4、学会盐酸配制和标定
二、实验原理
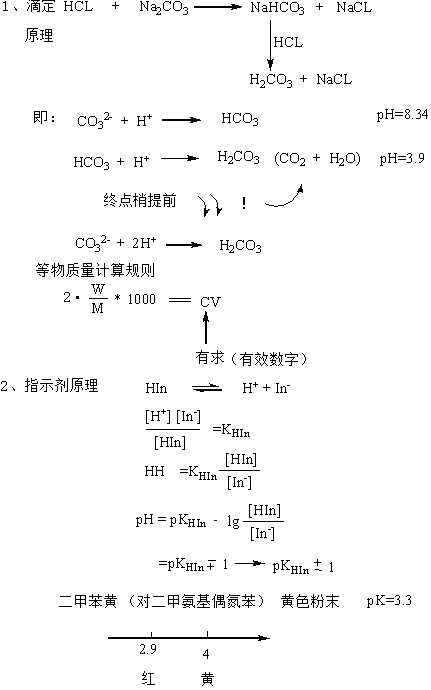

三、实验步骤
1、0.1mol/L盐酸溶液的配制
(1) 计算配制500ml0.1mol/L盐酸溶液所需浓盐酸的体积。
(2) 量取计算体积的浓盐酸,倒入盛有适量蒸馏水的试剂瓶中,加水稀释至500ml,摇匀。
2、盐酸溶液浓度的标定
(1) 差减法称取0.13—0.15g无水Na2CO3三份,称准至0.0001g。
(2) 加水50ml搅拌,使Na2CO3完全溶解。
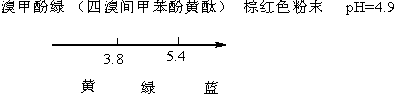
(3) 加入9滴溴甲酚绿-二早基黃混合指示剂,用已读好读数的滴定管慢慢滴入待测盐酸溶液,当溶液由绿色变为亮黃色即为终点。
四、实验记录
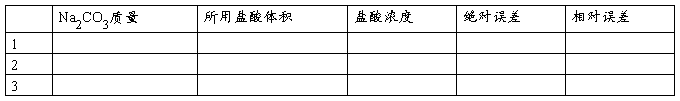
五、数据处理
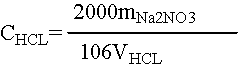
六、思考题
1、 滴定管内壁挂有液滴,可否对实验结果产生影响?
…… …… 余下全文