篇一 :实验四 醋酸解离常数的测定
实验四 醋酸解离常数的测定
(一) pH法
一. 实验目的
1. 学习溶液的配制方法及有关仪器的使用
2. 学习醋酸解离常数的测定方法
3. 学习酸度计的使用方法
二. 实验原理
醋酸(CH3COOH,简写为HAc)是一元弱酸,在水溶液中存在如下解离平衡:
HAc(aq) + H2O(l) D H3O+(aq) + Ac- (aq)
其解离常数的表达式为
[c (H3O+)/cθ][c(Ac-)/ cθ]
…… …… 余下全文
篇二 :无机化学实验六 醋酸电离度和电离常数的测定1
实验六 醋酸电离度和电离常数的测定—pH法
一、实验目的
1.测定醋酸的电离度和电离常数;
2.学习pH计的使用。
[教学重点]
醋酸的电离度、电离常数的测定
[教学难点]
pH计的使用
[实验用品]
仪器:滴定管、吸量管(5mL)、容量瓶(50 mL)、pH计、玻璃电极、甘汞电极
药品:0.200 mol·L-1HAc标准溶液、0.200 mol·L-1NaOH标准溶液、酚酞指示剂、标准缓冲溶液(pH=6.86、pH=4.00)
二、基本原理
HAc → H++ Ac-
C:HAc的起始浓度;[H+]、[Ac-]、[HAc]:分别为平衡浓度;
α:电离数;K:平衡常数
α =  × 100%
× 100%
Ka = 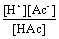 =
= 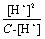
当α小于5时,C - [H+]≈C,所以Ka≈ 
根据以上关系,通过测定已知浓度HAc溶液的pH值,就可算出[H+],从而可以计算该HAc溶液的电离度和平衡常数。(pH=-lg[H+],[H+]=10-pH)
三、实验内容
1.HAc溶液浓度的测定(碱式滴定管)
以酚酞为指示剂,用已知浓度的NaOH溶液测定HAc的浓度。
…… …… 余下全文
篇四 :电导法测定乙酸电离平衡常数 实验报告
物理化学实验报告
姓名:何思思
班级:工艺五班
学号:10031010526
教师:李慎新
学院:材料化学与工程学院
电导法测定乙酸电离平衡常数
一、 实验目的
1、 掌握电导、电导率、摩尔电导率的概念以及他们之间的联系。
2、 掌握由电导法测定弱电解质电离平衡常熟的原理。
二、 实验原理
1、 电离平衡常数Kc的测定原理:
α=∧m/∧m∞
CH3COOH —→ CH3COO- + H
开始 C 0 0
平衡 C(1-α) Cα Cα
…… …… 余下全文
篇五 :四川理工实验报告电导法测定乙酸电离平衡常数 (2)
实验六 电导法测定乙酸电离平衡常数
报告人:曾辉 实验时间20##年03月07日
一.实验目的:
1.掌握电导、电导率、摩尔电导率的概念以及它们之间的相互关系。
3.掌握电导法测定弱电解质电离平衡常数的原理。
二.实验原理:
1.电离平衡常数Kc的测定原理
在弱电解质溶液中,只有已经电离的部分才能承担传递电量的任务。在无限稀释的溶液中可以认为弱电解质已全部电离,此时溶液的摩尔电导率为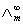 ,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率
,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率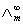 是有区别的,这由两个因素造成,一是电解质的不完全离解,二是离子间存在相互作用力。二者之间有如下近似关系:
是有区别的,这由两个因素造成,一是电解质的不完全离解,二是离子间存在相互作用力。二者之间有如下近似关系:
 (1)
(1)
…… …… 余下全文
篇六 :醋酸电离度和电离常数的测定
实验题目 醋酸电离度和电离常数的测定(教材p57-59)
一、实验目的
1、测定醋酸的电离度和电离常数;
2、掌握滴定原理,滴定操作及正确判断滴定终点;
3、练习使用pH计、滴定管、容量瓶的使用方法。
二、实验原理
醋酸(CH3COOH或写出HAc)是弱电解质,在溶液中存在下列电离平衡:
HAc  H+ + Ac-
H+ + Ac-
起始浓度/ mol·dm-3 c 0 0
…… …… 余下全文
篇七 :实验十四 醋酸电离度和电离常数的测定
实验十四 醋酸电离度和电离常数的测定
一、实验目的:标定醋酸溶液的浓度并测定不同浓度醋酸的pH值。计算电离平衡常数,加深对电离平衡常数的理解。学习使用酸度计。
二、另配仪器:三个50ml小烧杯、容量瓶三个、25mL移液管、和5mL吸管、酸度计(50ml小烧杯别放到自己抽屉),碱式滴管。
三、实验原理:
醋酸为弱电解质,在水溶液中存在如下电离平衡:

四、实验内容:
(1)醋酸溶液浓度的标定:
 标准NaOH溶液
标准NaOH溶液

 待测25.00mLHAc溶液
待测25.00mLHAc溶液
…… …… 余下全文
篇八 :醋酸电离常数和电离度的测定
实验三 醋酸电离常数和电离度的测定
一.实验目的
1.测定醋酸的电离常数,加深对电离度的理解;
2.学习正确使用pH计。
二.实验原理
醋酸(CH3COOH或简写成HAc)是弱电解质,在溶液中存在如下电离平衡:
HAc → H+ + Ac-
Ka = [H+][Ac-]/[HAc] α = [H+]/c
[H+]、[Ac-]和[HAc]分别为H+、Ac-、HAc的平衡浓度,Ka为电离常数,α为电离度
…… …… 余下全文