食品化学总结
第二章,水
水-溶质相互作用
一、 与离子和离子基团的相互作用(P15)
当食品中存在离子或可解离成离子或离子基团的盐类物质时,产生偶极-离子相互作用,可以固定相当数量的水。
随着离子种类及所带电荷的不同,与水之间的相互作用也有所差别。大致可以分作两类:
1、有助于水分子网状结构的形成,水溶液的流动性小于水,如:Li+、Na+、H3O+、Ca2+、Ba2+、Mg2+、Al3+、OH-等。
2、能阻碍水分子之间网状结构的形成,其溶液的流动性比水大,此类离子如:K+、Rb+、Cs+、NH4+、Cl-、Br-、I-、NO-3、BrO-3等;
二、水与具有氢键形成能力的中性基团(亲水性溶质)的相互作用
许多食品成分,如蛋白质、多糖(淀粉或纤维素)、果胶等中的极性基团,如羟基、羧基、氨基、羰基等,均可与水分子通过氢键相互结合。
水与溶质之间的氢键键合比水与离子之间的相互作用弱。
三、 水与非极性物质的相互作用
非极性的分子通常包括烃类、稀有气体、脂肪酸、氨基酸和蛋白质的非极性基团等。
疏水水合作用 疏水相互作用 疏水基团还能和水形成笼形水合物。
四、水与双亲分子的相互作用
双亲分子包括脂肪酸盐、蛋白脂质、糖脂、极性脂类和核酸。双亲分子在水中形成胶团。
食品中水的存在状态
根据食品中水分的存在状态,可以把食品中的水分作不同的类型(如下页图)。
 结合水,自由水(体相水)之间很难作截然的划分,其主要的区别在于:
结合水,自由水(体相水)之间很难作截然的划分,其主要的区别在于:
a.结合水的量与食品中所含极性物质的量有比较固定的关系。
b.结合水的蒸汽压比自由水低得多。
c.结合水不易结冰(冰点约-40℃)。
d.结合水不能作为溶质的溶剂。
e.体相水可被微生物所利用,结合水则不能。
(重点)水分活度和相对蒸汽压
水分活度:
定义:水分活度能反映水与各种非水成分缔结的强度。 aw=f/f0≈p/p0=%ERH/100
水分活度和温度的关系(结论)
温度对于水分活度的值有较大的影响,物理化学中的克劳修斯-克拉贝龙方程精确表示了水分活度与热力学温度(T)之间的关系:
a.由公式(可知, lnAw与1/T之间为直线关系。
b.但在较大的温度范围内, lnAw与1/T之间并非始终为直线关系;当冰开始形成时,lnAw与1/T图线中出现明显的折点。
c.冰点以上, Aw与试样成分和温度有关;冰点以下Aw与试样成分无关,只与温度有关。
水分吸着等温线(P24)
1、定义:在恒定温度下,食品水分含量(每单位质量干物质中水的质量)对Aw作图形成的曲线称为水分吸着等温线(MSI)。也叫吸湿等温线。
形状:大多数食品的吸湿等温线为S型,而水果、糖果和咖啡提取物等食品为J型。
2、分区:一般的MSI均可分为三个区,如图所示:
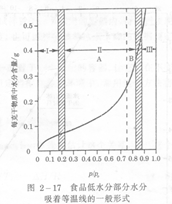 Ⅰ区:水与溶质结合得最牢固,是食品中最不容易移动的水。一般把Ⅰ区和Ⅱ区交界处的水分含量称为食品的“BET单层”水分含量,根据具体对象确定其单层值,对于食品的有效保存是非常重要的。
Ⅰ区:水与溶质结合得最牢固,是食品中最不容易移动的水。一般把Ⅰ区和Ⅱ区交界处的水分含量称为食品的“BET单层”水分含量,根据具体对象确定其单层值,对于食品的有效保存是非常重要的。
Ⅱ区:当食品中的水分含量相当于Ⅱ区和Ⅲ区的边界时,水将引起溶解过程,它还起了增塑剂的作用并且促使固体基质开始肿胀。溶解过程的开始将促使反应物质流动,因此加速了大多数的食品化学反应。
Ⅰ区和Ⅱ区的水通常占高水分食品原料中5%以下的水分。
Ⅲ区:自由水区,这部分水是食品中与非水物质结合最不牢固、最容易流动的水,也称为体相水。通常占高水分食品总水分的95%以上。食品中结合得最不牢固的那部分水对食品的稳定起着重要的作用。
3、水分吸着等温线与温度的关系:对同一食品,在任何指定的水分含量,食品的Aw随温度的提高而提高。
4、滞后现象
所谓滞后现象即向干燥的样品中添加水(回吸作用)后绘制的水分吸着等温线和由样品中取出一些水(解吸作用)绘制的水分吸着等温线并不完全重合,这种不重合性称为滞后现象
水分活度与食品化学变化的关系
以各类食品成分为线索,其化学变化与水分活度关系的一般规律如下:
a.淀粉:淀粉的食品学特性主要体现在老化和糊化上。在含水量大于30~60%时,淀粉的老化速度最快;降低含水量老化速度变慢;当含水量降至10~15%时,淀粉中的水主要为结合水,不会发生老化。
b.蛋白质及酶:据测定,当食品中的水分含量在2%以下时,可以有效的阻止蛋白质的变性;而当达到4%或其以上时,蛋白质变性变得越来越容易。
c.脂肪:影响脂肪品质的化学反应主要为氧化酸败。脂类的氧化反应与水分含量之间的关系为:在Ⅰ区,氧化反应的速度随着水分增加而降低;在Ⅱ区,氧化反应速度随着水分的增加而加快;在Ⅲ区,氧化反应速度随着水分增加又呈下降趋势。
d.褐变反应是影响食品质量和外观特性的重要的化学反应,包括酶促褐变和非酶褐变两类。当食品中的水分活度在0.25~0.30之间时,酶促褐变可被有效防止;但当水分活度在此基础上增加时,酶促反应就会明显发生。
当食品中的水分活度在0.6~0.7之间时,非酶褐变最为严重;水分活度下降,褐变速度减慢,在0.2以下时,褐变难以发生。但当水分活度超过褐变高峰要求的值时,其褐变速度又由于体系中溶质的减少而下降。
e.水溶性色素:一般而言,当食品中的水分活度增大时,水溶性色素分解的速度就会加快。
水分活度与微生物生命活动的关系
a.不同种类的微生物其正常生长繁殖所需要的水分活度不同,由此可以正确推断影响不同含水量食品质量的主要微生物;
b.表中每一个水分活度区间的下限为相应微生物正常生长的水分活度阈值,即在此水分活度以下,该类微生物不能正常生长。
c.不同种类的微生物其存活和生长与水分活度有关系,同一种类微生物在不同的生长阶段也要求不同的水分活度。一般讲,细菌形成芽孢时比繁殖时所需的水分活度要高;产毒微生物在产生毒素时所需的水分活度高于不产毒时所需的水分活度。
第三章,碳水化合物
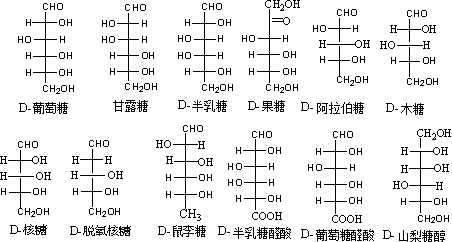 单糖的成糖结构
单糖的成糖结构
Maillard(美拉德)反应(重点)
Maillard (美拉德)反应指食品在油炸、焙烤、烘焙等加工或贮藏过程中,还原糖同游离氨基酸或蛋白质分子中氨基酸残基的游离氨基发生羰氨反应,这种反应被称为美拉德反应。
1、反应机理
(1)初期阶段:Maillard反应的初期阶段包括两个过程,即羰氨缩合与分子重排。
上步产物葡糖胺酸性条件下可以发生阿姆德瑞重排而转化为环式果糖胺
2)中期阶段:酮式果糖胺在中期阶段主要的分解过程可能有三个途径,这里仅介绍脱水转化成羟甲基糠醛(记住产物)的途径。
(3)末期阶段:前两个阶段得到的许多产物及中间产物进一步缩合、聚合形成复杂的高分子色素。
影响Mailard反应的因素
(1)底物结构:在糖类物质中:五碳糖(核糖>阿拉伯糖>木糖)>六碳糖(半乳糖>甘露糖>葡萄糖),醛糖>酮糖,单糖>二糖。
一般地,反应的活性:胺类>氨基酸;碱性氨基酸>中性或酸性氨基酸;氨基处于ε位或碳链末端的氨基酸>氨基处于α位的。而蛋白质的褐变速度则十分缓慢。
(2)反应物浓度Mailard反应速度与反应物浓度成正比;完全干燥的条件下难以发生,含水量在10~15%时容易发生;
(3)温度 Mailard反应是一个热反应,温度越高,反应时间越长,反应进行的程度越大。
(4)pH 碱性条件有利于Mailard反应的进行,而酸性环境,特别是pH3以下可以有效防止褐变反应的发生。
(5)金属离子 许多金属离子可以促进Mailard反应的发生,特别是铁离子与铜离子,三价铁比二价铁更为有效。
Mailard反应的抑制与促进
要抑制美拉德反应,可采用如下的方法:
(1)将水分含量降到很低;
(2)如果是流体食品则可通过稀释、降低PH、降低温度或除去一种作用物;
(3)亚硫酸盐或酸式亚硫酸盐可抑制美拉德反应;
(4)在食品加工的过程中避免混入铁和铜离子。
要促进美拉德反应则要采用与上面相反的条件。
焦糖化反应(和美拉德反应都属于非酶褐变)
糖类尤其是单糖类在没有含氨基化合物存在的情况下,加热到熔点以上时,会因发生脱水、降解等过程而发生褐变反应,这种反应称为焦糖化反应,又叫卡拉蜜尔作用。
低聚糖:环状低聚糖(看书)
环状低聚糖:它是由D-吡喃葡萄糖通过α-1,4糖苷键连接而成的环糊精,分别是由6-,7-,8-个糖单位组成,称为α-,β-,γ-环糊精。
多糖
由相同的糖组成的多糖称为均匀多糖。
由两种或多种不同的单糖组成的多糖称为非均匀多糖,或称杂多糖。
多糖溶液的黏度与稳定性(流动学性质)
高度支链的多糖分子比具有相同分子量的直链多糖分子溶液的黏度低;带电荷的多糖分子溶液的黏度大大增加。多糖溶液一般具有两类流动性质:一类是假塑性;一类是触变性。
直链淀粉与支链淀粉(结构上面的差别)
直链淀粉是D-吡喃葡萄糖通过α-1,4-糖苷键连接起来的链状分子。淀粉在水溶液中以螺旋、部分断开的螺旋或无规线团的形式存在的。
支链淀粉是D-葡萄糖通过α-1,4-糖苷键连接成一直链,此直链上又通过α-1,6-糖苷键形成侧链,在侧链上还有分支,支链的长度一般为20~30个葡萄糖基。
淀粉的糊化
糊化的概念:淀粉颗粒具有结晶区和非结晶区交替层的结构,通过加热提供足够的能量,破坏了结晶胶束区弱的氢键后,颗粒开始水合和吸水膨胀,结晶区消失,大部分直链淀粉溶解到溶液中,溶液粘度增加,淀粉颗粒破裂,双折射消失,这个过程称糊化。
具有胶束结构的生淀粉称为β-淀粉。处于糊化状态的淀粉称为α化淀粉。
糊化本质:淀粉粒中结晶区和非结晶区的淀粉分子间的氢键断开,分散在水中成为胶体溶液。
淀粉糊化可分为三个阶段
a.可逆吸水阶段:水分进入非结晶区,体积略有膨胀;
b.不可逆吸水阶段:随温度升高,水分进入淀粉微晶间隙,不可逆大量吸水,结晶“溶解”;
c.淀粉粒解体阶段,淀粉分子全部进入溶液。
淀粉糊化的影响因素:
1.淀粉种类与颗粒大小:小颗粒淀粉的结构较紧密,糊化较难;
2.温度:提高温度有利于糊化;
3.pH: pH4-7影响很小,高pH有利于淀粉的糊化;
4.水含量:糊化和水含量成正比;
5.糖:高浓度的糖可降低糊化速度;
6.脂肪:油脂可显著降低糊化速度和糊化率。
淀粉老化
老化的概念 :经过糊化的α-淀粉在室温或低于室温下放置后,会变得不透明甚至凝结而沉淀,这种现象称为老化(回生,凝沉)。
老化的本质:其本质是糊化的淀粉分子又自动排列成序,形成致密、高度晶化的不溶解性的淀粉分子微束。
影响淀粉老化的因素:
直链淀粉和支链淀粉的比例:直链淀粉比例高时易于老化 ;
温度:在2-4℃之间最易老化,60℃以上或-20℃以下不易老化;
水分含量:水分30%~60%时最易老化,而低于10%时不易老化。
pH:在偏酸( pH4以下)或偏碱的条件下也不易老化。
脂类:极性脂类如磷脂、硬脂酰乳酸钠、单甘酯等可以抗老化。
防止淀粉老化:可将糊化后的α-淀粉,在80℃以下的高温迅速除去水分(水分含量最好达10%以下)或冷至0 ℃以下脱水。这样淀粉成为固定的α-淀粉。 α-淀粉加水后,因无胶束结构,水易于浸入而将淀粉分子包蔽,不需加热,亦易糊化。
维生素(结构多糖)
黄原胶(微生物多糖,具有很好的粘胶特性)黄原胶的特性:(1)良好的增稠性,1%溶液粘度相当于100倍1%明胶溶液。 (2)较宽的pH范围(1~11)内稳定,粘度不变(耐酸碱),与高盐具有相容性。 (3)0~100℃内粘度基本不变。 (4)能稳定悬浮液和乳状液,具有良好的冷冻与解冻稳定性。 (5)具有高度假塑性,剪切变稀和粘度瞬时恢复的特性。 (6)与瓜尔豆胶、刺槐豆胶有协同作用。
由纤维素主链和三糖(2个甘露糖、1个葡萄糖醛酸)侧链构成。分子间可缔合成螺旋状,相互缠结成网状。
第四章,脂类
脂类物理性质(熔点和沸点)
天然油脂无固定的熔点和沸点,而只有一定的熔点范围和沸点范围。
油脂的熔点一般最高在40~55 ℃之间。酰基甘油中脂肪酸的碳链越长、饱和程度越高,熔点越高;反式结构的熔点高于顺式结构。油脂的沸点一般在180-200℃之间
结晶特性(重点)
同质多晶现象:指化学组成相同,但具有不同晶型的物质,熔化时可得到相同的液相的现象。
经X-射线衍射测定表明:固态脂的微观结构是高度有序的晶体结构。
油脂在固态的情况下有同质多晶现象。
油脂的晶型
三酰基甘油的晶胞有三种不同的堆积排列方式,形成三斜、正交以及六方晶系。可能形成的晶体形态:主要有β型、βˊ 型、和α型三种。
晶形 α β’ β
链堆积 六方 正 交 三 斜
稳定性 小 中 大
熔点 低 中 高
熔化:甘油三酯熔化时,β型晶体随温度增加,热焓增加,到达熔化温度时,吸热但温度不变,全部固体转化为液体后,温度继续上升。α型在E点开始转变成β型,此时放出热量。
油脂的塑性!!!
油脂的塑性是与油脂的加工和使用特性紧密相关的物理属性。
塑性是指固体脂肪在外力作用下,当外力超过分子间作用力时,开始流动,但当外力停止后,脂肪重新恢复原有稠度。
决定油脂塑性的因素:
(1)固体脂肪指数(SFI):在一定温度下脂肪中固体和液体所占份数的比值。
可以通过脂肪的熔化曲线来求出,SFI=ab/bc。只有SFI适当时,油脂才会有比较好的塑性。
(2) 熔化温度范围:熔化温度范围越宽的脂肪其塑性越好。
(3)脂肪的晶型 βˊ型比β型塑性好。
脂类氧化
自动氧化:油脂的自动氧化指油脂分子中的不饱和脂肪酸与空气中氧(基态氧)之间所发生的自由基类型的反应。
自动氧化的机理描述
引发剂
引发: RH-──→R· + ·H
传递: R· +O2--→ ROO·
ROO· + RH--→ ROOH+R·
终止: R· + R· --→R-R
R· + ROO· --→ROOR
ROO·+ ROO· --→ROOR + O2
游离基的引发通常活化能较高,所以最初游离基的产生,需引发剂的帮助。激发态氧(单线态氧,1O2)、过渡金属元素、热、光等均对此有密切影响。
链传递反应中的氧是能量较低的基态氧(三线态氧,3O2 )。链传递的活化能较低,故此步骤进行很快,并且可循环进行,产生大量氢过氧化物。H是与双键相邻的α-亚甲基氢原子。
光敏氧化
光敏氧化是在光的作用下(不需要引发剂)不饱和脂肪酸与单线态氧直接发生的氧化反应。
食品中如叶绿素、血红蛋白和一些合成色素等可以起光敏剂的作用,使三线态的氧变为活性较高的单线态氧。
光敏氧化的特点:
(1)不产生自由基 (2)双键的顺式构型改变成反式构型
(3)与氧浓度无关 (4)不存在诱导期;
(5)光敏氧化反应受到单线态氧猝灭剂β-胡萝卜素与生育酚的抑制。
(6)对于同样的反应底物,光敏反应的速度大于自动氧化(约1500倍)。
酶促氧化
脂肪在酶参与下发生的氧化反应,称为酶促氧化。
脂肪氧合酶专一性的催化具有1,4-顺,顺-戊二烯结构的多不饱和脂肪酸发生氧化反应。
影响食品中脂类氧化速率的因素
一)脂肪酸及甘油酯的组成:主要发生在不饱和脂肪酸上,饱和脂肪酸在室温下难以氧化,但在高温下会产生显著的氧化;不饱和脂肪酸中C=C数目增加,氧化速度加快;顺式构型比反式构型易氧化;共轭双键比非共轭双键氧化快。游离脂肪酸比甘油酯的氧化速率略高。
二)氧:当氧浓度较低时,氧化速率与氧浓度近似成正比;当氧浓度很高时,则氧化速率与氧浓度无关。单线态氧的氧化速率约为三线态氧的1500倍。
三)温度:一般来说,随着温度上升,氧化速率加快;但温度上升,氧的溶解度会有所下降。
四)表面积:一般来说,油脂与空气接触的表面积与油脂氧化速率成正比。
五)水分:当水分活度在0.3时,油脂的氧化反应速度最慢。随着水分活度的降低和升高,油脂氧化的速度均有所增加。
六)助氧化剂:一些具有合适的氧化还原电位的二价或多价过渡金属如Cu2+、Mn2+、Fe3+、Fe2+、Al3+、Pb2+等是有效的助氧化剂。血红素也是一种重要的助氧化剂。参与酶促氧化的酶均为氧化反应的催化剂
七)光和射线:光和射线不仅能促使氢过氧化物分解,还能引发自由基。
八)抗氧化剂:即能延缓和减慢油脂氧化速率的物质。这类物质可以通过不同方式发挥作用,有天然和人工合成两大类。
油脂的水解 油脂水解主要的特点是游离脂肪酸含量增加。这会导致油脂的氧化速度提高,加速变质;也能降低油脂的发烟点;使油脂的风味变差。
脂类氧化的评价方法
过氧化值(POV):指1kg油脂中所含氢过氧化物的毫摩尔数。用过氧化值评价油脂氧化的趋势多用于氧化的初期。
碘值:指100g油脂吸收碘的克数。
酸价(AV):中和1g油脂中游离脂肪酸所需的KOH的毫克数。酸价与油脂中游离脂肪酸的量成正比,反映了油脂品质的优劣,一般新鲜油脂的酸价较低
油脂的改性
1、油脂的氢化:油脂的氢化是指三酰基甘油中不饱和脂肪酸双键在催化剂如镍的作用下的加氢反应。氢化后的油脂,熔点提高,颜色变浅,稳定性提高。
2、酯交换
天然油脂中脂肪酸的分布模式,有时限制了他们在工业上的应用。通过酯交换可以改变甘油三酯中脂肪酸的分布,以适应特定需要。如增加油脂的稠度,并具有所期望的熔点和结晶性。酯交换可以在分子内进行,也可以在不同分子之间进行。酯交换一般以甲醇钠作催化剂,通常只需在50-70℃下,不太长的时间内就能完成。
第五章 蛋白质
简单蛋白的溶解度分类
简单蛋白质按溶解度可分为清蛋白、球蛋白、谷蛋白、醇溶谷蛋白、
1、清蛋白:溶于水及稀盐、稀酸或稀碱溶液,能被饱和硫酸铵所沉淀,加热可凝固。
2、球蛋白:不溶于水而溶于稀盐、稀酸和稀碱,为半饱和硫酸铵所沉淀。
3、谷蛋白:不溶于水、乙醇及中性盐溶液,但易溶于稀酸和稀碱。
4、醇溶谷蛋白:不溶于水及无水乙醇,但溶于70%-80%乙醇、稀酸和稀碱。
蛋白质的分子结构
蛋白质按照不同的结构水平分为一级、二级、三级及四级结构。 蛋白质的构成单元氨基酸通过共价键即肽键连结而成的线性序列称为蛋白质的一级结构。蛋白质的二级结构是指在多肽链的部分氨基酸残基周期性的空间排列。当线性蛋白质链进一步折叠成紧密的三维形式时就形成了蛋白质的三级结构。四级结构是指含有多于一条多肽链的蛋白质分子的空间排列。
稳定蛋白质构象的作用力和键
维持蛋白质高级结构的作用力包括共价键和非共价键(次级键)。
共价键主要指二硫键(个别情况下还包括酯键);非共价键主要指氨基酸残基间的氢键、静电作用、疏水相互作用和范德华力。
除共价键二硫键的键能较大外,其他的作用能较小。
蛋白质的变性(重点)
把蛋白质二级及其以上的高级结构在酸、碱、盐、热、有机溶剂等的作用下遭到破坏而一级结构并未发生变化的过程叫蛋白质的变性。
蛋白质变性所产生的影响:
①溶解度降低; ②与水的结合能力降低;
③生物活性(功能)丧失,如失去酶活性或免疫活性;
④容易被水解; ⑤黏度变大;⑥难以结晶。
影响蛋白质变性的因素
(一)物理因素
1.热与蛋白质变性:当蛋白质溶液被逐渐加热并超过临界温度时,蛋白质将发生从天然状态向变性状态的剧烈转变。在此转变中点的温度被称作熔化温度(Tm)或变性温度(Td)。大多数蛋白质在45~50℃时开始变性,也有些蛋白的Td可以达到相当高的温度。温度导致蛋白质变性主要涉及到非共价相互作用的去稳定作用。氢键、静电和范德华相互作用在高温下不稳定在低温下稳定,而疏水相互作用随温度升高作用力增强(在60-70℃达到最高)。一般认为,温度越低,蛋白质的稳定性越高。蛋白质还可以发生冻结变性。蛋白质的平均疏水性和热变性温度之间呈一定的正相关。蛋白质(或酶)在干燥条件下比含水分时对热变性的耐受力大,说明蛋白质在有水存在时易变性。
2.静水压和变性:压力使蛋白质变性的原因主要是蛋白质的柔性和可压缩性。大多数纤维状蛋白质分子不存在空穴,它们对压力的稳定性高于球状蛋白质。这种蛋白变性是高度可逆的。
3.剪切和变性:一些食品的加工过程,如振动、打擦、捏合、高速均质等,会产生高的剪切力,能导致蛋白质变性。高温和高剪切力相结合能使蛋白质发生不可逆的变性。
4.辐照和变性:电磁波对蛋白质结构的影响与电磁波的波长与能量有关。如果辐照仅引起蛋白质构象的改变,那么将不会显著影响蛋白质的营养价值;如果辐照导致了氨基酸残基的变化,便会导致营养价值的降低。
(二)化学因素
1.pH值和变性:蛋白质在等电点时比其他pH下稳定。在极端pH值时,蛋白质内的离子基团产生强静电排斥作用,促使蛋白质分子的构象发生变化。
2.有机溶质和变性:不同种类的有机物使蛋白变性的原因不尽相同。
3.表面活性剂和变性:表面活性剂,如十二烷基硫酸钠(SDS)是强有力的变性剂,在较低浓度下可使蛋白质完全变性,同时SDS类表面活性剂诱导的蛋白变性是不可逆的。
4.有机溶剂和变性:许多有机溶剂可以导致蛋白质变性。亲水有机溶剂通过改变水的介电常数从而改变了稳定蛋白质结构的静电力;疏水有机溶剂由于进入蛋白质疏水区,打断疏水相互作用,从而导致变性。
5.促溶盐与蛋白质变性:碱土金属只能有限度地与蛋白质起作用,过渡金属如铜、铁、汞和银等离子易与蛋白质发生作用。在低浓度时,盐的离子与蛋白质发生非特异性的静电相互作用,稳定了蛋白质的结构;在高浓度时,盐对蛋白质的稳定性不利,阴离子的影响更大。
蛋白质的功能性质:指在食品加工、保藏、制备和消费期间影响蛋白质在食品体系中的性能的那些蛋白质的物理和化学性质。
蛋白质分子可以通过氢键、静电引力、疏水作用等形式与水分子相互结合
蛋白质的持水能力:蛋白质吸收水并将水保留在蛋白质组织中的能力。
影响蛋白质水合性质的因素主要有:
1、蛋白质的总吸水量随蛋白质浓度的增加而增加;
2、蛋白质在其等电点时水合性质最差,吸水量最少;偏离等电点吸水量增加;
3、随温度的升高,蛋白质水合能力变差;
4、低盐浓度有助于蛋白质分子的水合;高盐浓度将降低蛋白质分子的水化能力。
影响蛋白质溶解度的因素:
1、 pH和溶解度:大多数食品蛋白质的溶解度-pH值图是一条U形曲线,最低溶解度出现在蛋白质的等电点附近。但β-乳球蛋白、明胶、蛋清蛋白和血清清蛋白即使在它们的等电点时,仍然是高度溶解的。
2、离子强度和溶解度:在低离子强度(<0.5),如果蛋白质含有高比例的非极性区域,溶解度下降;反之,溶解度提高。当离子强度>1.0时,硫酸盐和氟化物(盐)逐渐降低蛋白质的溶解度,硫氰酸盐和过氯酸盐逐渐提高蛋白质的溶解度
3、温度和溶解度
在恒定的pH和离子强度,大多数蛋白质的溶解度在0-40℃范围内随温度升高而提高。一些高疏水性的蛋白质的溶解度和温度呈负相关。当温度超过40 ℃,蛋白质的溶解度下降。
4、有机溶剂和溶解度
加入有机溶剂,如乙醇和丙酮,蛋白质在有机溶剂-水体系中的溶解度降低或沉淀。
界面性质
影响蛋白质起泡(水气界面)的因素
a.蛋白质性质:作为起泡剂的蛋白质必须快速地分散至气-水界面;易于在界面上展开和重排;它必须通过分子间相互作用形成黏合性膜。
蛋白质的起泡力是与平均疏水性正相关的。往往具有良好起泡能力的蛋白质不具有稳定泡沫的能力,而能产生稳定泡沫的蛋白质往往不具有良好的起泡力。
b.蛋白溶液浓度:大多数蛋白质在浓度2%~8%范围内显示最高的起泡能力。但浓度超过10%时气泡变小,泡沫变硬。
c.温度:起泡前适当加热可提高一些蛋白的起泡能力,但过度加热会损害蛋白的起泡能力。
d. pH值:当蛋白质处于或接近等电点时,蛋白质的起泡能力和泡沫稳定性提高。在pI以外的pH值范围内,蛋白质的起泡能力往往较好,但其泡沫的稳定性却较差。
e.盐:盐类对蛋白质起泡性质的影响取决于盐的种类、浓度和蛋白质的性质。
f.糖:小分子糖可以提高泡沫的稳定性但却降低蛋白质的起泡能力。
g.脂:脂类物质,尤其是磷脂类物质会使起泡能力和泡沫稳定性下降。 (消泡)
h.搅打:搅打或搅拌的时间和强度既要足够也要适当,过度搅打将破坏泡沫。
影响蛋白质乳化作用(水油界面)的因素主要有:
1.蛋白质的乳化性质与它的表面疏水性存在着一个弱正相关联,然而与平均疏水性不存在这样的关系。
2.蛋白质的溶解度在它的乳化性质方面起着重要的作用。蛋白质必须具有一定的溶解度。
3.pH对蛋白质乳化作用有明显的影响。如果蛋白质在其等电点时仍有较大的溶解度,这种蛋白在此pH具有优良的乳化性能。
蛋白质在热处理中的变化
蛋白质经过热处理会发生一系列的物理和化学变化
热处理的有利影响:经过适当的热处理,绝大多数蛋白质的营养价值会得到提高。因为适度的热处理使蛋白质发生变性,提高了消化率和必需氨基酸的生物利用率和生物有效性;也能使食品中的大多数酶由于变性而失活;使豆类和油料种子中含有的一些抗营养因子失活,使它们不会发生不利于营养物质消化吸收或其它不利的作用。
热处理的不利影响:热处理的不利影响主要表现在氨基酸结构(残基)发生变化,导致营养价值降低。
牛乳中的蛋白质(不用背,了解)
牛乳中含有大约33g/L蛋白质,可分为酪蛋白和乳清蛋白两大类。酪蛋白约占牛乳的蛋白质中80% ,乳清蛋白占20%。
1、酪蛋白:酪蛋白是一类磷蛋白,疏水性很强,在牛乳中聚集成胶团形式。
2、乳清蛋白 :乳清蛋白,主要是β-乳球蛋白和α-乳清蛋白、免疫球蛋白和血清白蛋白。
小麦蛋白质 (不用背,了解)
按溶解度分为清蛋白(溶于水)、球蛋白(溶于10%NaCl,不溶于水),麦醇溶蛋白(溶于70%-90%乙醇)和麦谷蛋白(不溶于水或乙醇而溶于酸或碱)。商业面筋蛋白是从面粉中分离出来的水不溶性蛋白质,主要成分是麦醇溶蛋白和麦谷蛋白。
大豆蛋白质(不用背,了解)
大豆含蛋白质42%,是优良的植物蛋白质。
按溶解性,分为:
清蛋白(5%)
球蛋白(90%) pH = 4.5时沉淀
若用超速离心沉降速度法,可将大豆蛋白分为2S、7S、11S、15S四种组分。
大豆蛋白中,7S、11S的含量最高。
其中7S为37%, 7S组分含量高的豆腐细腻、嫩;
11S为31%, 11S含量高的豆腐结构坚实、有筋性
第六章酶
固定化葡萄糖异构酶
将葡萄糖异构成果糖,可将玉米淀粉水解成葡萄糖后,再异构成高果糖玉米糖浆。
食品原料中的内源酶的作用(第四节重点)
一、颜色 与颜色有关的关键性的酶有脂肪氧合酶、叶绿素酶和多酚氧化酶。
(一)脂肪氧合酶
1、系统名称:亚油酸:氧 氧化还原酶;EC 1.13.11.12
2、作用底物:含顺戊二烯的脂肪酸如亚油酸、亚麻酸、花生四烯酸。
3、产物及适宜pH 使不饱和脂肪酸生成氢过氧化物。 适宜pH值:7~8
4.、对食品质量的影响
(1)有益功能
a.小麦粉、大豆粉的漂白 (活性大豆粉中含脂肪氧合酶、催化胡萝卜素降解而使面粉漂白。)
b.在制作面团过程中形成二硫键,面筋网络形成更好,改善面包等产品质量。
(2)有害作用
a. 破坏叶绿素和胡萝卜素,造成色泽异常; b. 产生氧化性不良风味,具有青草味或豆腥味;
c. 使维生素、蛋白质被氧化破坏 ;d. 必需脂肪酸被氧化破坏。
5. 控制方法: 热处理 如大豆 80~100ºC 10min
二) 多酚氧化酶与酶促褐变
1.多酚氧化酶
(1)系统名称:1,2—苯二酚:氧 氧化还原酶 EC.1.10.3.1
(2) 水果、蔬菜中底物为:一元酚类、邻二酚类、对位二酚也可,但间位二酚不作底物。
(3)辅基:铜 (4)存在:植物、动物和一些微生物(主要是霉菌)中
2、酶促褐变
水果、蔬菜在受到机械性损伤及处于异常环境变化,在酶促下氧化而呈褐色,称为酶促褐变。
3、酶促褐变防止方法
酶促褐变的三个条件,缺一不可。 多酚类物质、酚酶、氧气
除去多酚类物质困难,所以一般为降低酚酶活性、驱氧,用于食品方面主要有以下5种:
(1)加热处理 :在适当温度和时间条件下加热新鲜果蔬,可使酚酶及其它相关的酶都失活。 (2)酸处理法 :酚酶最适pH在4~7之间,PH < 3失活。
(3)二氧化硫及亚硫酸盐类处理 :亚硫酸类是酚酶抑制剂。
(4)驱除或隔绝氧气
(5)加入酚酶底物类似物 :如肉桂酸、对位香豆酸及阿魏酸等酚酸,以肉桂酸的效率最高。
褐变的利用 :期望的褐变: 苹果酒、红茶发酵(生成茶红素)、咖啡、葡萄干、梅干等。
二、质构 影响质构的酶主要有果胶酶、纤维素酶、戊聚糖酶、淀粉酶和蛋白酶等。
(一)果胶酶
1.存在 高等植物、微生物
2.类型 主要有:果胶酯酶、聚半乳糖醛酸酶、果胶酸裂解酶。
(1)果胶酯酶(果胶甲酯酶)
果胶 果胶基水解酶 EC 3.1.1.11 存在:高等植物、细菌、真菌
(2)聚半乳糖醛酸酶
聚-α-1,4-半乳糖醛酸苷糖基-水解酶,EC 3.2.1.15 分内切酶和端解酶
存在:植物、真菌、细菌
(3)果胶裂解酶
聚(1,4-半乳糖醛酸苷)裂解酶,EC 4.2.2.2 存在: 黑曲霉
3.对果蔬质构的影响 :果胶物质是植物细胞的胞间层的主要成分,其聚合度及酯化度的改变会影响其质构,使组织软化。所以在贮藏及运输中应避免伤、烂。
4.应用 果胶酶主要用于果汁加工,可以提高果汁产率和澄清果汁。还可用于澄清果酒。
(二)淀粉酶
1、存在 动物、植物和微生物
2、类型 α-淀粉酶、β-淀粉酶和葡萄糖淀粉酶。
(1) α-淀粉酶(液化酶)
存在:所有生物 作用的键的类型:内切酶,水解α-1,4-糖苷键
(2)β-淀粉酶(转化酶、糖化酶)
存在:高等植物 作用的键的类型:端解酶,从淀粉的非还原末端水解β-1,4-糖苷键
(3)葡萄糖淀粉酶
作用的键的类型:α-1,4-糖苷键和α-1,6-糖苷键
3、应用:应用于淀粉的酶水解,这是食品工业,尤其是发酵工业中的一个重要过程。不仅可以用于生产甜味剂,还可以用于生产乙醇、乙酸、氨基酸等。
(三) 蛋白酶
1、组织蛋白酶
存在:动物组织细胞的溶菌体中。 适宜PH:2.5~4.5
应用:参与肉成熟期间的变化。动物死亡,组织破坏,pH下降,酶激活。
2、钙离子激活中性蛋白酶(CANP)
类型:主要有两种CANPⅠ和CANPⅡ,它们都是二聚体。可以被钙离子激活。
作用:这些酶在宰后的肌肉组织中被激活,在肌肉转变成肉的过程中与组织蛋白酶协同作用
三、风味
氧化物酶 (Peroxidases)
1.存在 高等植物、动物组织、牛奶 2.结构 含有一个血色素作为辅基
3.催化反应 ROOH + AH2→ ROH + H2O + A
4.特性 具有很高的耐热性。含有不耐热部分和耐热部分,热处理后在常温或低温的保藏中,酶活力有部分恢复现象(酶的再生)
四、营养质量
脂肪氧合酶会导致亚油酸、亚麻酸、花生四烯酸、类胡萝卜素、VE、VC和叶酸等的含量下降;破坏Cys、Tyr、Trp、His残基。抗坏血酸氧化酶会破坏VC,硫胺素酶会破坏硫胺素。
多酚氧化酶会降低蛋白质中有效的赖氨酸量。这些作用最终降低食品中营养素的含量或生物利用率,影响食品的营养价值。
第七章 维生素与矿物质
食品中维生素损失的常见原因
1、原料食品的成熟度与部位分布的影响:植物在不同采收期VC含量不同;植物的不同部位含量也不同
2、植物采收后和动物屠宰后处理的影响:内源性酶会分解维生素。
3、加工前处理的影响:浸提,切碎,研磨等均会造成维生素的损失。
4、热烫和热加工的影响:温度越高损失越大,加热时间越长,损失越多
5、 产品贮藏中维生素的损失:水分活度,包装材料及贮藏条件对维生素的保存率都有影响。在相当于单分子层水的AW下,维生素很稳定。
6、 加工中化学添加物和食品成分的影响 : 氧化剂会破坏VA、VE、 VC ,二氧化硫和亚硫酸盐有利于VC的保存,但会与VB1反应。亚硝酸盐可造成VC的破坏。
水溶性维生素
抗坏血酸(VC)最不稳定的维生素,易通过各种方式或途径进行降解食品放置在有氧气的环境或在有氧时持续加热或暴露于光下或处于碱性条件,均会有VC的损失。VC的破坏率随金属的存在而增加,尤其是铜和铁的作用最大。许多酶可加速VC的氧化降解。 食品中的其它成分如花青素及多羟基酸如苹果酸等对VC有保护作用,亚硫酸盐对其也有保护作用。
硫胺素(B1)①其降解受AW影响极大,温度为45℃时,在AW为0.5-0.65范围降解最快。
②对热非常敏感,在碱性介质中加热易分解。
③能被VB1酶降解,同时,血红蛋白和肌红蛋白可作为降解的非酶催化剂。
④对光不敏感,在酸性条件下稳定,在碱性及中性介质中不稳定。
⑤二氧化硫和亚硫酸盐会破坏VB1。
⑥在烹调时因为食物的清洗而大量损失。
核黄素(B2) ①对热稳定,对酸和中性pH也稳定。
②在碱性条件下迅速分解。
③在光照下转变为光黄素和光色素及一系列自由基,破坏其它营养成分产生异味,
维生素A ①对O2、氧化剂 、脂肪氧化酶等因素较敏感;
②光照会加速其氧化;
③在加热、碱性条件和弱酸性条件下较稳定,但在无机强酸条件下不稳定。
维生素D 较稳定,但在光照和氧气存在下会迅速破坏
维生素E
①VE极易受分子氧和自由基氧化,因此可以充当抗氧化剂和自由基清除剂;
②VE对氧、氧化剂、强碱均不稳定
③在食品的加工贮藏过程中,VE会大量损失。由于机械作用损失,或是由于氧化作用损失。
第八章 色素与着色剂
分类:
1、来源
动物色素(血红素) 微生物(红曲色素)
植物色素(叶绿素、类胡萝卜素、花青素等)
2、化学结构
四吡咯衍生物(卟啉类衍生物)如叶绿素、血红素
异戊二烯衍生物(类胡萝卜素) 多酚类衍生物(花青素、叶黄素)
酮类衍生物(姜黄素、红曲色素) 醌类衍生物(虫胶色素、胭脂虫红素)
3、溶解性
脂溶性色素 水溶性色素
食品中的天然色素
血红素化合物
肉色在贮藏加工中的变化
肉中还原态的肌红蛋白向两个不同的方向转变,一部分发生氧合反应生成鲜红色的氧合肌红蛋白,一部分发生氧化反应生成棕褐色的高铁肌红蛋白。随着分割肉在空气中放置时间的延长,肉色就越来越转向褐红色,说明后一种反应逐渐占了上风。上述反应处于动态平衡之中,这种平衡受氧气分压的强烈影响。
①氧合作用 血红素中的亚铁与一分子氧以配位键结合,而亚铁原子不被氧化,生成鲜红色的氧合肌红蛋白。
②氧化作用 血红素中的亚铁与氧发生氧化还原反应,生成棕褐色的高铁肌红蛋白的作用被称为氧化作用。
肉和肉制品的护色
1、真空包装,必要时还可加入除氧剂;
2、高氧分压保护;
3、气调或气控技术,采用100%CO2气体条件,配合使用除氧剂;
4、加入抗氧化剂;
5、腌制肉品的护色措施只要是避光和除氧;
6、不论哪种包装方法,还必需严防微生物生长和失水。
叶绿素类
叶绿素在食品加工储藏中的变化
1、酶促变化:叶绿素酶可直接使叶绿素及脱镁叶绿素脱去植醇。脂酶、蛋白酶、果胶酶等通过作用于相应的底物(非叶绿素),间接使叶绿素遭受破坏。
2、酸和热的作用:在加热中,由于酸的作用,叶绿素发生脱镁反应,生成脱镁叶绿素,并进一步生成焦脱镁叶绿素,使颜色由绿色向橄榄绿到褐色转变。pH影响叶绿素的分解速度,pH9.0时最稳定,3.0时最不稳定。
3、光解:加工储藏中的食品或食品原料,其中所含的叶绿素很易受光作用而分解褪色。
护绿技术
1、中和酸而护绿:中和酸的重点是绿色植物内部不断产生的酸性物质,所以要长期保持体系中pH接近中性,要采取一些特殊的方法,如缓慢释放的碱等。
2、高温瞬时杀菌:能显著减轻植物性食品在杀菌中发生的绿色破坏程度。
3、绿色再生:绿色再生技术是利用一定的方法将叶绿素中的镁置换为锌或铜。
4、其它方法如气调保鲜技术等。
类胡萝卜素化合物
胡萝卜素类目前指四种物质:α-胡萝卜素、β-胡萝卜素、γ-胡萝卜素、番茄红素
胡萝卜素类为典型的脂溶性色素,易溶于石油醚、乙醚难溶于乙醇。
叶黄素类
叶黄素类是胡萝卜素类的含氧衍生物,随着含氧量的增加,它们的脂溶性下降 ,因此叶黄素在甲醇和乙醇中很好溶解,而难溶于乙醚、石油醚,有个别甚至亲水。
花色苷类
花色苷是黄酮的一种,具有2-苯基苯并吡喃阳离子结构。
第九章 食品风味
风味的概念:是指摄入口腔的食物使人的感觉器官,包括味觉、嗅觉、痛觉及触觉等在大脑中留下的综合印象。
嗅觉理论 立体化学理论 2、膜刺激理论 3、振动理论
风味物质的特点:
食品中的风味物质一般具有以下的特点:
(1)种类繁多,相互影响。 (2)含量极微,效果显著。
(3)大多数是非营养物质。 (4)呈味性能与其分子结构有高度特异性的关系。
(5) 稳定性差,容易被破坏。
影响味觉产生的因素
1、物质的结构
糖类—甜味 酸类—酸味 盐类—咸味 生物碱—苦味
2、浓度和溶解度
适当的浓度使人愉快,否则使人不愉快。完全不溶于水的物质是无味的,溶解度小于阈值的物质也是无味的。所谓阈值是指能够感受到该物质的最低浓度,
3、温度
最适宜的味觉产生的温度是10-40℃,尤其是30℃最敏感,大于或小于此温度都将变得迟钝。
呈甜机理 AH/B理论→AH-B-γ学说
-
食品化学知识点总结
食品化学知识点总结1食品剖析的目的包含两方面一方面是确切了解营养成分如维生素蛋白质氨基酸和糖类另一方面是对食品中有害成分进行监测如…
-
西北农林科技大学食品化学总结
第一章绪论食品化学从化学的角度和原子离子分子的水平研究食品的化学组成结构理化性质生理生化性质营养与功能性质及它们在食品储藏加工运输…
-
食品化学总结
绪论定义食物营养素食品化学食物是指含有营养素的可食性物料营养素是指那些能维持人体正常生长发育和新陈代谢所必需的物质蛋白质脂质碳水化…
-
食品化学总结
第二章水水溶质相互作用一与离子和离子基团的相互作用P15当食品中存在离子或可解离成离子或离子基团的盐类物质时产生偶极离子相互作用可…
-
食品化学自我总结
食品化学食品化学考试内容主要包括食品的化学组成食品的营养成分和食品色香味成分的结构性质食品加工储藏过程中营养成分和色香味成分的变化…
-
某某区20xx年清真食品检查总结
***区20xx年清真食品检查总结为认真贯彻《***清真食品管理条例》,进一步加强对社区清真食品的管理,尊重食用清真食品民族的饮食…
-
重庆大学“化学与生活”论文《食品添加剂》
《化学与生活》课程论文--浅谈食品添加剂食品添加剂是近代才出现,但它的直接应用可以追溯到很久以前。中国在远古时代就有在食品中使用天…
-
食品风味化学分析总结
食品风味化学分析总结一.名词解释1.RI值:即保留指数,保留指数仅与固定相的性质、柱温有关,与其它实验条件无关。其准确度和重现性都…
-
食品安全学总结
绪论一概念1食品安全p4食品无毒无害符合应有的营养要求对人体健康不造成任何急性亚急性或慢性危害2无公害食品指在良好的生态环境条件下…
-
课题_《食品化学与生活》课程论文
食品化学论文题目学院班级20xx级应用化学2班姓名完成日期20xx年05月03日食品化学与生活课程论文浅谈食品添加剂摘要食品是我们…