氧化还原反应知识点归纳
氧化还原反应知识点归纳
(氧化还原反应中的概念与规律;氧化还原反应的表示方法及配平。)
氧化还原反应中的概念与规律:
一、 五对概念
在氧化还原反应中,有五对既相对立又相联系的概念。它们的名称和相互关系是:
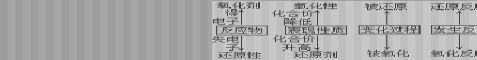
二、 五条规律
1、表现性质规律
同种元素具有多种价态时,一般处于最高价态时只具有氧化性、处于最低价态时只具有还原性、处于中间可变价时既具有氧化性又具有还原性。
2、性质强弱规律
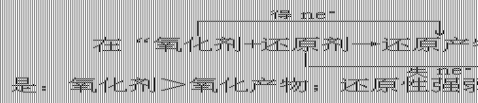
3、反应先后规律
在浓度相差不大的溶液中,同时含有几种还原剂时,若加入氧化剂,则它首先与溶液中最强的还原剂作用;同理,在浓度相差不大的溶液中,同时含有几种氧化剂时,若加入还原剂,则它首先与溶液中最强的氧化剂作用。例如,向含有FeBr2溶液中通入Cl2,首先被氧
2+化的是Fe
4、价态归中规律
含不同价态同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价→中间价”的规律。
5、电子守恒规律
在任何氧化—还原反应中,氧化剂得电子(或共用电子对偏向)总数与还原剂失电子(或共用电子对偏离)总数一定相等。
三.物质氧化性或还原性强弱的比较:
(1)由元素的金属性或非金属性比较
<1>金属阳离子的氧化性随其单质还原性的增强而减弱

非金属阴离子的还原性随其单质的氧化性增强而减弱

(2)由反应条件的难易比较
不同的氧化剂与同一还原剂反应时,反应条件越易,其氧化剂的氧化性越强。如:
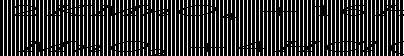
前者比后者容易发生反应,可判断氧化性:
与同一氧化剂反应时,反应条件越易,其还原剂的还原性越强。
(3)根据被氧化或被还原的程度不同进行比较
当不同的氧化剂与同一还原剂反应时,还原剂被氧化的程度越大,氧化剂的氧化性就越强。如 ,根据铁被氧化程度的不同 , 。同理,不同的还原剂可判断氧化性: 。同理,当不同的还原剂与同一氧化剂反应时,氧化剂被还原的程度越大,还原剂的还原性就越强。
(4)根据反应方程式进行比较
氧化剂+还原剂=还原产物+氧化产物
氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物
(5)根据元素周期律进行比较
一般地,氧化性:上>下,右>左;还原性:下>上,左>右。
(6)某些氧化剂的氧化性或还原剂的还原性与下列因素有关:
温度:如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
浓度:如浓硝酸的氧化性比稀硝酸的强。 酸碱性:如中性环境中 不显氧化性,酸性环境中 显氧化性;又如 溶液的氧化性随溶液的酸性增强而增强。
注意:物质的氧化性或还原性的强弱只决定于得到或失去电子的难易,与得失电子的多少无关。如还原性: ,氧化性:。
【注意】氧化还原反应中的不一定:
⑴含有最高价态元素的化合物不一定具有强氧化性。如前述的氯元素的含氧酸及其盐,
是价
态越低,氧化性超强。H3PO4中+5价的P无强氧化性。
⑵有单质参加的反应不一定是氧化还原反应。如同素异形体之间的转化。
⑶物质的氧化性或还原性与物质得到或掉失去电子的多少无关。
⑷得到电子难的元素失去电子不一定容易,例如:第ⅣA族的C,既难得到电子,又难失去电
子,与其它原子易以共价键结合。
⑸元素由化合态变为游离态不一定是是氧化反应,也可能是还原反应。
四、常见的氧化剂和还原剂
1、常见的氧化剂
(1)活泼的非金属单质:Cl2、Br2、O2、I2、S等
(2)元素处于高价时的氧化物:CO2、NO2、SO3、MnO2、PbO2等
(3)元素处于高价时的含氧酸:浓H2SO4、HNO3等
(4)元素处于高价时的盐:KClO3、KMnO4、FeCl3、K2Cr2O7等
(5)过氧化物:Na2O2、H2O2等
(6)次氯酸及其盐:HClO、Ca(ClO)2、NaClO等
2、常见的还原剂
(1)活泼的金属单质:Na、Mg、Al、Zn、Fe
(2)某些非金属单质:H2、C、Si
(3)元素处于低价时的氧化物:CO、、SO2
(4)元素处于低价时的酸:HCl、HI、H2S、H2SO3等
(5)元素处于低价时的盐:Na2S、KI、Na2SO3、FeSO4等
氧化还原反应的表示方法及配平
1、表示方法
2、 配平的方法和步骤:
写好化学式,标明化合价;画上双箭头,列出变化价;
升降化合价,公倍求相等;观察再配平,两边添系数。
步骤:(1)标出有变价的元素反应前后的化合价.
(2)用“双桥线”连接反应前后的元素并在桥上或桥下注明化合价升降数.
(3)找出化合价升降数之间的最小公倍数,再依据以上有关原则首先配平有关物
质前面的系数.
要求:(1)质量守恒:即反应前后各元素原子的种类和个数相等.
(2)氧化剂和还原剂之间电子转移关系正确.
(3)电荷守恒:反应物总电荷数与生成物总电荷数相等,且电性相同.
常见的氧化还原反应方程式的配平
(1)整体法的应用:
A.还原剂或氧化剂的所有元素完全被氧化或完全被还原,可以看成一个整体,在配平时按各元素的系数比考虑得失电子的总数.如

:
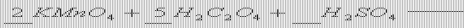
分析:H2C2O4中碳元素的平均价态为+3价,都被氧化到+4价,可考虑整体法 H2C2O4中
KMnO4中2C:?3??4?1?2?2 ×5指H2C2O4计量数为5 Mn:?7??2?5 ×2指KMnO4计量数为2
B.还原剂或氧化剂的元素部分被氧化或部分被还原,不能看成一个整体,要分别考虑.如:
Cl2?H2O______HCl?HClO
分析:氯气中的氯元素部分被还原,部分被氧化,分别考虑
Cl2中Cl:0??1(HCl)?1 ×1指HC1O计量数为1
Cl:0??1(HClO)?1 ×1指HC1计量数为1
(2)离子型氧化还原反应配平
离子型氧化还原反应配平时,遵循整体法配平的同时,还可从两边的电荷守恒出发.如

分析:Na2O2中的氧元素都被还原为-2价,可用整体法
Cr3?:?3??6?3 ×2指Cr3?计量数为2
Na2O2中2O:?1??2?1?2?2 ×3指Na2O2计量数为3
根据电荷守恒,用观察法配平其他化学计量数:
2Cr3?3Na2O2?4OH?
(3) 难点突破: 2CrO42??6Na??2H2O
1.缺项配平:
一般先确定氧化剂、还原剂、氧化产物、还原产物的化学计量数,在通过比较反应物与
??生成物,确定缺项(一般为H2O、H、OH),最后观察法配平.
3?将NaBiO3固体加入MnSO无色),反应的4的混合溶液里,加热后溶液显紫色(Bi
离子方程式如下:
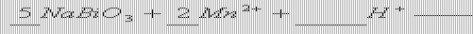
试
完成并配平方程式.
分析:溶液显紫色说明由MnO4生成,H与NaBiO3的氧元素生成H2O,所以右边缺项为MnO4和H2O. ???
NaBiO3中Bi:?5??3?2 ×5指NaBiO3计量数为5
Mn2?:?2??7?5 ×2指Mn2?计量数为2
根据电荷守恒,用观察法配平其他化学计量数:
5NaBiO3?2Mn2??14H?
2.零价配平: ?5Na??5Bi3??2MnO4?7H2O
复杂的化合物中的化合价无法标出,且仅靠观察法也无法配平,此时可把不知(或难知)化合价的物质看成一个电中性的整体,假设其中所有的元素都为0价,在根据化合价升降配平方程式,不影响配平结果.但需要注意的是:按零价法分析的价态升降根据与该反应实际的价态升降不符,零价法只是配平的一种方法和技巧.
1Fe3C?HNO3_____Fe(NO3)3?13NO2??CO2??H2O分析:设Fe3C中各元素均为0价
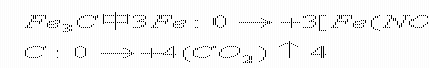
×1指Fe3C计量数为1
×13指NO2计量数为13
HNO3中N:?5??4(NO2)?1
有观察法配平其他化学计量数:
1Fe3C?22HNO33Fe(NO3)3?13NO2??1CO2??11H2O
3.均价配平:
适用于有机氧化还原方程式的配平.根据氢元素为+1价,氧元素为-2价,确定碳元素的平均价态,在通过适当方法配平.
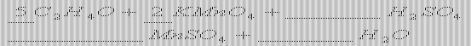
分析:C2H4O中2C:?1?0?1?2?2 ×5指C2H4O计量数为5
×2指KMnO4计量数为2 KMnO4中Mn:?7??2?5
用观察法配平其他化学计量数:

第二篇:专题一 氧化还原反应 知识点归纳
专题 一 氧化还原反应
考试大纲:理解氧化还原反应,了解氧化剂和还原剂等概念。掌握重要的氧化剂、还原剂之间常见的反应。能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
知识清单
一、氧化还原反应
1、氧化还原反应的本质:
升、失、氧化( )、还原( )、还原( )、氧化( )
降、得、还原( )、氧化( )、氧化( )、还原( )
2、氧化还原反应与四大基本反应的关系
二、常见氧化剂和还原剂
1、常见氧化剂 2、常见还原剂
(1)、活泼的非金属单质: 1)、单质(金属、非金属):
(2)、高价金属阳离子: 2)、低价金属阳离子:
(3)、高价含氧化合物: 3)、低价氧化物:
(4)、过氧化物: 4)、非金属阴离子及其低价化合物:
从元素化合价考虑,高价态只有氧化性,低价态只有还原性,中间价态既有氧化性又有
还原性。
注意:最高价元素的化合价不一定不低价化合物氧化性强,如氧化性HClO4<HClO
3、判断氧化性(还原性的方法)
氧化性、还原性的强弱取决于得失电子的难易程度,与得失电子的数目无关。
1)、金属活动顺序表
K Ca


Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属单质还原性减弱,对应阳离子氧化性增强
Zn2+<Cr3+<Fe2+<Ni2+<Sn2+<Pb2+<(H)<Cu2+<Hg2+3++非金属活动顺序
F Cl/O Br I S N P C Si H
非金属单质氧化性减弱,对应阴离子还原性增强
2)、根据在元素周期表中的位置
(1)同主族元素从上到下
非金属原子(或单质)氧化性逐渐减弱,金属原子还原性逐渐增强
周期元素从左到右,还原性减弱,氧化性增强。
专题 一 氧化还原反应
3)、元素最高价氧化物的水化物的酸性
HClO4>H2SO4>H3PO4>H2CO3 氧化性:Cl2>S>P>C
4)、化学反应方向
氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物
5)、氧化产物价态高低
当含有变价元素的还原剂在相似的条件下作用于不同的氧化剂时,可根据氧化产物价态的高低来判断氧化剂氧化性强弱。
6)、根据反应条件
当不同氧化剂分别于同一还原剂反应时,如果氧化产物价态相同,可根据反应条件的难易来判断。反应越容易,该氧化剂氧化性就强。
7)、根据物质的浓度大小
具有氧化性(或还原性)的物质浓度越大,氧化性(还原性)越强。
8)、电极反应判断
原电池: 其还原性:负极金属>正极金属
电解池:惰性电极电解,在阴极先放电的阳离子氧化性较强,在阳极先放点的阴离子还原性较强。
三、配平方法
1)、逆向配平法(部分氧化还原、自身氧化还原、歧化反应)
K2CrO7 + HCl(浓)------ KCl + CrCl3 + Cl2 + H2O
2)、零价配平法(无法用常规方法确定其化合价)
Fe3C + HNO3 ------- Fe(NO3)3 + NO2 + CO2+ H2O
3)、整体标价法(当某一元素在某一化合物中有数个时,可将其看做一个整体) S + Ca(OH)2 ------- CaSx + CaS2O3 + H20
4)、缺项配平法(先配平含有变价的化合物,再通过比较观察配平)
H202 + Cr(SO4)3 + ------- K2SO4 + K2CrO4 + H2O
四、氧化还原计算
氧化剂的物质的量X变价元素原子个数X化合价的变化=还原剂的物质的量X变价元素原子个数X化合价的变化
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳(氧化还原反应中的概念与规律;氧化还原反应的表示方法及配平。)氧化还原反应中的概念与规律:一、五对概念在氧化…
-
高中化学知识点总结氧化还原反应
燕园教育教师培训手册三氧化还原反应1准确理解氧化还原反应的概念11氧化还原反应各概念之间的关系1反应类型氧化反应物质所含元素化合价…
-
氧化还原反应知识点总结
一氧化还原基本概念1四组重要概念间的关系1氧化还原反应凡是反应过程中有元素化合价变化或电子转移的化学变化叫氧化还原反应氧化还原反应…
-
高一化学之三 氧化还原反应知识点总结
714氧化还原反应知识点一概念氧化还原反应的实质电子的转移电子的得失或共用电子对的偏移口诀失电子化合价升高被氧化氧化反应还原剂得电…
-
氧化还原反应知识点总结
专题四氧化还原反应一氧化还原反应的基本概念1基本概念略氧化还原反应氧化反应还原反应氧化剂还原剂等2知识体系3常见氧化剂1活泼非金属…
-
氧化还原反应知识点总结
一氧化还原基本概念1四组重要概念间的关系1氧化还原反应凡是反应过程中有元素化合价变化或电子转移的化学变化叫氧化还原反应氧化还原反应…
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳一、概念1、氧化反应:元素化合价升高的反应还原反应:元素化合价降低的反应氧化还原反应:凡有元素化合价升降的化…
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳(氧化还原反应中的概念与规律;氧化还原反应的表示方法及配平。)氧化还原反应中的概念与规律:一、五对概念在氧化…
-
氧化还原反应知识点总结
专题四氧化还原反应一氧化还原反应的基本概念1基本概念略氧化还原反应氧化反应还原反应氧化剂还原剂等2知识体系3常见氧化剂1活泼非金属…
-
氧化还原反应知识点总结
一氧化还原基本概念1原反应氧化还原反应的特征元素化合价的升降氧化还原反应的实质电子转移2氧化反应和还原反应在氧化还原反应中反应物所…
-
高一化学下册知识点总结
高一化学必修二知识点总结一、元素周期表★熟记等式:原子序数=核电荷数=质子数=核外电子数1、元素周期表的编排原则:①按照原子序数递…