氧化还原反应知识系统总结
专题一:氧化还原反应及其配平
一、基本概念
[例1]火法炼铜首先要焙烧黄铜矿,其反应:2CuFeS2+O2 Cu2S+2FeS+SO2下列说法正确的是
Cu2S+2FeS+SO2下列说法正确的是
A. SO2既是氧化产物又是还原产物 B.CuFeS2仅作还原剂,硫元素被氧化
C.每生成1mol Cu2S,有4 mol硫被氧化D.每转移1.2 mol电子,有0.2 mol硫被氧化
答案:AD
[知识规律]
还原性 化合价升高 弱氧化性
 ↑
↑


 ↑
↑




 还原剂 氧化反应 氧化产物
还原剂 氧化反应 氧化产物


 氧化剂 还原反应 还原产物
氧化剂 还原反应 还原产物


 ↓
↓ 

 ↓
↓
氧化性 化合价降低 弱还原性
二、常见的氧化剂、还原剂归纳
【例2】(肇庆中学20##届高三10月考)一种海水电池的反应原理可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,有关该反应的说法正确的是
A.反应中MnO2是还原剂 B.Ag的还原性比Na2Mn5O10强
C.该反应中MnO2具有催化作用 D.每生成1 mol Na2Mn5O10转移1 mol电子
答案:B
三、物质的氧化性强弱、还原性强弱的比较。
[例3](2012浙江?13)化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:
2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl; 2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2Fe(OH)2 + I2 + 2KOH= 2Fe(OH)3 + 2KI; 3I2 + 6KOH= 5KI + KIO3 + 3H2O
复分解反应:
2HSCN + K2CO3 = 2KSCN + CO2 ↑ + H2O; KCN + CO2 + H2O = HCN + KHCO3
热分解反应:
4NaClO  3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是:
A.氧化性(酸性溶液):FeCl3 > Co(OH)3> I2 B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3
C.热稳定性:NaCl > NaClO4 > NaClO D.酸性(水溶液):HSCN > H2CO3 > HCN
答案:A
四、能判断氧化还原反应中的电子转移方向和数目
1、双线桥分析法 2、单线桥分析法
【例4】用双线桥法分析氧化还原反应:CuO+H2======Cu+H2O



 +
+  =====
=====  +
+ 

五、考查氧化还原反应的计算
得失电子守恒:氧化还原反应中得失电子的物质的量相等;
质量守恒:反应前后各元素原子的物质的量相等;
电荷守恒:在离子反应中,阴离子所带的电荷总数与阳离子所带的电荷总数相等
【例5】将0.195g锌粉加入到20.0 mL的0.100 mol.L-1 MO2+溶液中,恰好完全反应,则还原产物可能是
A. M B.M2+ C. M3+ D.MO2+
D.MO2+
答案:B
练习.某含铬Cr2O72- 废水用硫亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3 。不考虑处理过程中的实际损耗,下列叙述错误的是
A.消耗硫酸亚铁铵的物质量为n(2-x)mol B.处理废水中Cr2O72- 的物质量为mol
C.反应中发生转移的电子数为3nx mol D.在FeO·FeyCrxO3中3x=y
答案:A
六、氧化还原反应方程式的配平
(一)、配平原则1、化合价升降守恒(即得失电子守恒)2、质量守恒
(二)、配平步骤:标变价、列变化、求总数、配系数
(三)、几种不同类型的氧化还原方程式的配平技巧
1、氧化剂、还原剂中某元素化合价全升全降
技巧:以反应物或生成物作为参照物均可
C6H12O6+ KNO3 — CO2↑+  N2↑+ KOH+ H2O
N2↑+ KOH+ H2O
2、反应物中某一物质中元素化合价部分变化
技巧:一般以生成物作为参照物
Fe+ HNO3(浓) — Fe(NO)3+ NO2↑+ H2O
3、对于歧化、分解、归中、化合反应
技巧:看分不看合
P+ KOH+ H2O — PH3+ KH2PO2 KClO3—— KCl + O2↑
NH3 + NO — N2 + H2O NO+ O2+ H2O — HNO3
4、同一物质中有多种元素化合价发生改变
技巧:整体法配
FeS2 + O2 — Fe2O3 + SO2
Cu2S+ HNO3 — H2SO4+ Cu(NO3)2+ NO↑+ H2O
P+ CuSO4+ H2O — Cu3P+ H3PO4+ H2SO4
KMnO4+ H2O2+ H2SO4— K2SO4+ MnSO4 + O2↑+ H2O
KClO3 + HCl — Cl2↑+ KCl + H2O
Cl2 + NH3 — NH4Cl + N2
S + KOH — K2S + K2SO3 + H2O
CrI3+ Cl2+ KOH— K2CrO4+ KIO4 + KCl+ H2O
(四)、氧化还原反应离子方程式的配平
方法:离子方程式的配平与化学方程式一致,只是检查时应注意质量守恒和电荷守恒!顺序:一电子、二电荷、三原子。即先确保电子守恒,在考虑等号前后的电荷相 等。
等。
Cr2O72-+ Cl-+ H+ — Cr3++ Cl2↑+ H2O
MnO4- + I-+ H+— Mn2++ IO3-+ H2O
Cl-+ ClO2-+ H+— Cl2↑+ H 2O
2O
Cr2O72-+ Fe2++ H+— Cr3++ Fe3++ H2O
(五)、缺项配平
方法:缺项的氧化还原方程式配平时,先用化合价升降法配出发生氧化还原的系数,再观察两端, 通过比较反应物与生成物,观察增减的原子或离子数,确定未知物并配平(元素守恒和电荷守恒)一般为酸、碱、H2O 。
。
KMnO4+ KNO2+ [ ]= MnSO4+ K2SO4+ KNO3+ H2O
MnO4- + Cl-+ [ ] — Mn2++ Cl2↑+ H2O
P + KOH+ [ ] = KH2PO4 + PH3
MnO4- + NO2-+ [ ] = MnO42-+ NO3- + H2O
KI+ KIO3+ [ ] — I2+ K2SO4+ H2O
新信息化学方程式的书写
1.高锰酸钾在水溶液中放出活性氧,起到消毒作用,同时生成+4价的氢氧化锰和氢氧化钾。若活性氧用[O]来表示,请写出该反应的化学方程式
2.铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度的硝酸反应时,可将方程式表示为:Cu+HNO3=Cu(NO3)2+NO↑+NO2↑+H2O。
(1)硝酸在该反应中的作用是 ,该反应的还原产物是 。
(2)0.3mol Cu被硝酸完全溶解后,Cu失去的电子数是 ,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是 ,若用排水法收集这些气体,可得标准状况下的气体体积 。
(3)如果参加反应的Cu和HNO3的物质的量之比是3︰10,写出并配平该反应的离子方程式。
(4)如果没有对该反应中的某些物质的比例作限定,则方程式可能的配平系数有许多组。原因是 。
3.(原创)铁酸钠(Na2FeO4)是一种新型净水剂,制取铁酸钠的离子反应方程式为: Fe3++OH-+Cl2→FeO42-+Cl-+H2O,该反应的离子方程式中H2O的化学计量数是( )
A.4 B.6 C.10 D. 8
4.某些非金属单质能发生自身氧化还原反应(歧化反应)。例如,硫在碱液中加热,零价的硫被歧化为负二价态和正四价态;碘在碱液中能歧化为负一价态和正五价态。试分别写出硫和碘在碱液中发生歧化反应的离子方程式 。
5.硫粉、炭粉与硝酸钾混合,可以得到黑火药。黑火药爆炸的产物与其组成有关。一般黑火药组成为一硫二硝三碳,爆炸产物为K2S、N2、CO2。
(1)写出黑火药爆炸反应的化学方程式
该反应的氧化剂是 ,还原剂是 。
(2)求氧化产物与还原产物的物质的量之比 。
6.某校曾发生在实验室中学生误将高锰酸钾与红磷相混,发生爆炸,造成一死一残的严重事故。试写出这一变化的化学方程式(KMnO4的还原产物是MnO2) (并用双线桥标明化合价升降)
7.某一反应体系中共有Pb3O4、NO、MnO2、Cr2O3、Cr(MnO4)2和Pb(N3)2(名称叠氧化铅,其中Pb为+2价)六种物质,已知Pb(N3)2是反应物之一。根据你学过的有关化学定律和知识,试写出 这个反应的化学方程式 。
8.完成并配平以下化学方程式。
(1)在MnBr2的硝酸溶液中,加入PbO2,反应后溶液呈紫红色,并有溴单质生成。(要求:化学方程式,用双桥式表示电子得失关系)
(2)在一支试管中,盛少量As2O3和K2S粉末(物质的量之比为1︰2),往其中加入足量硝酸并微热。(提示:As和S氧化为最高价态,HNO3还原为NO。要求:用一个化学方程式反映出还原剂的物质的量之比)
(3)在SnCl2的硫酸溶液中滴入KMnO4至刚好反应完全。(要求:写离子方程式)
9.完成并配平以下化学方程式。
(1)氯化钠、溴化钠、碘化钠晶体分别与浓硫酸共热(300℃以下)。【提示:碘化钠可跟浓硫酸反应生成硫化氢。】
(2)在MnBr2的硝酸溶液中,加入PbO2,反应后溶液呈紫红色,并有溴单质生成。(要求:化学方程式,用双桥式表示电子得失关系)
(3)在一支试管中,盛少量As2O3和K2S粉末(物质的量之比为1︰2),往其中加入足量硝酸并微热。(提示:As和S氧化为最高价态,HNO3还原为NO。要求:用一个化学方程式反映出还原剂的物质的量之比)
(4)在SnCl2的硫酸溶液中滴入KMnO4至刚好反应完全。(要求:写离子方程式)
10.固态KMnO4在200℃加热,失重10.8%。
固态KMnO4在240℃加热,失重15.3%。写出上述两个反应的化学方程式
。
。
11.为实现消除碘缺乏病的目标,国家卫生部规定食盐必须加碘,其中碘以碘酸钾或碘化钾的形式存在。
(1)有人烹调时,分别含有碘化钾和碘酸钾的加碘食盐混合,当滴食醋时,产生紫色蒸气,反应的离子方程式为
(2)这两种加碘食盐可以在潮湿的空气中曝露而加以鉴别,其原理是
(用离子方程式表示)。
12.分析化学上常用硫代硫酸钠与单质碘反应来进行元素分析。硫代硫酸根(S2O3 )离子与I2之间的反应进行得迅速、完全,但必须在中性或弱酸性溶液中进行。因为在碱性溶液中,I2会发生反应,其离子方程式为 :而且I2与S2O32-发生副发应,其离子方程式为 。
)离子与I2之间的反应进行得迅速、完全,但必须在中性或弱酸性溶液中进行。因为在碱性溶液中,I2会发生反应,其离子方程式为 :而且I2与S2O32-发生副发应,其离子方程式为 。
若在强酸性溶液中,Na2S2O3会发生分解,其离子方程式为 ,
同时I 离子容易与空气中的氧气发生反应,其反应的离子方程式为 。在用碘量法进行测定时,为防止碘的挥发,在实验中首先应该采取的措施是 。
离子容易与空气中的氧气发生反应,其反应的离子方程式为 。在用碘量法进行测定时,为防止碘的挥发,在实验中首先应该采取的措施是 。
13.[2008·全国Ⅰ,26.有删改]实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿和过量的固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩溶液,结晶得到深紫色的针状KMnO4。试回答:(1)软锰矿制备K2MnO4的化学方程式是 ;
(2)K2MnO4制备KMnO4的离子方程式是 ;
(3)若用2.5g软锰矿(含MnO280%)进行上述实验,计算KMnO4的理论产量:
(4)KMnO4能与热的经硫酸酸化的Na2C2O4反应,生成Mn2+和CO2,该反应的化学方程式是 。
14.铁酸钠(Na2FeO4)是处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成Fe3+离子。
(1)配平制取铁酸钠的化学方程式:
□Fe(NO3)3+□NaOH+□Cl2---□Na2FeO4+□NaNO3+□NaCl+□H2O
反应中 元素被氧化,转移电子总数为 。
(2)铁酸钠之所以能净水,除了能消毒杀菌外,另一个原因是 。
15.在一定条件下,将m体积NO和n体积O2同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留m/2体积的气体,该气体与空气接触后变为红棕色,则m与n的比值为 .。
新信息化学方程式的书写练习
1.铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2中加入,铜屑可以逐渐溶解,该反应的离子方程式:
2.将20mL 0.5mol·L-1 K2SO3溶液逐滴加入到20 mL 0.2mol·L-1 KMnO4溶液(硫酸酸化)中,溶液恰好褪为无色。写出反应的离子方程式:________________________________
3.已知CO是工业上常用的还原剂,500℃时,11.2 L(标准状况)SO2在催化剂作用下与CO发生化学反应。若有2×6.02×1023个电子转移时,写出该反应的化学方程式 。
4.在氢氧化钠的环境中,氯气与碘化钠反应,每1摩碘化钠完全反应转移6摩尔电子,反应化学方程式为
5.氮气的实验室制法是用氯化铵(NH4Cl)与亚硝酸钠(NaNO2)反应,同时生成氯化钠和水.写出该反应的化学方程式:
6.(07上海)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e→NO+2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:__________________
7.根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(2)某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
(3)写出Cl2将Z氧化为K2EO4的化学方程式: 。
8.工业上利用KOH和MnO2为原料制取KMnO4。主要生产过程分两步进行:
第一步将MnO2和固体KOH粉碎,混合均匀,在空气中加热至熔化,并连续搅拌以制取K2MnO4;
第二步为电解K2MnO4的浓溶液制取KMnO4。
① 第一步反应的化学方程式为________________________________________。
② 电解K2MnO4的浓溶液时,电解池中阴极的实验现象为______________________________。
9.K2FeO4也是一种常见的理想净水剂,工业上有多种方法制备高铁酸钾。
 A.① 电解法:原理如右图所示。阴极的电极反应
A.① 电解法:原理如右图所示。阴极的电极反应
是 。
② 湿法氧化:在溶液中用次氯酸钠、氢氧化铁和氢氧化钾
制高铁酸钾,其反应的离子方程式为: 。
B. 已知K2FeO4溶液中加入稀硫酸,迅速反应产生Fe2(SO4)3的离子方程式
C. 用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,已知该电池的总
反应是: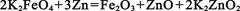 ,则负极的电极反应是
,则负极的电极反应是
。
10.污水及自来水处理的方法有很多
(1)碱性环境下,Cl2可将水中的CN-转化为两种无毒的气体
(2)酸性环境下,向含重铬酸根的废水中加入FeSO4溶液,然后调节溶液的PH,使生成的Cr3+转化为Cr(OH)3,写出第一步对应的离子方程式:
(3)含CN-的污水危害很大。处理污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-。CNO-在酸性条件下继续被NaClO氧化生成N2和CO2。试写出上述两步反应的离子方程式:
(4)臭氧也是一种常用的污水处理剂。它的氧化性很强,可以和酸性KI淀粉溶液反应,呈现蓝色,同时放出一种气体,试写出对应的离子方程式
(5)二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定。温度过高,二氧化氯的水溶液有可能爆炸。其制备方法有:
方法一:用氯酸钠(NaClO3)和硫酸酸化的H2O2反应生成ClO2。请写出该反应的化学方程式。
NaClO3+H2SO4+H2O2ClO2。
方法二:用氯酸钠氧化浓盐酸,生成二氧化氯的同时会有氯气产生。请写出该反应的离子方程式。
比较两种方法的优缺点:
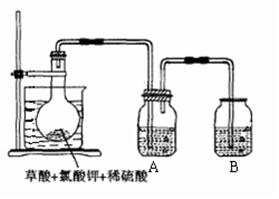
方法三、
①如图,在烧瓶中先放入一定量的KClO3和草酸(H2C2O4),
然后再加入足量的稀硫酸,水浴加热。反应后产物中有
ClO2、CO2和一种酸式盐,该反应的化学方程式为:
,
氧化产物与还原产物的物质的量之比为 。
② 控制水浴温度在60~80℃之间的目的是 ,
图示装置中缺少的一种必须的玻璃仪器是 。
③A装置用于吸收产生的二氧化氯,其中最好盛放 。(填序号)
①60 ℃的温水 ②冰水 ③饱和食盐水
④将足量二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成。请写出二氧化氯溶液和硫化氢溶液反应的离子方程式。
新信息化学方程式的书写答案
1.【答案】2KMnO4+5H2O=2KOH+2Mn(OH)4+3[O]
2.【答案】(1)氧化剂、酸 NO、NO2
(2)0.6mol 0.9mol 4.48L
(3)3Cu+10H++4NO3-=3Cu2++NO↑+3NO2↑+5H2O
(4)该反应式含两种还原产物,两者的比例和氧化剂、还原剂的用量都可以发生变化。
3.【答案】D
4.【答案】3S+6OH-=2S2-+SO32-+3H2O 3I2+6OH-=5I-+IO3-+3H2O
5.【解析】(1)S+2KNO3+3C K2S+N2+3CO2,从此化学方程式可以看出,反应物的化学计量数正好是一硫二硝三碳。氧化剂S、KNO3,还原剂是C。(2)还原产物K2S、N2,氧化产物CO2,所以氧化产物与还原产物的物质的量之比是3︰2。
K2S+N2+3CO2,从此化学方程式可以看出,反应物的化学计量数正好是一硫二硝三碳。氧化剂S、KNO3,还原剂是C。(2)还原产物K2S、N2,氧化产物CO2,所以氧化产物与还原产物的物质的量之比是3︰2。
6.【答案】
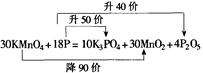
7. 【答案】15Pb(N3)2+44Cr(MnO4)2 22Cr2O3十88MnO2+5Pb3O4+90NO↑
22Cr2O3十88MnO2+5Pb3O4+90NO↑
8.【答案】(1)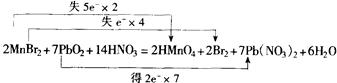
(2)3As2S3+6K2S+56HNO3=6H3AsO4+15H2SO4+44NO↑+4H2O+12KNO3。
(3)5Sn2++10Cl-+4MnO4-+32H+=5Sn4++5Cl2↑+4Mn2++16H2O
9.【答案】2KMnO4=K2MnO4+MnO2+O2↑或2KMnO4=K2Mn2O6+O2↑
4KMnO4=2K2Mn2O5+3O2↑
10【答案】(1)IO3-+5I-+6CH3COOH=3I2+6CH3COO-+3H2O
(2) KI在潮湿空气里,在阳光的作用下会被空气氧化而产生紫黑色固体(或紫色蒸气),而KIO3不被空气氧化。4I-+O2+2H2O=2I2+4OH-
11.【答案】3I2+6OH-=IO3-+5I-+3H2O S2O32-+4I2+10OH-=2SO42-+8I-+5H2O
S2O32-+2H+=SO2↑+S↓+H2O 4I-+O2+4H+=2I2+2H2O
12【答案】(1)3MnO2+KClO3+6KOH =3K2MnO4+KCl+3H2O.
(2)3MnO42—+4H+=MnO2↓+2MnO4—+2H2O
(3)由上述两个方程式可知,反应物和生成物的计量关系为:
MnO2→K2MnO4→KMnO4
87 158×
2.5g×80%
x = =2.4g。
(4)2KMnO4+8H2SO4+5Na2C2O4=2MnSO4+K2SO4+10CO2↑+5Na2SO4+8H2O
13.【答案】(1)2 16 3-2 6 6 8 铁 ,6e (2)还原产物Fe3+水解生成Fe(OH)3胶粒,能吸附悬浮杂质而沉积下来。
14.【答案】8:3
新信息化学方程式的书写练习答案
1.⑴Cu + H2O2 + 2H+ == Cu2+ + 2H2O 2. 2MnO4-+5SO32-+6H+=2Mn2++5SO42-+4H+
3. SO2+2CO=S+2CO2(500℃、催化剂) 4. 3Cl2+NaI+6NaOH==NaIO3+6NaCl+3H2O
5.制N2的化学方程式为NH4Cl+NaNO2=NaCl+2H2O+N2↑
6.(1)14HNO3+3Cu2O→6Cu(NO3)2+2NO↑+7H2O
(2)酸性 氧化性 (3)0.6mol (4)使用了较浓的硝酸,产物中有部分NO2生成
7.⑴Cu + H2O2 + H2SO4 == CuSO4 + 2H2O ⑵4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O 2Fe3+ + 2I— == 2Fe2+ + I2
⑶10KOH + 3Cl2 + 2Fe(OH)3 == 2K2FeO4 + 6KCl + 8H2O
8.①2MnO2+4KOH+O2==2K2MnO4+2H2O ②产生无色气泡
9.A. 2H++2e—=H2↑ ②2Fe(OH)3+3ClO-+4OH-==2FeO4-+3Cl-+5H2O
B. 4FeO42- + 20 H+ = 4Fe3+ + 3O2↑+10H2O C. 
10.答案:2CN-+8OH-+5Cl2=2CO2+N2+10Cl-+4H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe2++7H2O


2I-+2H++O3=I2+O2+H2O 4FeO42- + 20 H+ = 4Fe3+ + 3O2↑+10H2O
方法三:  1:1
1:1
(2)使反应正常进行,并防止温度过高引起爆炸。温度计。
(3)②
(4)5H2S+8ClO2+4H2O=5SO42—+8Cl—+18H+
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳(氧化还原反应中的概念与规律;氧化还原反应的表示方法及配平。)氧化还原反应中的概念与规律:一、五对概念在氧化…
-
高中化学知识点总结氧化还原反应
燕园教育教师培训手册三氧化还原反应1准确理解氧化还原反应的概念11氧化还原反应各概念之间的关系1反应类型氧化反应物质所含元素化合价…
-
氧化还原反应知识点总结
一氧化还原基本概念1四组重要概念间的关系1氧化还原反应凡是反应过程中有元素化合价变化或电子转移的化学变化叫氧化还原反应氧化还原反应…
-
高一化学之三 氧化还原反应知识点总结
714氧化还原反应知识点一概念氧化还原反应的实质电子的转移电子的得失或共用电子对的偏移口诀失电子化合价升高被氧化氧化反应还原剂得电…
-
氧化还原反应知识点总结
专题四氧化还原反应一氧化还原反应的基本概念1基本概念略氧化还原反应氧化反应还原反应氧化剂还原剂等2知识体系3常见氧化剂1活泼非金属…
-
氧化还原反应知识点总结
一氧化还原基本概念1四组重要概念间的关系1氧化还原反应凡是反应过程中有元素化合价变化或电子转移的化学变化叫氧化还原反应氧化还原反应…
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳一、概念1、氧化反应:元素化合价升高的反应还原反应:元素化合价降低的反应氧化还原反应:凡有元素化合价升降的化…
-
氧化还原反应知识点归纳
氧化还原反应知识点归纳(氧化还原反应中的概念与规律;氧化还原反应的表示方法及配平。)氧化还原反应中的概念与规律:一、五对概念在氧化…
-
氧化还原反应知识点总结
专题四氧化还原反应一氧化还原反应的基本概念1基本概念略氧化还原反应氧化反应还原反应氧化剂还原剂等2知识体系3常见氧化剂1活泼非金属…
-
氧化还原反应知识点总结
一氧化还原基本概念1原反应氧化还原反应的特征元素化合价的升降氧化还原反应的实质电子转移2氧化反应和还原反应在氧化还原反应中反应物所…