第二章 《化学物质及其变化》:2.3《氧化还原反应》教案+随堂练习(新人教版必修1)
第三节 氧化还原反应
(第一课时)
教学目标:
1.初步学会根据化合价变化分析、判断、理解氧化还原反应
2.通过氧化还原反应概念的学习,培养学生准确描述概念、比较辨析概念的能力

 3.通过氧化还原反应概念的演变,培养学生用发展的观点、科学的态度,勇于探索的品质学习化学,并对学生进行对立统一的辩证唯物主义教育
3.通过氧化还原反应概念的演变,培养学生用发展的观点、科学的态度,勇于探索的品质学习化学,并对学生进行对立统一的辩证唯物主义教育
教学重点、难点
重点:用化合价变化的观点理解氧化还原反应等概念
难点:用化合价变化的观点理解氧化还原反应等概念
教学过程

巩固练习:
1.下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A.Fe+CuSO4=FeSO4+Cu
B.Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
C.AgNO3+NaCl=AgCl↓+NaNO3
D.2KMnO4 K2MnO4 +MnO2 +O2↑
K2MnO4 +MnO2 +O2↑
2.下列属于氧化还原反应的是( )
A.CaCO3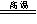 CaO+CO2↑
CaO+CO2↑
B.Na2O+H2O=2NaOH
C.Na2CO3+H2SO4=.Na2SO4+CO2↑+H2O
D.MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
3.下列变化需要加入氧化剂才能实现的是( )
A.NaOH→NaCl B. H2SO4→H2 C. HCl→Cl2 D. CaCO3→CO2
4.在下列反应中,水既不作氧化剂,又不作还原剂的是( )
A.2Na+2H2O=2NaOH+H2↑ B. Na2O=2NaOH
C. H2O H2↑+O2↑ D.C+H2O
H2↑+O2↑ D.C+H2O CO+H2
CO+H2
5.下列变化过程一定属于还原反应的是( )
A. HCl→MgCl2 B. Na→Na+ C.CO→CO2 D.Fe3+→Fe2+
6.下列反应氯元素只被氧化的是( )
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.MnO2+4HCl MnCl2+Cl2↑+H2O
MnCl2+Cl2↑+H2O
C.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2 +2H2O
D.2HClO 2HCl+O2↑
2HCl+O2↑
7.分析下列氧化还原反应中化合价的变化,指出氧化剂和还原剂
(1)2Fe+3Cl2 2FeCl3 氧化剂_________ 还原剂___________
2FeCl3 氧化剂_________ 还原剂___________
(2) CuO+CO Cu+CO2 氧化剂_________ 还原剂___________
Cu+CO2 氧化剂_________ 还原剂___________
 (3)2Al+3H2SO4=Al2(SO4)3+3H2↑ 氧化剂_________ 还原剂___________
(3)2Al+3H2SO4=Al2(SO4)3+3H2↑ 氧化剂_________ 还原剂___________
(4) 2KClO3 2KCl+3O2↑ 氧化剂_________ 还原剂___________
2KCl+3O2↑ 氧化剂_________ 还原剂___________
备课参考
1. 练习答案:1.B 2.D 3.C 4.B 5.D 6.B 7.(1)Cl2 Fe (2) CuO CO
(3)H2SO4 Al (4) KClO3 KClO3
2. 资料选用:氧化还原反应在工农业生产、科学技术和日常生活中的意义
我们所需要的各种各样的金属,都是通过氧化还原反应从矿石中提炼而得到的。如制造活泼的有色金属要用电解或置换的方法;制造黑色金属和别的有色金属都是在高温条件下用还原的方法;制备贵重金属常用湿法还原,等等。许多重要化工部的制造,如合成氨、合成盐酸、接触法制硫酸、氨气体法制硝酸、食盐水电解制烧碱等等,主要反应也是氧化还原反应。石油化工里的催化去氢、催化加氢、链烃氧化制羧酸、环氧树脂的合成等等也都是氧化还原反应。
在农业生产中,植物的光合作用、呼吸作用是复杂的氧化还原反应。施入土壤的肥料的变化,如铵态转化为硝态氨,SO42-转化为H2S等,虽然需要有细菌起作用,但就其实质来说了,也是氧化还原反应。土壤里铁或锰的氧化态的变化直接影响着作物的营养,晒田和灌田主要就是为了控制土壤里的氧化还原反应的进行。
我们通常应用的干电池、蓄电池以及在窨技术上应用的高能电池都发生着氧化还原反应,否则就不可能 把化学能转变为电能、把电能转变成化学能。
人和动物的呼吸,把葡萄糖氧化为二氧化碳和水。通过呼吸把储藏在食物的分子内的能,转变为存在于三磷酸腺苷(ATP)的高能磷酸键的化学能,这种化学能再供给人和动物进行机械运动、维持体温、合成代谢、细胞的主动运输等所需要的能量。煤、石油、天然气等燃料的燃烧更是供给人们生活和生产所必需的大量的热。
由此可见,在许多领域里都涉及到氧化还原反应,我们引导学生学习和逐步掌握氧化还原反应对于他们今后参加生产、走向社会等都是有意义的。w.w.w.k.s.5.u.c.o.m
www.ks5u.com
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
第二篇:高一化学化学反应总结【必修一、二(苏教版)】
高一化学化学反应总结
1、钠在空气中燃烧(黄色的火焰) 2Na+O2 Na2O在空气中加热(变黄) 2Na2O+O22、钠与水反应(浮、熔、游、消、变)
2Na + 2H2O =2NaOH+H2 ↑ 2Na+2H2O=2Na+2OH +H2 ↑ 3、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白)
2Na2O2+2H2O=4NaOH+O2↑ 改写成: 2Na2O2+2H2O=4Na+4OH +O2↑ 碱性氧化物Na2O与水的反应 Na2O+H2O=2NaOH
4、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源原因是:2Na2O2+2CO2=2Na2CO3+O2 5、苏打(纯碱)与盐酸反应 ①盐酸中滴加纯碱溶液
Na2CO3+2HCl=2NaCl+H2O+CO2↑ 改写成:CO3+2H=H2O+CO2↑
②纯碱溶液中滴加盐酸,至过量Na2CO3+HCl=NaHCO3+NaCl,改写成:CO3+H=HCO3
NaHCO3+HCl=NaCl+H2O+CO2↑改写成:HCO3+H=H2O+CO2↑6、小苏打受热分解 2NaHCO3
NaHCO3+ NaOH
△
-
+
2-
+
-
2-
+
+
-
+
-
Na2O2
△
钠块在空气中变暗 4Na+O2=2Na2O
2Na2O2
△
2CO3+H2O+CO2 ↑
-
-
2-
7、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热
Na2CO3 + H2O 溶液中:HCO3+OH = H2O + CO3
点燃
8、氯气的性质:
铜丝在氯气中剧烈燃烧(棕色烟)Cu+Cl2
CuCl2 溶于水成绿色溶液
Cl2+2FeCl2 =2FeCl3 Cl2+2NaBr=2NaCl+Br2 Cl2 +2NaI =2NaCl+I2
点燃
2NaCl Cl2+SO2+2H2O=H2SO4+2HCl 2Na+Cl2
点燃
9、铁在氯气中剧烈燃烧 2Fe+3Cl22FeCl3(棕色烟)溶液为黄色
点燃
10、氢气在氯气中燃烧(苍白色火焰) H2+Cl22HCl 11、氯气溶于水(新制氯水中含H 、Cl 、ClO 、OH、Cl2、HClO、H2O)
Cl2+H2O=HCl+HClO改写成:Cl2+H2O=H+Cl+HClO
12、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)+ O2↑ 13、工业制漂白粉的原理2Ca(OH)2 + 2Cl2 =Ca(ClO)2 + CaCl2 + 2H2O
漂白粉的失效Ca(ClO)2+CO2+H2O=CaCO3↓++ O2↑ (若在溶液中)Ca+2ClO+CO2+H2O=CaCO3↓+ 2HClO 14、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶)
MnO2+4HCl(浓)2H2O
15、新制氯水注入盛溴化钠溶液的试管中Cl2+2NaBr=Br2+2NaCl改写成:Cl2+2Br=Br2+2Cl
16、铁与硫加热反应 Fe+S
FeS, 铁与氧气加热反应 3Fe+2O2Fe3O4
高温
17、工业制单质硅(碳在高温下还原二氧化硅) SiO2+2CSi+2CO↑
18、二氧化硅与氢氧化钠反应SiO2+2NaOH=Na2SiO3+H2O改写成:SiO2+2OH=SiO3+H2O 19、Al、Fe遇浓HNO3、浓硫酸钝化(常温)
-2---2+
-
+
-+
-
-
-
光照
光照
MnCl2+Cl2↑+2H2O改写成:MnO2 +4H+2Cl
+-
Mn+Cl2↑+
2+
20. 铝箔在氧气中剧烈燃烧 4Al+3O2
点燃
2Al2O3
+
3+
21. 铝片与稀盐酸反应2Al+6HCl=2AlCl3+3H2↑改写成:2Al+6H=2Al+3H2↑ 22. 铝与氢氧化钠溶液反应
2Al+2NaOH +2H2O= 2NaAlO2+3H2↑改写成:2Al+2OH+2H2O=2AlO2+3H2↑
高温
23. 铝与三氧化二铁高温下反应(铝热反应) 2Al+Fe2O32Fe+Al2O3
点燃
24. 镁在二氧化碳中燃烧 2Mg+CO22MgO+C
--
25. 氧化铝溶于氢氧化钠溶液
Al2O3 + 2NaOH 错误!未找到引用源。 2NaAlO2 +H2O, Al2O3 + 2OH = 2AlO2 + H2O
26. 硫酸铝溶液中滴过量氨水
Al2(SO4)3+6NH3·H2O错误!未找到引用源。2Al(OH)3↓+(NH4)2SO4改写成:Al+
3+
+3NH3·H2O=Al(OH)3↓+3NH4
-
-
27. ①氢氧化铝溶液中加盐酸
Al(OH)3+3HCl=AlCl3+3H2O改写成:Al(OH)3+3H=Al+3H2O
+
3+
②Al(OH)3与NaOH溶液反应
Al(OH)3+NaOH 错误!未找到引用源。 NaAlO2+2H2O Al(OH)3+OH- =AlO2-+2 H2O
高温
28. 高温下铁与水反应 3Fe+4H2O(g)Fe3O4+4H2 29. 铁与盐酸反应 Fe+2HCl=FeCl2+H2↑改写成:Fe+2H=Fe+H2↑
+
2+
30. 氧化铁溶于盐酸中 Fe2O3+6HCl=2FeCl3+3H2O改写成:Fe2O3+6H=2Fe+3H2O
+
3+
31. 氯化铁中滴入氢氧化钠溶液(红褐色沉淀)
FeCl3+3NaOH=Fe(OH)3↓+3NaCl改写成:Fe+3OH =Fe(OH)3↓
3+
-
32. 氢氧化亚铁在空气中被氧化(白色沉淀变为红褐色沉淀)4Fe(OH)2+O2+2H2O=4Fe(OH)3 33. 氯化亚铁溶液中通入氯气2FeCl2+Cl2=2FeCl3改写成:2Fe+Cl2=2Fe+2Cl-
2+
3+
34. 氯化铁溶液中加入铁粉2FeCl3+Fe=3FeCl2 改写成:2Fe+Fe=3Fe
3+2+
35 用KSCN检验的存在离子方程式 Fe+3SCN-= Fe (SCN)3 36、铜与浓硫酸反应: Cu+2H2SO4 (浓)37、碳与浓硫酸反应:C+2H2SO4(浓)
3+
CuSO4 +2H2O+SO2 ↑
2H2O+CO2↑+2SO2↑
38、SO2+CaO =CaSO3
-2-39、SO2+2NaOH=Na2SO3+H2O改写成:SO2+2OH=SO3+H2O
2+ -40、SO2 + Ca(OH)2 = CaSO3↓ + H2O改写成:SO2 + Ca+ 2OH = CaSO3↓+H2O + -2-41、SO2+ Cl2+2H2O=2HCl + H2SO4改写成:SO2+Cl2+2H2O=4H+2Cl +SO4
42、SO2+2H2S =3S+ 2H2O
-
对氧化还原反应教学反思
对氧化还原反应的教学反思南沙中学冼瑞熔氧化还原反应理论是中学化学的重要理论如何才能使学生从初中对氧化还原反应的肤浅认识提升到构建氧…
-
《氧化还原反应》教学反思
氧化还原反应教学反思氧化还原反应是高中化学必修1第二章化学物质及其变化中的第三节有其重要的意义因为在中学阶段的基本概念基础理论知识…
-
《氧化还原反应》教学设计及反思
氧化还原反应教学设计昌吉州二中化学组吕玲英一教材分析11教材的地位与作用氧化还原反应是高中化学基本理论的重要内容之一本章内容是日常…
-
氧化还原反应教学反思
教学反思我选择的这节课属于化学基本概念的教学目的是让学生感知在学习过程中要正确恰当地看待概念的形成和发展教学过程以从学生已有的初中…
-
氧化还原反应教案及教学反思
第二章第三节氧化还原反应教案教材分析氧化还原反应是日常生活工农业生产和现代科技中经常遇到的一类重要的化学反应它贯穿中学化学学习的全…
-
高中化学知识点总结氧化还原反应
燕园教育教师培训手册三氧化还原反应1准确理解氧化还原反应的概念11氧化还原反应各概念之间的关系1反应类型氧化反应物质所含元素化合价…
-
高一化学氧化还原反应经典总结
氧化还原反应1从得失氧的角度认识氧化还原反应根据反应物中物质是否得到氧或者失去氧将化学反应分为氧化反应和还原反应注氧化反应和还原反…
-
高一化学之三 氧化还原反应知识点总结
714氧化还原反应知识点一概念氧化还原反应的实质电子的转移电子的得失或共用电子对的偏移口诀失电子化合价升高被氧化氧化反应还原剂得电…
-
北京四中高中化学 2.3氧化还原反应(2)教案 新人教版必修1
氧化还原反应121有单质参加的化合反应和有单质生成的分解反应一定是氯化还原反应2没有单质参加的化合反应和没有单质生成的分解反应一定…
-
高中化学氧化还原反应归纳
氧化还原反应考情直播例120xx茂名一模金属钛Ti性能优越被称为继铁铝制后的第三金属工业上以金红石为原料制取Ti的反应为aTiO2…
-
氧化还原反应知识点总结
一氧化还原基本概念1四组重要概念间的关系1氧化还原反应凡是反应过程中有元素化合价变化或电子转移的化学变化叫氧化还原反应氧化还原反应…