实验报告:脉冲塔萃取

实验报告
课程名称: 过程工程控制甲(Ⅱ)实验 同组实验者: 指导老师: 成绩 实验名称: 脉冲塔萃取操作及体积传质系数测定
一.实验目的和要求
1、了解脉冲萃取实验装置及萃取操作。
2、观察脉冲强度(脉冲幅度或脉冲频率)变化时,萃取塔内轻、重两相流动状况,了解萃取
操作的主要影响因素,研究萃取操作条件对萃取过程的影响。
3、测量每米萃取高度的传质单元数、传质单元高度和体积传质系数KYV,关联传质单元高度与脉冲萃取过程操作变量的关系。
4、计算萃取率η。
二、实验内容和原理 萃取是分离和提纯物质的重要单元操作之一,是利用混合物中各个组分在外加溶剂中的溶解度的差异而实现组分分离的单元操作。进行液-液萃取时,两种液体在塔内作逆流流动,
其中一种液体作为分散相,以液滴形式通过另一作为连续相的液体,两种液相的浓度则在设
备内作微分式的连续变化,并依靠密度差在塔的两端实现两夜相间的分离。当轻相作为分散
相时,相界面出现在塔的上端;反之,当重相作为分散相时,则相界面在塔的下端。
1.萃取的基本符号
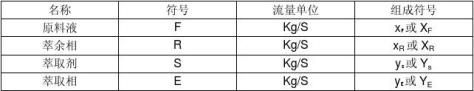
2.萃取的物料衡算
萃取计算中各项组成可用操作线方程相关联,操作线方程的P(XR,YS)h和点Q(XF,YE)

与装置的上下部相对应。
在第一溶剂B与萃取剂S完全不互溶时,萃取过程的操作线在X-Y坐标上时直线,其方程式如下形式: YE?YSY?YS?X?XRX?XR ————————————————(1) F
由上式得:
Y?Y?m?X?X? SS
其中: m?YE?YS
XF?XR
单位时间内从第一溶剂中萃取出的纯物质A的量M,可由物料衡算确定:
M?B?X?X??S?Y?Y? ——————————————(2) FRES
3、萃取过程的质量传递
不平衡的萃取相与萃余相在塔的任一截面上接触,两相之间发生质量传递。物质A以扩散的方式由萃余相进入萃取相,该过程的界限是达到相间平衡,相平衡的相间关系为:
Y*?kX ————————————————————(3)
k为分配系数,只有在较简单体系中,k才是常数,一般情况下均为变数。本实验已给出平衡数据,见附表。
与平衡组成的偏差程度是传质过程的推动力,可用操作线与平衡线之间的线段来表示,在装置的顶部,推动力是:
?Y?Y*?Y —————————————————(4) RRS
在塔的下部是: ?Y?Y*?Y —————————————————(5) FFE
传质过程的平均推动力,在操作线和平衡线为直线的条件下为: ?Y??YF??YR ———————————————(6) m
ln?YF
?YR
物质A由萃余相进入萃取相的过程的传质动力学方程式为:
M?KYA?Ym ———————————————————(7)
式中:K——单位相接触面积的传质系数,kg/m2?s?kg/kg?; Y
A——相接触表面积,m2。
该方程式中的萃取塔内相接触表面积A不能确定,因此通常采用另一种方式。 相接触表面积A可以表示为:
A?aV?a?h ———————————————————(8) 式中:a——相接触比表面积,m2/m3;
V——萃取塔有效操作段体积,m3;
?——萃取塔横截面积,m2;
h——萃取塔操作部分高度,m。
这时, M?KaV?Y?KV?Y —————————————————(9) YmYVm
式中:KYV?KYa——体积传质系数,kg/m3?s?kg/kg?。
根据(2)、(7)、(8)和(9)式,可得
h?
在该方程中: YE?YS?HOE?NOE ———————————————(10) KYV??YmS?
HOE?S
KYV?,称为传质单元高度; NOE?YE?YS,称为总传质单元数。
?Ym
KY、KYV、HOE是表征质量交换过程特性的,KY、KYV越大,HOE越小,则萃取过程进行的越快。
KYV?
4.萃取率 η S?YE?YS? —————————————————(11) M?V?YmV?Ym
??被萃取剂萃取的组分A的量?100%
原料液中组分A的量
??S?YE?YS??100% ————————————————(12)
BXF
??或 ??B?XF?XR??100%??1?XR??100% ———————(13) ??BXF?XF?
5.数据处理中应注意的问题
(1)第一溶剂B的质量流量
B?F?1?x??V??1?x? ——————————————(14) FFFF
式中:V——料液的体积流量,m3/h; F
?——料液的密度,kg/m3; F
x——料液中A的含量,kg/kg。 F
?由比重计测量而得。VF由下式计算: VF?VN?0?f??F?0 —————————————(15) ?VN?F?f??0?F
式中:V——转子流量计读数,ml/min或m3/h; N
?——转子密度,kg/m3; f
?——20 ℃时水的密度,kg/m3。 0
B?VN
(2)萃取剂S的质量流量 0F?1?xF? ————————————————(16)
因为萃取剂为水,所以
S?V’ ————————————————(17) N?0’
(3)原料液及萃余液的组成x、x FR
对于煤油、苯甲酸、水体系,采用酸碱中和滴定的方法可测定进料液组成xF、萃余相组成xR和萃取相组成yE,即苯甲酸的质量分率,yE也可通过如上的物料衡算而得,具体步骤如下: 用移液管取试样V1ml,加指示剂1-2滴,用浓度为Nb的KOH溶液滴定至终点,如用去KOH溶液V2ml,则试样中苯甲酸的摩尔浓度Na为:
N?V2Nb —————————————————(18) aV1
则 x?NaMA —————————————————(19) F?F
式中:M——溶质A的分子量,g/mol,本实验中苯甲酸的分子量为122g/mol; A
?——溶液密度,g/l 。 F
x亦用同样的方法测定: R
xR?Na'Ma ——————————————————(20)
?R
式中: N'?V2'Nb ——————————————————(21) aV1'
其中:V'、V'——分别为试样的体积数与滴定所耗的KOH溶液的体积数。 12
四、 操作方法和实验步骤
1.打开设备除脉冲转向器之外的所有电源开关。
2.调节萃取剂和原料液的流量均为200ml/min,取原料液10ml用于酸碱滴定测定原料中苯甲酸含量。另取3/4试管的原料液测定比重,测定完成的原料液可倒回原料槽中。
3.不断调节萃取液出口阀门,使油、水相分界面控制在萃取剂与萃余液出口之间,并保持在此期间萃取剂和原料液的流量基本不变。
4.待稳定后,取萃余液10ml用于酸碱滴定测定萃取后的苯甲酸含量。另取3/4试管的萃余液测定比重。
5.打开离心泵、脉冲转向器电机。调节脉冲流量调节阀,得到一个较小的脉冲频率。
6.保持萃取剂和原料液的流量为200ml/min不变。不断调节萃取液出口阀门,使油、水相分界面控制在萃取剂与萃余液出口之间。
7.待稳定后,取萃余液10ml用于酸碱滴定测定萃取后的苯甲酸含量。另取3/4试管的萃余液测定比重。
8.调节脉冲流量调节阀,得到一个相对较大的脉冲频率。
9.保持萃取剂和原料液的流量为200ml/min不变。不断调节萃取液出口阀门,使油、水相分界面控制在萃取剂与萃余液出口之间。
10.待稳定后,取萃余液10ml用于酸碱滴定测定萃取后的苯甲酸含量。另取3/4试管的萃余液
测定比重。
11.实验结束后,关闭塔设备电源并清洗仪器。
五、实验装置
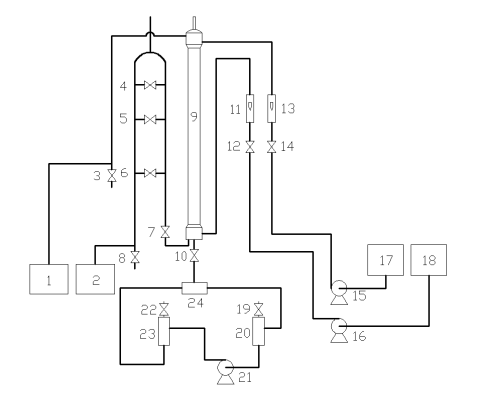


图1 萃取实验装置流程示意图
六.数据记录和处理
1.原始数据
表一 原始数据记录表
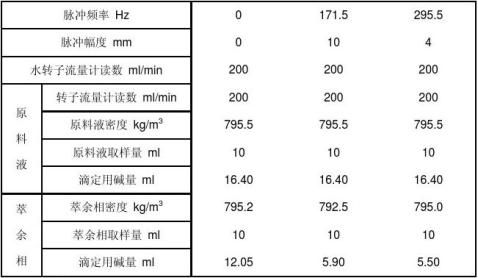
2.实验数据处理
(1)原料液的浓度及质量流量
原料液和萃取剂在实验过程中是保持不变的,因此提出列在下方。又20摄氏度下水的密度为998.2kg/m3;实验条件下料液密度近似为测得的比重值,即795.5kg/m3。 a.xF及XF
原料液中苯甲酸的摩尔浓度:
N?V2Nb?16.40?0.01?0.0164mol/l
a
V1
10
原料液组成摩尔分数:
xF?
NaMA
?F
?
0.0164?122
?2.515?10?3
795.5
摩尔比XF
XF?
x?2.521?10-3
1?xF
与XF相平衡的YF*
由图二得到平衡线的拟合公式:
2
-771.892?2(x?4.46651)。
y?0.245414 ? e
2.38862.3886/2
将XF=2.521*10-3 代入公式,得出YF*=1.056*10-2 b.原料液的质量流量 料液的质量流量:
B?V
N
??
200?60
?1?x???FF6
10
998.2?795.5?(1-2.515?10-3)?10.67kg/h
c.萃取剂水的质量流量
S?V’?’?
N0
200?60
?998.2?11.98kg/h 10d.萃取塔有效段操作体积
1
V?h???0.7???0.052?1.374?10?3
4
(2)其余
表二 数据处理表
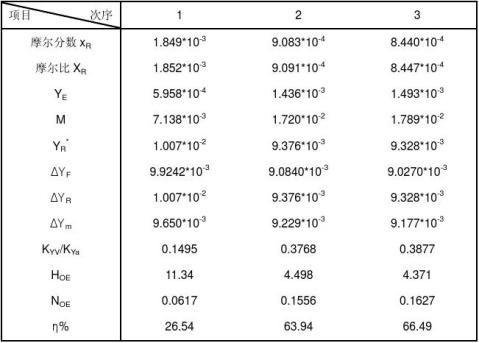
计算过程(以第一组为例): a.萃余液组成xR及XR
Na'?V2'Nb12.05?0.01??0.01205mol/l
V1'10
N'M0.01205?122x???1.849?10-3 R?795.2R
XR?x?1.852?10?3
1?xR
b.萃取液组成YE及M(溶剂为纯水,YS=0)
YE?B10.67(XF?XR)??(2.521?10?3?1.852?10?3)?5.958?10?4
S11.98
M?BX?X?10.67?(2.521?10?3?1.852?10?3)?7.138?10?3 FR??
C.YR*
2-3(1.852??4.46651)10-771.892?2y?0.245414 ? ?0.01007 e22.38862.3886/2
c.塔底塔顶推动力ΔYF、ΔYR、ΔYm
?Y?Y*?Y?1.007?10-2-0?1.007?10-2 RRS
?Y?Y*?Y?1.052?10-2-5.958?10-4?9.9242?10-3 FFE
?Y??Y?0.009242-0.01007?9.650??3 ?Y?10mlnln0.01007?YR
d.体积传质系数、传质单元高度和总传质单元数
M7.138?10-3Ka?K???0.1495kg/m3?s(kg/kg)YYVV?Ym1.374?10?9.650?10?3600
HOE?S
K?YV?4?11.980.1495?3600???0.052
?4?11.34
NOEY?YS5.958??0?E??0.0617 ?3?Ym9.650?10
?X?1.852?10-3????1??100%?(1-)?100%?26.54% ?X?-32.521?10F??
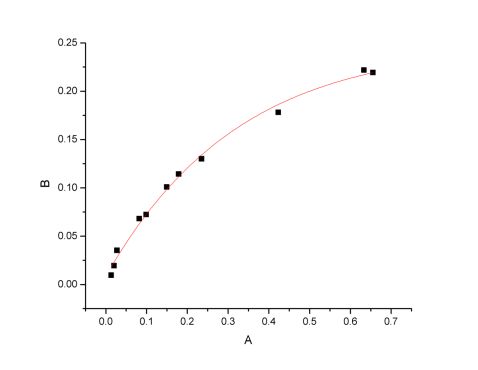
图2 平衡线图
七.实验讨论
1.脉冲的影响
在脉冲塔中,当脉冲从无到有时,传质单元高度迅速减小,萃取率大大增加。当在有脉冲的前提下,由于总的能量大体维持不变,所以增大脉冲,萃取效率的变化不明显。
有脉冲存在时,填料塔内的液体产生一个附加的脉冲运动,塔内液体不断地与填料接触,是分散相的液滴细化,滴径变小的同时,界面更新速度加快,传质效果变好。因此有脉冲能量加入后,液体传质过程得到强化,萃取相传质单元高度变小,由于填料层高度一定,传质单元数增加。
2.误差分析
A.滴定过程中,由于试样是油相,滴定液是水相,彼此并不完全相容,滴定时很容易过量。虽然实验条件设定时,将试样改为两个油相,尽量减少滴定时的误差,但是不能避免。
B.滴定中终点判断误差、读数误差,移液管量取液体时的误差等等。
C.取样滴定时萃取并未完全稳定。
D.实验设备的系统误差
E.转子流量计和脉冲器不稳定,在实验过程中不断波动。
F.试剂的密度只是用比重计测定,并不精确。而且实验中我们没有测定水相的密度,在计算中用20摄氏度的水密度代替。
八.思考题
1、请分析比较萃取实验装置与吸收、精馏实验装置的异同点?
萃取实验装置与吸收、精馏实验装置都是基于传质理论建造的设备。
三种实验装置的共同点是塔设备为主要设备,均有进料和出料口,均可以使物料在塔内物理分离。
不同点是精馏设备的有一个进料位置,通常在塔体上;萃取和吸收有两个进料位置,通常一上一下,吸收时气相从塔底进入,液相从塔顶流下;萃取时重相从塔顶进入,轻相从塔底进入。精馏塔需要加热设备,为了强化传质效果萃取实验装置有转盘或脉冲发生器,吸收实验装置仅仅是利用普通的塔设备。
2、说说本萃取实验装置的(或脉冲幅度)是如何调节和测量的?从实验结果分析脉冲强度变化对萃取传质系数与萃取率的影响。
脉冲频率是通过调节脉冲转向器电机上的旋钮来调节,控制面板上的数字显示即为脉冲频率。该实验中的脉冲器是一个十字转盘,且与离心泵相连。通过旋钮调节离心泵的功率,从而调节十字转盘的转动速度,进而调节形成的脉冲频率。又由于脉冲发生器的功率一定,脉冲幅度与脉冲频率成反比,可通过调节脉冲频率间接调节脉冲幅度。测量时,利用方格纸,读出油水相分界面的振幅即为脉冲幅度。实验结果表明,当脉冲从无到有的时候,脉冲对实验影响很大,体积传质系数和萃取率明显增大。但在此前提下,再次增大脉冲后,由于脉冲的能量一定,脉冲对实验影响很小,萃取率和体积传质系数有提高,但幅度很小。
3、测定原料液、萃取相、萃余相组成可用哪些方法?采用中和滴定时,标准碱为什么选用甲醇为溶剂,而不是水?
酸碱中和滴定法、色谱分析仪分析法。
滴定时,试样为油相,滴定液呈水相,彼此不相容,很容易产生误差。而甲醇在水相中和油相中的溶解度都很大,能够增大标准碱在油相中的溶解度,尽量减少误差。
4、萃取过程是否会发生液泛,如何判断液泛?
可能。因为对于直径一定的萃取塔,可供液液两相自由流动的截面是有限的。两相之一的流量如果增大到某个限度,填料塔内的液体不能便不能顺畅的流下,在塔内形成积液,导致液泛。液泛时,塔内液体不能顺利流通,滞液率增大;当填料塔内分层界面明显快速上升时,则认为产生了液泛。
第二篇:萃取和分液实验报告
萃取和分液实验报告
一、实验目的:
(1)了解萃取分液的基本原理。
(2)熟练掌握分液漏斗的选择及各项操作。
二、实验原理:
利用某溶质在互不相溶的溶剂中的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,在利用分液的原理和方法将它们分离开来。
三、实验仪器和药品:
药品:碘水、CCl4
器材:分液漏斗、100ml烧杯、带铁圈的铁架台、20ml
四、实验步骤:
1、分液漏斗的选择和检验:验分液漏斗是否漏水,检查完毕将分液漏斗置于铁架台上;
2、振荡萃取:用量筒量取10 ml碘水,倒入分液漏斗,再量取5 ml萃取剂CCl4加入分液漏斗,盖好玻璃塞,振荡、放气;需要重复几次振荡放气。
3、静置分层:将振荡后的分液漏斗放于铁架台上,漏斗下端管口紧靠烧怀内壁;
 4、分液:调整瓶塞凹槽对着瓶颈小孔,使漏斗内外空气相通,轻轻旋动活塞,按“上走上,下走下”的原则分离液体;
4、分液:调整瓶塞凹槽对着瓶颈小孔,使漏斗内外空气相通,轻轻旋动活塞,按“上走上,下走下”的原则分离液体;
五、实验室制备图:(见右图)
六、实验总结(注意事项):
1、分液漏斗一般选择梨形漏斗,需要查漏。方法为:关闭活塞,在漏斗中加少量水,盖好盖子,用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡,看是否漏水。
2、将溶液注入分液漏斗中,溶液总量不超过其容积的3/4;
3、振荡操作要领:右手顶住玻璃塞,左手握住活塞,倒置振荡;振荡过程中要放气2-3次,让分液漏斗仍保持倾斜状态,旋开旋塞,放出蒸气或产生的气体,使内外压力平衡;
4、要及时记录萃取前后的液面情况及颜色变化;振荡前,上层为黄色,下层为无色;振荡静置后,上层为无色(或淡黄色),下层为紫色;
5、萃取剂的选择
a.溶质在萃取剂的溶解度要比在原溶剂(水)大。
b.萃取剂与原溶剂(水)不互溶。
c.萃取剂与溶液不发生发应。
6、按“上走上,下走下”的原则分离液体是为了防止上层液体混带有下层液体。
七、问 题:
1、如果将萃取剂换成苯,实验现象是否相同?使用哪种有机溶剂做萃取剂更好些?为什么?
-
萃取实验报告
实验名称萃取实验一实验目的了解转盘萃取塔的结构和特点掌握液液萃取塔的操作掌握传质单元高度的测定方法并分析外加能量对液液萃取塔传质单…
-
萃取实验报告
实验名称萃取实验一实验目的了解转盘萃取塔的结构和特点掌握液液萃取塔的操作掌握传质单元高度的测定方法并分析外加能量对液液萃取塔传质单…
-
转盘萃取塔实验装置实验指导书
化工原理实验装置系列之转盘萃取塔实验装置实验指导书杭州言实科技有限公司20xx4转盘萃取塔实验装置实验指导书目录一实验目的3二实验…
- 液液萃取实验报告
-
碘水中碘的萃取实验报告
碘水中碘的萃取一实验目的体验从碘水中提取碘单质树立实验环保意识认识各种仪器熟悉和掌握分液漏斗的操作验证萃取的原理二实验原理利用溶解…
-
脉冲塔萃取实验报告
专业姓名实验报告学号日期地点课程名称过程工程原理实验指导老师成绩实验名称脉冲塔萃取实验实验类型同组学生姓名一实验目的和要求必填三主…
-
转盘塔萃取操作及体积传质系数测定实验报告
课程名称:过程工程原理实验指导老师:成绩:_________________实验名称:转盘塔萃取实验实验类型同组学生姓名:_一、实…
-
脉冲塔萃取实验报告
课程名称:过程工程原理实验指导老师:成绩:_______________实验名称:脉冲塔萃取实验实验类型同组学生姓名:一、实验目的…
-
萃取实验报告
北方民族大学学生实验报告院部化学与化学工程姓名郭俊雄学号20xx2995专业化学工程与工艺班级081同组人员林艺明胡鹏秦开勉课程名…
-
化工原理实验报告精馏实验
化工原理实验报告精馏实验精馏实验一目的及任务熟悉精馏的工艺流程掌握精馏实验的操作方法了解板式塔的结构观察塔板上汽液接触状况测定全回…
-
蒸馏、萃取实验报告单
蒸馏萃取实验报告单姓名班级一实验室制取蒸馏水1蒸馏是利用物质沸点的不同加热使液体混合物中的液体变为气体挥发出来再冷凝为液体除去难挥…