阿司匹林的制备实验报告
阿司匹林的制备
实验名称:
班 级:
姓 名:
实 验 报 告
第二篇:阿司匹林的合成
阿司匹林的制备
一、 实验目的:
1、了解阿司匹林制备的反应原理和实验方法。
2、通过阿司匹林制备实验,初步熟悉有机化合物的分离、提纯等方法。
3、巩固称量、溶解、加热、结晶、洗涤、重结晶等基本操作。
4、了解合成中的副产物以及相应的除杂方法。
5、了解阿司匹林合成中可使用的催化剂
二、实验原理:
阿司匹林的合成原理是在催化剂作用下,以醋酐为酰化剂,与水杨酸羟基酰化成酯。传统的合成阿司匹林的催化剂为浓硫酸,它存在如下缺点:
1)收率较低(65%~70%),腐蚀设备,有排酸污染;
2)操作条件要求严格。浓硫酸具有强氧化性,反应要严格控制其加入速度和搅拌速度,否则会导致反应物碳化;
3)粗产品干燥时,由于硫酸分离不完全而导致部分产品氧化,引起产品成色不好;4)产品不能加热干燥,否则产品中残余的浓硫酸会催化乙酰水杨酸水解成水杨酸。
因而寻找一类新的催化活性高、环保型的催化剂来代替质子酸催化合成乙酰水杨酸必要的,改进后的催化剂大体可分为酸性催化剂、碱性催化剂和其他类型催化剂。
酸性催化剂
酸性催化剂催化合成阿司匹林的机理如下:在酸作用下,乙酸酐中羰基碳原子的正电性增强,使乙酸酐中酰基容易向羟基转移形成酯基,即完成乙酰水杨酸的合成。催化剂酸性越强,氢质子流动性越好,越易于催化酯基的生成,但在乙酰水杨酸的合成中,催化剂酸性太强,也会造成水杨酸分子中羧基与另一水杨酸分子中的酚羟基脱水酯化,生成较多的酯聚合副产物。因此,以浓硫酸为催化剂合成阿司匹林的反应为基础,人们对酸性化合物替代浓硫酸为催化剂合成阿司匹林进行了大量研究,取得了可喜成果。酸性催化剂包括路易斯酸、固体酸、有机酸、酸性无机盐、酸性膨润土等。
1、酸性膨润土的催化效果
膨润土是以蒙脱石为主要矿物成分的非金属矿产资源,具备二维通道和大孔分子筛的性质,用酸处理后所得的酸性膨润土催化酯化反应最大优点是收率高,催化剂经热过滤与产品分离后,再经干燥、净化、活化处理,可反复使用,成本低,不污染环境,是一种绿色催化剂,该方法消除了环境污染,产品质量但收率中等。
2、对甲苯磺酸的催化效果
对甲苯磺酸为固体有机酸,经济易得,污染少,收率高,操作方便,具有较好的工业化前景。对甲苯磺酸具有催化活性高,选择性好,操作方便,污染少等显著优点。
3、活性二氧化锡固体酸的催化效果
用微波辐射法制备的活性二氧化锡固体酸为催化剂,85℃下,反应45 min可使阿司匹林收率达到81.6%,产物中酯聚合物的含量较少,所得产品为纯白色,可在干燥箱中加热干燥而且乙酰水杨酸极少水解。活性二氧化锡性质稳定,操作安全,所得产品容易分离,回收的二氧化锡除去少量杂质可重复使用。
4、 NaHSO4催化
用硫酸氢钾催化合成乙酰水杨酸,具有催化剂在反应过程保持固态,反应完毕经热过滤即可与产品分离、不溶于反应体系、易回收等特点,克服了浓硫酸对设备的强腐蚀性、对环境的污染等缺点,符合绿色化学的发展方向,具有工业应用的前景。
碱性化合物
碱性化合物为催化剂基于碱性化合物能与水杨酸反应、能破坏水杨酸分子内氢键、活化水杨酸的羟基机理,许多碱性化合物可以作为催化剂合成阿司匹林。常见的催化剂包括强碱、弱碱和弱酸强碱盐。
1、吡啶催化效果
吡啶催化效果优良,收率高,适合工业化生产,但较易吸水形成共物,形成共沸物,使反应温度较难控制,且反应中产生难闻的气味。反应温度为80℃,反应时间为30min,催化剂用量为5%,试剂摩尔比为1:4.2时产率最高。吡啶作催化剂为水杨酸质量的5%时,产率为80.2%。弱碱性吡啶催化剂合成乙酰水杨酸产率高于浓硫酸催化剂产率。
2、碳酸钠催化微波合成阿司匹林的效果
采用无水碳酸钠作为催化剂以微波合成法合成乙酰水杨酸的实验技术比用浓硫酸作催化剂的加热合成法速度快数10倍,产率和纯度均较高,不污染环境,避免浓硫酸存在造成的设备腐蚀和操作的不安全因素,适合21世纪绿色合成,经济环境可持续发展的要求。
其他类型催化剂
1、 维生素C为催化剂
维生素C是一种内酯类化合物,分子中有一双烯醇结构,呈酸性和还原性,对酯化反应有一定的催化作用,催化效率与温度有关。用维生素C为催化剂催化的该反应,反应速度快,操作简单,催化剂无需回收,反应条件温和,不腐蚀仪器设备,对环境无污染。维生素C是一种常见的维生素类药,价廉易得,以其作为催化剂具有独特的优势,具有一定的工业应用前景。
2、以三氯稀土为催化剂
三氯稀土是一种简单、便宜和易得的Lewis酸,具有可溶性强、可回收再使用、对设备腐蚀轻、无污染等优点,是一种可望用来解决传统Lewis酸造成环境污染问题的环境友好催化剂,符合绿色化学的时代潮流。用三氯稀土作催化剂与用浓硫酸作催化剂效果相当,但同时又克服了浓硫酸作催化剂所具有的腐蚀设备,污染化境的缺点。其中稀土中YCl3的催化效果较好。用三氯稀土作催化剂,其优点在于反应结束分离出产品后,将水溶液蒸干,剩余物可再次用于该反应的催化,采用相同的反应条件,重复利用3次,产率不变,但成本较高。
3、以碳酸钾为催化剂
实验原理:用碳酸钾代替浓硫酸或浓磷酸作催化剂合成阿司匹林。分析及比较:(1)K2CO,作为催化剂合成阿司匹林具有较好的催化效果。克服了浓酸作催化剂时对设备的腐蚀,造成环境污染等缺点。
4、以活性炭固载SnCl4·5H2O为催化剂
通过用活性炭固载SnCl4 · 5H20作为催化剂催化合成阿司匹林。该催化剂具有催化活性高、反应时间短、易分离、无污染的特点,符合绿色生产的要求,且具有较高的实用价值,可代替其它催化剂。其催化效果良好,不仅改善了传统用的催化剂硫酸带来的腐蚀设备,环境污染等缺点,而且比活炭固载A1C1,催化的产率高[1引。该催化剂还可以通过简单的操作便可回收利用,符合绿色生产的要求,具有投入工业生产的价值。
5、强酸树脂环境友好催化
用强酸性阳离子交换树脂作催化剂比传统的浓硫酸作为催化剂合成阿司匹林有更高的收率,且无腐蚀性,不污染环境,反应重现性好强酸性阳离子交换树脂作为一种绿色催化剂催化活性高,后处理简单,可重复利用3次,所得产品结晶色择好。在工业生产中,可简化生产工艺,节省能源最主要的是它可以避免如浓硫酸催化时,对经基苯甲酸的破坏以及引起自身缩合等副反应。
6、以离子液体为催化剂
可使用的离子液体有Brφnsted酸性离子液体[Hmim]BF4、[bmim]HSO4和[bmim]H2PO4,例如采用Br离子液体对阿司匹林的合成有较好的催化作用。产物和离子液体不溶而分层,便于分离, 且离子液体可以重复使用。离子液体不仅是一种绿色溶剂,在反应中还显示出反应速率快,转化率高,反应的选择性高,催化体系可循环重复使用等优点。
阿司匹林的工业制法:
苯酚与二氧化碳在氢氧化钠存在下在高温高压的条件下反应,得到水杨酸二钠盐(Kolbe-Schmidt反应)。反应后加入稀硫酸中和。
加入乙酸酐进行乙酰化,得到阿司匹林。
这是由酚羟基的特殊性质决定,酚羟基很难直接和乙酸发生酯化反应。该反应实际上依然是酯化反应。
阿司匹林的其他合成方法就是以不同的催化剂来催化合成。
本实验采用传统法来合成阿司匹林。水杨酸分子中含羟基(—OH)、羧基(—COOH),具有双官能团。本实验采用以强酸为硫酸作为催化剂,以乙酐为乙酰化试剂,与水杨酸的酚羟基发生酰化作用形成酯。反应如下:
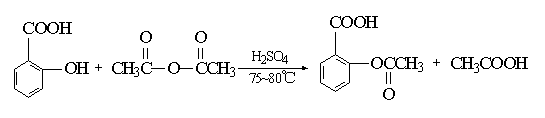
水杨酸 乙酸酐 乙酰水杨酸 乙酸
引入酰基的试剂叫酰化试剂,常用的乙酰化试剂有乙酰氯、乙酐、冰乙酸。本实验选用经济合理而反应较快的乙酐作酰化剂。
副反应有:

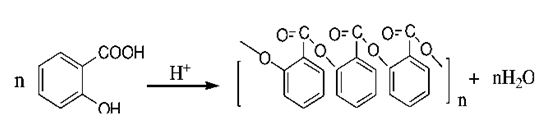
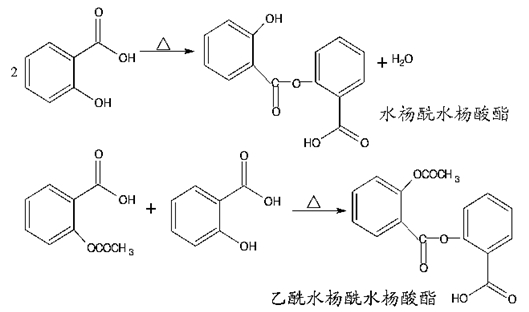
本实验可能产生的副产物有:乙酰水杨酸酐,水杨酸,乙酸苯酯,水杨酸苯酯,乙酰水杨酸苯酯;可能的副反应:原料水杨酸可能带入脱羧产物苯酚和水杨酸苯酯,与原料醋酸酐酸化,生成乙酸苯酯和水杨酸苯酯。另外苯酚和水杨酸苯酯有可反应生成乙酰水杨酸苯酯,三者不溶于碳酸钠。
制备的粗产品不纯,除上面两副产品外,可能还有没有反应的水杨酸等杂质。
本实验用FeCl3检查产品的纯度。杂质中有未反应完酚羟基,遇FeCl3呈紫蓝色。如果在产品中加入一定量的FeCl3,无颜色变化,则认为纯度基本达到要求。
三、主要仪器及试剂
试剂:水杨酸2.00g(0.015mol),乙酸酐5mL(0.053mol),NaHCO3(aq),4mol/L盐酸,浓流酸,冰块,95%乙醇,蒸馏水,1%FeCl3 。
仪器:150mL锥形瓶,5mL吸量管(干燥,附洗耳球),100mL、250mL、500mL烧杯各一只,加热器,橡胶塞,温度计,玻璃棒,布氏漏斗,表面皿, 50mL量筒,烘箱
四、实验步骤
1. 乙酰水杨酸制备
(1)称取水杨酸1.98g于锥形瓶(150mL);在通风条件下用吸量管取乙酸酐3mL,加入锥形瓶,滴入5滴浓流酸,(浓硫酸用量要控制(V<0.2mL),附乙酰水杨酸分解126℃-135℃,水杨酸与乙酐混合后没有及时加硫酸并加热,会发生较多副反应)摇动使固体全部溶解,盖上带玻璃管的胶塞,在事先预热的水浴中加热约10-15min。
水浴装置:500mL烧杯中加100mL水、沸石,用温度计控制85℃-90℃。
(2)取出锥形瓶,将液体转移至250mL烧杯并冷却至室温(可能会没有晶析出)。加入50mL水,同时剧烈搅拌(搅拌要激烈,否则会析出块状物体,影响后续实验),冰水中冷却10min,晶体完全。
(3)抽滤。冷水洗涤几次,尽量抽干,固体转移至表面皿,风干.
2.乙酰水杨酸提纯
(1)粗产品置于100mL烧杯中缓慢加入饱和NaHCO3溶液,产生大量气体,固体大部分溶解。共加入约5mL 饱和NaHCO3(aq)搅拌至无气体产生。
(2)用干净的抽滤瓶抽滤,用5-10mL水洗(可先转移溶液,后洗)。将滤液和洗涤液合并并转移至100mL烧杯中,缓缓加入15mL 4mol/L的盐酸(加入盐酸要滴加,加入过快会导致析出过大的晶粒影响干燥)。边加边搅拌,有大量气泡产生。
(3)用冰水冷却10min后抽滤,2-3mL冷水洗涤几次,抽干。干燥(烘箱55min)。称量(产品秤量理论:2.58g)。
(4)产品纯度检验:取几粒结晶,加5mL水,加少量乙醇增加其解度,滴加1%FeCl3溶液。检验纯度。
(5)杂质的含量是=所得产物的总质量—产品的理论值。
五、实验注意事项及参考数据
1、参考数据:

2、注意事项
1)、实验在通风橱中进行,因为乙酸酐具有强烈刺激性,并注意不要粘在皮肤上。
2)、仪器要全部干燥,药品也要实现经干燥处理。
3)、醋酐要使用新蒸馏的,收集139~140℃的馏分。长时间放置的乙酸酐遇空气中的水,容易分解成乙酸。
4)、要按照书上的顺序加样。否则,如果先加水杨酸和浓硫酸,水杨酸就会被氧化。
5)、水杨酸和乙酸酐最好的比例为1:2或1:3
6)、本实验中要注意控制好温度(85-90℃),否则温度过高将增加副产物的生成,如水杨酰水杨酸、乙酰水杨酰水杨酸、乙酰水杨酸酐等。
7)、 将反应液转移到水中时,要充分搅拌,将大的固体颗粒搅碎,以防重结晶时不易溶解。
-
阿司匹林的合成实验报告
阿司匹林的合成高分子113班09一实验原理阿司匹林为解镇痛药用于治疗伤风感冒头痛发烧神经痛关节痛及风湿病等近年来又证明它具有抑制血…
- 阿司匹林的制备实验报告
- 阿司匹林的制备实验报告
-
阿司匹林实验报告
综合实验报告题目阿司匹林的合成表征及含量测定班徳忠姓专业班级工业分析2学号0806060213同组者蔡召志指导教师万其进喻20xx…
-
实验报告 阿司匹林的合成
阿司匹林的合成一实验目的通过阿司匹林的合成掌握酯化反应和精制原理及基本操作熟悉药物合成实验装置的安装和使用掌握水杨酸的限量检查方法…
-
实验七 阿司匹林片的制备
试验七片剂第一部分片剂制备与部分质量检查一实验目的1通过阿司匹林片剂制备掌握湿法制粒压片的工艺过程2了解单冲与11冲压片机的基本构…
-
有关阿司匹林制法的开放实验报告
开放实验总结报告学生姓名班级学号所在院系开放实验室名称日期北京理工大学实验室设备处制一实验项目概况二实验项目技术报告于氢氧化碱溶液…
-
阿司匹林的合成实验报告
阿司匹林的合成高分子113班09一实验原理阿司匹林为解镇痛药用于治疗伤风感冒头痛发烧神经痛关节痛及风湿病等近年来又证明它具有抑制血…
-
阿司匹林湿法制粒压片及含量测定实验报告
阿司匹林颗粒剂的制备及含量测定学生姓名专业班级指导教师阿司匹林Aspirin又名乙酰水杨酸醋柳酸AcetylsalicylicAc…
-
阿司匹林20xx(实验室版实验报告)
阿司匹林合成论文阿司匹林合成摘要通过该项实验可以使同学们掌握有机物质分离提纯的方法了解乙酰水杨酸的化学性质乙酰水杨酸俗名阿司匹林又…
- 阿司匹林的制备实验报告