乙苯脱氢制苯乙烯实验报告 浙大化工
实验报告
课程名称: 化工专业实验 指导老师: 王晓钟 成绩:__________________
实验名称: 乙苯脱氢制苯乙烯 实验类型: 同组学生姓名:
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、实验材料与试剂(必填) 四、实验器材与仪器(必填)
五、操作方法和实验步骤(必填) 六、实验数据记录和处理
七、实验结果与分析(必填) 八、讨论、心得
一、实验目的
1.了解以乙苯为原料,氧化铁为催化剂,在固定床单管反应器种制备苯乙烯的过程;
2.学会使用化学工艺类实验中温度控制和流量控制的仪表、仪器;
3.学会稳定工艺操作条件的方法。
二、实验原理
1.本实验的主副反应
主反应:




 -CH2-CH3 _—CH=CH2 + H2 117.8KJ/mol
-CH2-CH3 _—CH=CH2 + H2 117.8KJ/mol
副反应:




 -C2H5 +C2H4 105KJ/mol
-C2H5 +C2H4 105KJ/mol




 -C2H5+H2 +C2H6 -31.5KJ/mol
-C2H5+H2 +C2H6 -31.5KJ/mol




 -C2H5+H2 -CH3+CH4 -54.4KJ/mol
-C2H5+H2 -CH3+CH4 -54.4KJ/mol
在水蒸气存在的条件下,还可能发生下列反应:




 -C2H5+2H2O -CH3+CO2+3H2
-C2H5+2H2O -CH3+CO2+3H2
此外还有芳烃缩合及苯乙烯聚合生成焦油和焦等。这些连串副反应的发生不仅使反应选择性下降,而且极易使催化剂表面结焦进而活性下降。
2.影响本反应的因素
1)温度的影响
乙苯脱氢反应为吸热反应,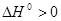 ,从平衡常数与温度的关系式
,从平衡常数与温度的关系式 可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。但是温度过高副反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适宜的反应温度。本实验的反应温度为:540~600℃。
可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。但是温度过高副反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适宜的反应温度。本实验的反应温度为:540~600℃。
2)压力的影响
乙苯脱氢为体积增加的反应,从平衡常数与压力的关系式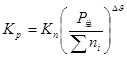 可知,当时
可知,当时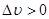 ,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。本实验加水蒸气的目的使降低乙苯的分压,以提高平衡转化率。较适宜的水蒸气用量为:水:乙苯=1.5:1(体积比)或8:1(摩尔比)。
,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。本实验加水蒸气的目的使降低乙苯的分压,以提高平衡转化率。较适宜的水蒸气用量为:水:乙苯=1.5:1(体积比)或8:1(摩尔比)。
3)空速的影响
乙苯脱氢反应系统中有平衡副反应和连串副反应,随着接触时间的增加,副反应也增加,苯乙烯的选择性可能下降,适宜的空速与催化剂的活性及反应温度有关,本实验乙苯的液空速以0.6/h为宜。
3. 催化剂
本实验采用氧化铁系催化剂。其组成为:Fe2O3-CuO-K2O-Cr2O3-CeO2。
三、实验装置及流程
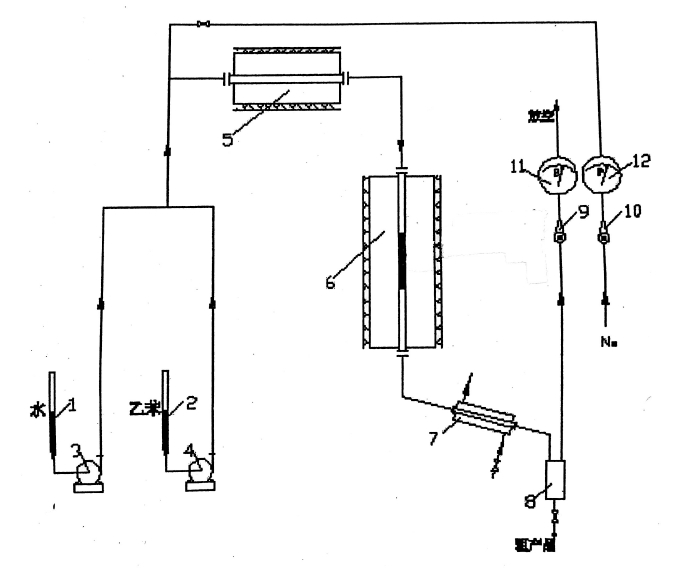
1-水计量管;2-乙苯计量管;3、4-进料泵; 5-汽化室;6-反应室;7-冷凝室;
8-集液罐;9-H2流量计;10-N2流量计;11-湿式气体流量计;12-N2压力表。
图1 乙苯脱氢制备苯乙烯实验工艺流程图
四.实验步骤与方法
(1) 反应条件控制:
汽化温度300℃,脱氢反应温度540和580℃,水:乙苯=1.5:1(体积比),相当于乙苯加料0.5毫升/分钟,蒸馏水0.75毫升/分钟。
(2) 操作步骤
1) 了解并熟悉实验装置及流程,搞清物料走向及加料、出料方法。
2) 将气化室温度控制设定在300℃,反应器温度控制设定为540℃
3) 系统通氮气20l/h,打开气化室加热开关,并打开冷却水开关。
4) 打开反应器加热开关。
5) 当反应器温度到达400℃,开始加入蒸馏水,控制流量为0.75毫升/分钟,并改变氮气流量为10l/h。
6) 当反应器温度稳定在540℃,停止通入氮气,开始加入乙苯,控制流量为0.50毫升/分钟。
7) 记录乙苯加料管内起始体积,并将积液灌放空。
8) 反应50分钟后停止进料改通氮气流量为10l/h。
9)记录原料加入体积。
10)将粗产品取出后静置分层,用分液漏斗分去水层,称出烃层质量。
11)取少量样品进行气相色谱分析并计算出各组分的百分含量。
12)改变反应器温度为580℃后再加入乙苯,重复8~11,测得有关数据。
13)反应结束后,维持温度为500℃持续通入水蒸气,进行催化剂的清焦再生,半小时后停止加水,通入氮气并使反应器降温,至300℃以下时,可切断电源和冷却水,停通氮气。
五.实验数据记录及处理
1)原始记录
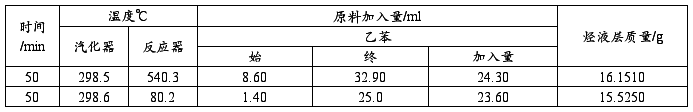
2)粗产品分析结果
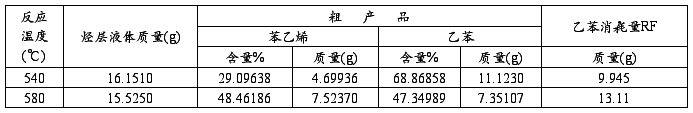
3)计算结果
乙苯的转化率: 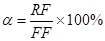
540℃下,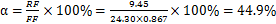
580℃下,
苯乙烯的选择性: 
540℃下,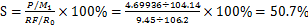
580℃下,
苯乙烯的收率: 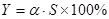
540℃下,Y=α·S×100%=0.449×0.507×100%=22.8%
580℃下,Y=α·S×100%=0.641×0.585×100%=37.5%
注: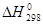 —298K下标准热焓,KJ/mol;
—298K下标准热焓,KJ/mol;
KP,Kn—平衡常数;
ni—i组分的摩尔分数;
P总—压力,Pa;
R—气体常数;
T—温度,K;
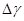 —反应前后摩尔数变化;
—反应前后摩尔数变化;
 —原料的转化率%;
—原料的转化率%;
S—目的产物的选择性%;
Y—目的产物的收率;
RF—原料消耗量,g;
FF—原料加入量,g;
P—目的产物的量,g。
六.结果与讨论
由实验计算结果可以知道,在较高温度下乙苯制苯乙烯的反应在转化率上有一定提高,而且在选择性上也有一定,说明这个反应在高温下更加有利,这与理论相符合。
实验转化率很低,可能是由于水未完全汽化,导致部分催化剂失效或流失,或催化剂使用时间过长,部分已失效。
七、思考题
1、该反应是吸热还是放热,如何判断?如果是吸热,则升高温度对反应是否有利?是不是越高越好?
答:因为温度升高后乙苯的转化率和苯乙烯的收率均变大,该反应吸热;从热力学角度上来看,温度越高越好,但不能超过催化剂的适用温度,而且反应温度越高,就需要消耗更多能源,导致费用增大。
2、对本反应而言,体积增大还是减小?加压对反应有利吗?为什么要加入蒸馏水?可以用自来水吗?
答?反应压力 对于给定的反应温度和水比,乙苯的转化率随着反应压力的降低而显著增加。体积增大后,反应压强减小,对反应有利。
加压对反应不利,苯乙烯是容易聚合的物质。反应压力高,将有利于苯乙烯自聚,生成对装置正常运转十分不利的聚合物,它会造成管道、设备的堵塞。
加入水蒸汽可以较少乙苯分压,达到类似于降低反应压力的效果;水蒸汽可与催化剂上生成的碳发生反应,起到减少催化剂表面结焦的作用;水蒸汽还可防止催化剂的活性组份还原为金属,有利于延长催化剂寿命。
不能用自来水,自来水中含有微量金属离子和氯离子,会使催化剂中毒失效。
第二篇:浙江大学化工原理(过程工程与控制乙)实验报告 精馏实验
实验报告
课程名称:过程工程原理实验(乙) 指导老师:xx 成绩:__________________
实验名称:筛板塔精馏操作及效率测定 实验类型:工程实验 同组学生姓名:xx
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、主要仪器设备(必填) 四、操作方法和实验步骤
五、实验数据记录和处理 六、实验结果与分析(必填)
七、讨论、心得
筛板塔精馏操作及效率测定
1实验目的
1.1 了解板式塔的结构和流程,并掌握其操作方法;
1.2 测定筛板塔在全回流和部分回流时的全塔效率。
2 实验装置
2.1 精馏塔装置由塔釜、塔体、全凝器、加料系统、回流系统、贮槽(原料、产品、釜液)以及测量、控制仪表等组成。装置流程如图1所示。
2.2 装置规格介绍:筛板精馏塔内径68mm,共7块塔板,其中精馏段5块,提馏段2块;精馏段塔板间距150mm,提馏段塔板间距180mm;筛孔孔径1.5m,正三角形排列,孔间距4.5mm,开孔数104个。装置采用电加热,塔釜内有3支额定功率为3kW的螺旋管加热器。
3 实验原理
3.1在板式精馏塔中,偏离平衡的汽液两相在塔板上进行传质、传热,当离开该板的汽、液两相组成平衡、温度相同时,则此板称为理论板。
实际操作中,由于塔板上的汽、液两相接触时间有限及相间返混等因素影响,使汽、液两相尚未达到平衡即离开塔板。即一块实际塔板的分离效果达不到一块理论板的作用,因此精馏塔所需的实际板数比理论板数多。
3.2 全回流操作时的全塔效率ET的测定
全塔效率(总板效率)ET
 (1)式中:
(1)式中: —为完成一定分离任务所需的理论板数,包括蒸馏釜;
—为完成一定分离任务所需的理论板数,包括蒸馏釜;
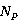 —为完成一定分离任务所需的实际板数,本装置
—为完成一定分离任务所需的实际板数,本装置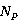 =7块。
=7块。
在全回流操作中,操作线在x-y图上为对角线。根据实验中所测定的塔顶组成xD、塔底组成xW(均为摩尔百分数)在操作线和平衡线间作梯级,即可得到理论板数 。
。
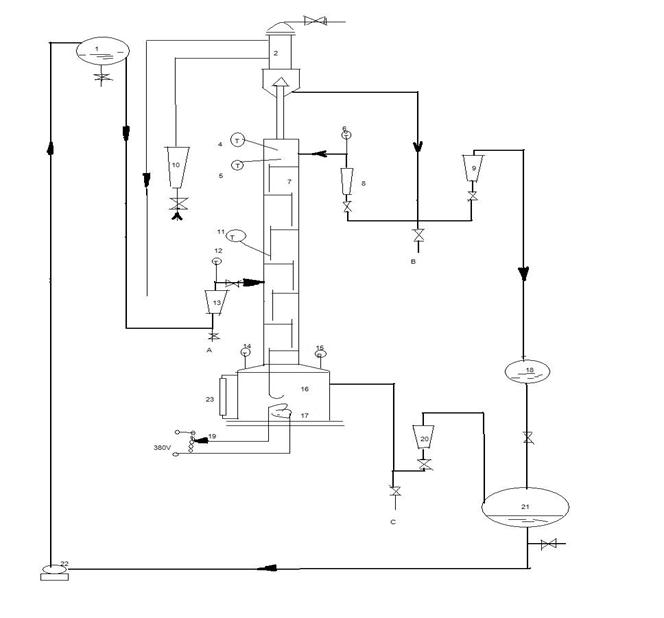

图1.实验装置图
3.3 部分回流时全塔效率ET’的测定
3.3.1 精馏段操作线方程为:
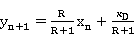 (2)
(2)
式中:R—回流比;
xD—塔顶产品的组成,摩尔百分数。
实验中回流量由回流转自流量计测量,但由于实验操作中一般作冷液回流,所以实际操作回流量应作如下修正:
 (3)
(3)
式中:L0—回流转子流量计上的读数值,ml/min;
L—实际回流量,ml/min;
tD—塔顶液相温度,℃;
tR—回流液温度,℃;
CpD——塔顶回流液在平均温度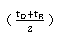 下的比热,kJ/kg·K;
下的比热,kJ/kg·K;
rD——塔顶回流液组成下的汽化潜热,kJ/kg 。
产品量D可由产品转子流量计测量。由于产品量D与回流量L的组成和温度相同,故回流比R可直接用两者的比值来得到。
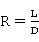 (4)
(4)
式中:D—产品转子流量计上的读数值,ml/min 。
实验中根据塔顶取样可得塔顶组成xD,并测量回流和产品转子流量计读数L0和D以及回流温度tR和
塔顶液相温度tD,再查附表可得CPD、rD,代入即可以得到精馏段操作线方程。
3.3.2 进料q线方程为:
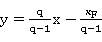 (5)
(5)
式中:q—进料的液相分率;
xF—进料液的组成,摩尔百分数;
且: 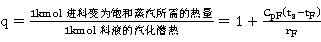 (6)
(6)
式中:ts—进料液的泡点温度,℃;
tF—进料液的温度,℃;
CpF—进料液在平均温度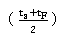 下的比热,kJ/kg·K;
下的比热,kJ/kg·K;
rF—进料液组成下的汽化潜热,kJ/kg 。
实验中根据进料液取样可得到xF,并测量其进料温度tF,再查附表得到ts、tF、CpF,代入就可以得到q,进而得到q线方程。
3.3.3 理论板数的求取
根据上述得到的精馏段操作线方程和q线方程,以及测量得到的塔顶组成xD、塔底组成xW和进料组成xF,就可以在x-y图上作出精馏段操作线、q线和提馏段操作线,然后用x-y图解法即可得到理论板数NT,代入(1)式即可得到全塔效率ET。
4 实验步骤
4.1 全回流操作:关闭进、出料阀门,全开冷凝器顶部排气阀,稍开冷凝冷却水阀门,将回流和产品流量计开为最大。待灵敏板温度稳定后,分别取塔顶液和塔釜液两个样品,并读取回流液流量,再分别读取各个温度计温度读数。用比重法测定塔顶液和塔釜液的组成度。
4.2 部分回流操作:打开进料阀门,调节转子流量计读数为200ml/min左右,调节产品转子流量计,使回流比保持在3~5。通过对釜液转子流量计得调整,使塔釜液位计的液位保持恒定。等待釜液液面恒定以及灵敏板温度逐渐稳定后,记录温度计的温度,记录进料、馏出液、釜液流量计读数,测定组成。
4.3 实验结束:先关闭进料、产品和釜液得流量调节阀,再将调压器旋钮调至零位,关总电源开关切断电源,等待酒精蒸气完全冷凝后,再关闭冷却水,并做好整洁工作。
5 实验数据处理
5.1 原始数据记录表

5.2 数据处理
5.2.1 全回流操作塔板数,如图2
由图可知:所需理论板数为6.4
所以全塔效率为:

5.2.2部分回流时全塔效率ET′
5.2.2.1 精馏段操作线方程
平均温度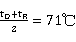 ,乙醇质量分数:90%,查表得:
,乙醇质量分数:90%,查表得: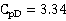 kJ/kg·K ,
kJ/kg·K , 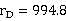 kJ/kg
kJ/kg
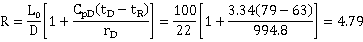
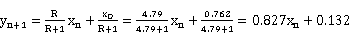
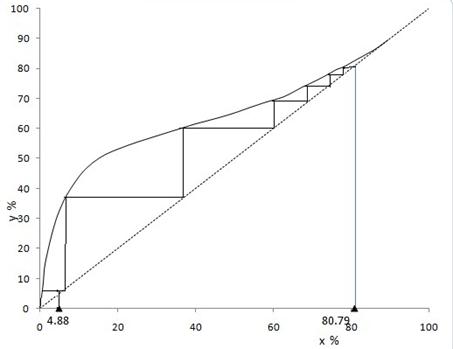
图2. 全回流时理论塔板数计算
5.2.2.2 q 线方程:同理可得: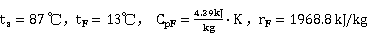

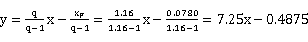
根据精馏段操作线方程和q 线方程,以及取样得到的馏出液组成xD,塔釜组成x w和进料液组成
x F,在x-y图中用图解法即可得到理论塔板数NT,见图3 :
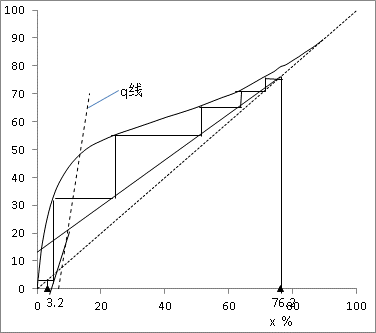
图3. 部分回流时理论塔板数计算
由图可知,NT=5.5
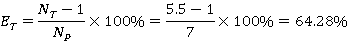
6 实验分析及讨论
6.1 在进行部分回流实验时,由于没有控制好回流比在3~5之间,导致实验结果出现很大的偏差,所以在时间允许的条件下,本小组重新进行实验,才得到比较理想的结果。这告诉我们实验前要充分预习实验得步骤和注意事项,掌握好实验条件的要求,才能将实验顺利完成。
6.2 精馏是利用回流手段、经过多次平衡级过程,使物系实现高纯度分离的操作。二元连续精馏的简化计算前提为理论板假定和恒摩尔流假定,而实际上这两个假定并不严格成立,所以计算的结果会有一定误差。但是过程工程原理实验是工程实验,对精确度要求并不是特别高,所以工程上可以认为假定成立。
6.3影响精馏操作稳定的因素是哪些?维持塔稳定操作应注意哪些操作?如何判断塔的操作已经达到稳定?
影响精馏操作稳定的因素有:回流比、进料状态、进料量、进料组成、进料温度、塔顶冷剂量、塔顶采出量、塔底采出量等。
为了维持塔操作的稳定,需要在操作中不断调节回流比,使之基本固定在3~5之间,并维持塔底采出量不变。
判断操作是否达到稳定的依据是灵敏板的温度是否稳定。
6.4 塔顶冷回流对塔内回流流量有何影响?如何校正?
塔顶冷回流时,回流液的温度与塔顶的蒸气之间有温差,将一部分热量传递给回流液后蒸气自身凝结成液体,即内回流的部分,从而增大了回流液的流量。
应作以下的校正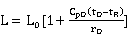 (实验原理部分已经阐明,此处不再重复)。
(实验原理部分已经阐明,此处不再重复)。
6.5 操作线斜率大,意味着经过一块理论板后,汽相的增浓程度变大,液相的减浓程度变大。故操作线斜率大对精馏段的分离是有利的。而进料状况则影响到提馏段传质推动力和再沸器的热负荷,本实验中并不涉及再沸器。
6.6 本实验用图解法求理论塔板数。具体做法为:做出精馏、提留以及进料操作线。分做过回流液浓度点点的垂线,与对角线交于a点,以塔釜液浓度点为b点。从点a开始在平衡线和精馏段操作线之间画阶梯,当梯级跨过点d时,就改在平衡线和提馏段操作线之间画阶梯,直至梯级跨过点b为止;所画的总阶梯数就是全塔所需的理论塔板数。另外也可用逐步计算的方法求得理论塔板数。
参考文献:《过程工程原理实验(乙)》 . 杭州:浙江大学化学工程实验室 . 2009.8.
《化工原理下册》 . 何潮洪等 . 北京:科学出版社 . 2008.5.
-
乙苯脱氢制苯乙烯实验报告 浙大化工
实验报告课程名称:化工专业实验指导老师:王晓钟成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学…
-
乙苯脱氢制苯乙烯实验报告
乙苯脱氢制苯乙烯实验报告一实验目的1了解以乙苯为原料在铁系催化剂上进行固定床制备苯乙烯的过程学会设计实验流程和操作2掌握乙苯脱氢操…
-
乙苯脱氢制苯乙烯实验思考题
1乙苯脱氢生成苯乙烯反应是吸热还是放热反应如何判断如果是吸热反应则反应温度为多少本实验采用的什么方法工业上又是如何来实现的答乙苯脱…
-
乙苯脱氢制苯乙烯
实验报告课程名称:化工专业实验指导老师:XX成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学生…
-
实验22 乙苯脱氢制苯乙烯
实验22乙苯脱氢制苯乙烯一实验目的与要求1了解苯乙烯制备过程设计合理工艺流程并安装好实验装置2掌握检查实验装置漏气的方法3学会稳定…
-
乙苯脱氢制苯乙烯实验报告
乙苯脱氢制苯乙烯实验报告一实验目的1了解以乙苯为原料在铁系催化剂上进行固定床制备苯乙烯的过程学会设计实验流程和操作2掌握乙苯脱氢操…
-
乙苯脱氢制苯乙烯实验思考题
1乙苯脱氢生成苯乙烯反应是吸热还是放热反应如何判断如果是吸热反应则反应温度为多少本实验采用的什么方法工业上又是如何来实现的答乙苯脱…
-
乙苯脱氢制苯乙烯
实验报告课程名称:化工专业实验指导老师:XX成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学生…
-
实验22 乙苯脱氢制苯乙烯
实验22乙苯脱氢制苯乙烯一实验目的与要求1了解苯乙烯制备过程设计合理工艺流程并安装好实验装置2掌握检查实验装置漏气的方法3学会稳定…
-
网上试验乙苯脱氢制苯乙烯
实验名称实验五乙苯脱氢制苯乙烯块名称预习考查题目权重1乙苯脱氢反应实采用哪种反应器A绝热列管式反应器B等温列管式反应器C流化床反应…