乙苯脱氢制苯乙烯

 实验报告
实验报告
课程名称: 化工专业实验 指导老师: 成绩:__________________
实验名称: 乙苯脱氢制苯乙烯 实验类型:_____同组学生姓名:
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、主要仪器设备(必填) 四、操作方法和实验步骤
五、实验数据记录和处理 六、实验结果与分析(必填)
七、讨论、心得
一、实验目的
1、了解以乙苯为原料,氧化铁系为催化剂,在固定床单管反应器中制备苯乙烯的过程。
2、掌握乙苯脱氢操作条件对产物收率的影响,学会获取稳定的工艺条件的方法。
3、掌握乙苯脱氢制备苯乙烯的转化率、选择性、收率与反应温度的关系;找出最适宜的反应温度区域。
4、学会使用温度控制和流量控制的一般仪表、仪器。
5、了解气相色谱分析及使用方法。
二、实验内容和原理
1、本实验的主副反应
主反应: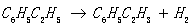
副反应:
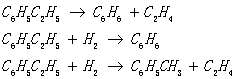
在水蒸气存在的条件下,还可能发生下列反应: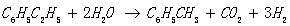
此外还有芳烃脱氢缩合及苯乙烯聚合生成焦油。这些连串副反应的发生不仅使反应的选择性下降,而且极易使催化剂表面结焦进而活性下降。
2、影响本反应的因素:
(1) 温度的影响
乙苯脱氢反应为吸热反应,△H0>0,从平衡常数与温度的关系式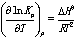 可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。但是温度过高副反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适应的反应温度。本实验的反应温度为540~600℃。
可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。但是温度过高副反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适应的反应温度。本实验的反应温度为540~600℃。
(2) 压力的影响
乙苯脱氢为体积增加的反应,从平衡常数与压力的关系式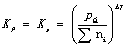 可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。本实验中加水蒸气的目的是降低乙苯的分压,以提高乙苯的平衡转化率。较适宜的水蒸气用量为:水:乙苯=1.5:1(体积比)或8:1(摩尔比)。
可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。本实验中加水蒸气的目的是降低乙苯的分压,以提高乙苯的平衡转化率。较适宜的水蒸气用量为:水:乙苯=1.5:1(体积比)或8:1(摩尔比)。
(3) 空速的影响
乙苯脱氢反应系统中有平行副反应和连串副反应,随着接触时间的增加,副反应也增加,苯乙烯的选择性可能下降,故需采用较高的空速,以提高选择性。适宜的空速与催化剂的活性及反应温度有关,本实验乙苯的液空速以0.6h-1适宜。
3、催化剂
本实验实用GS-08催化剂,以Fe,K为主要活性组分,添加少量的IA,IIA,IB族以稀土氧化物为助剂。
三、实验装置、实验准备物料及仪器
1、乙苯脱氢制苯乙烯实验装置流程见下图:
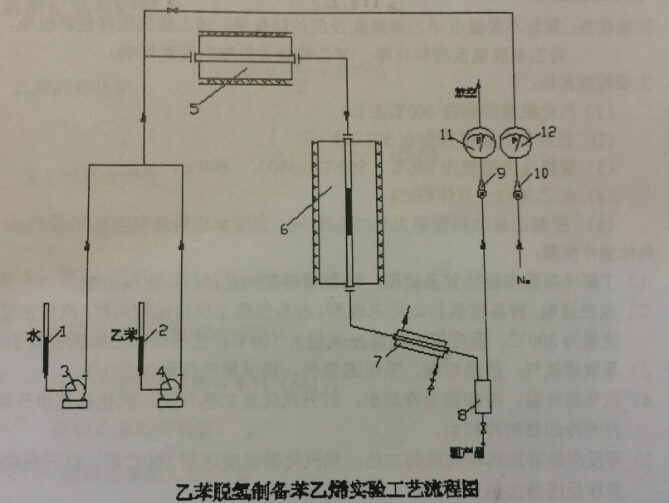
1-水计量管;2-乙苯计量管;3、4进料泵;5-气化室;6-反应室;7-冷凝器;
8-集液罐;9-H2流量计;10-N2流量计;11-湿式气体流量计;12-N2压力表
2、药品:乙苯(分析纯) 1瓶;瓶蒸馏水 一桶;氮气一钢瓶
3、实验器具:电子天平一台;色谱一台(测液体浓度);秒表一只(或用手机等其他代替)
100ml量筒2个;100ml烧杯4个;100ml分液漏斗2个;1ug色谱取样管2个
四、操作方法和实验步骤
1、 实验任务:测定不同温度下乙苯脱氢反应的转化率、苯乙烯的选择性和收率,考察温度对乙苯脱氢反应转化率、苯乙烯选择性和收率的影响。
2、 主要控制指标:
(1)汽化温度控制在300℃左右,
(2)反应器前温度控制在500℃,
(3)脱氢反应温度为540℃、600℃,
(4)水:乙苯=1.5:1(体积比)。
(5)控制乙苯加料速度为0.5ml/min,蒸馏水进料速度为0.75ml/min。
3、 具体操作步骤
(1)了解并熟悉实验装置及流程,搞清物料走向及加料、出料方法。
(2)仪表通电,待各仪表初始化完成后,在各仪表上设定控制温度:汽化室温度控制设定值为300℃、反应器前温度控制为500℃,反应器温度控制值为540℃。
(3)系统通氮气:接通电源,系统通氮气,调节氮气流量为20l/h。
(4)汽化器升温,冷却器通冷却水:打开汽化室加热开关,汽化室逐步升温,并打开冷却器的冷却水。
(5)开反应器前加热和反应器加热:当汽化器温度达到200℃后,打开反应器前加热开关和反应器加热开关。
(6)开始通蒸馏水并继续通氮气:当反应器温度达400℃时,开始加入蒸馏水,控制流量为0.75ml/min,氮气为10l/h。
(7)停止通氮气加乙苯:当反应器内温度升到540℃左右并稳定后,停止通氮气,开始加入乙苯,流量控制为0.5ml/min。
(8)记下乙苯加料管内起始体积,并将集液管内的料液放空。
(9)物料在反应器内反应50分钟左右,停止乙苯进料,该通氮气,流量为10l/h。并继续通蒸馏水,保持汽化室和反应器内的温度。
(10)记录此时乙苯体积,算出原料加入反应器的体积:
(11)将粗产品从集液管内放入量筒内静置分层。
(12)分层完全后,用分液漏斗分去水层,称出烃层液体质量。
(13)量取少量烃层液样品,用气相色谱分析组成,并计算出各组分的百分含量。
(14)改变反应器控制温度为600℃,继续升温,当反应器温度升至600℃左右并稳定后,再次加入乙苯入反应器反应,重复之前操作,并记录相关数据。
(15)反应结束后,停止加乙苯。反应温度维持在500℃左右,继续通水蒸气,进行催化剂的清焦再生,约半小时后停止通水,停止各反应器加热,通氮气清除反应器内的氢气,并使实验装置降温。实验装置降温到300℃以下时,可切断电源,切断冷却水,停止通氮气,整理好试验现场,离开实验室。
(16)对实验结果进行分析讨论。
五、实验数据记录和处理
表1实验数据记录表
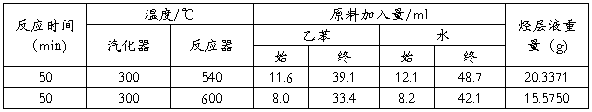
表2粗产品分析结果
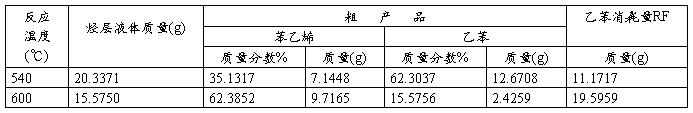
相对校正因子:苯:1.000 甲苯:0.8539 乙苯:1.006 苯乙烯:1.032
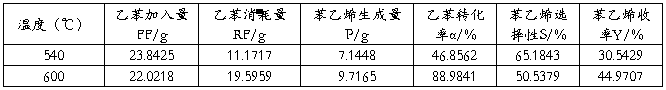
计算示例:
以温度为540℃为例进行计算
乙苯加入量: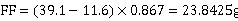
乙苯消耗量: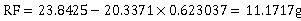
苯乙烯生成量:P=20.3371 0.351317=7.1448g
0.351317=7.1448g
乙苯转化率: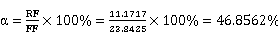
苯乙烯选择性: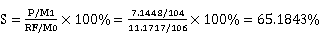
苯乙烯的收率:
六、实验结果与分析
1、乙苯转化率和温度关系
实验中温度升高,乙苯转化率增大。乙苯脱氢反应为吸热反应,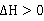 ,从平衡常数与温度的关系式
,从平衡常数与温度的关系式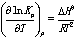 可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。
可知,提高温度可增大平衡常数,从而提高脱氢反应的平衡转化率。
2、苯乙烯选择性与温度关系
实验中升高温度,苯乙烯选择性降低。温度升高使副反应增加,苯乙烯选择性下降。从产物色谱图可以看出,600℃下色谱图中有四个明显的峰,而540℃下的色谱图中仅苯乙烯、乙苯的峰较明显。
3、苯乙烯收率
实验中升高温度,苯乙烯收率增加。
七、讨论、心得
1、 由温度升高后乙苯的转化率增大,确定该反应是吸热。适度的升温有利于主反应的进行,但随着温度升高,副反应增加,使苯乙烯选择性下降;且温度过高,能耗增大,设备材质要求增加。因而不是反应温度越高越好。
2、 乙苯脱氢为体积增加的反应。从平衡常数与压力的关系式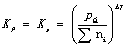 可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故减压有利于平衡向脱氢方向移动。本实验中加蒸馏水是为了产生水蒸气,目的是降低乙苯的分压,以提高乙苯的平衡转化率。不能用自来水代替蒸馏水。
可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故减压有利于平衡向脱氢方向移动。本实验中加蒸馏水是为了产生水蒸气,目的是降低乙苯的分压,以提高乙苯的平衡转化率。不能用自来水代替蒸馏水。
3、 试验中生成的苯乙烯、苯、甲苯在常温下为液态,而生成的氢气、二氧化碳、乙烷、乙烯为气态。可根据产物沸点来判定。
第二篇:乙苯脱氢制苯乙烯实验报告
乙苯脱氢制苯乙烯实验报告
一 实验目的
(1)了解以乙苯为原料在铁系催化剂上进行固定床制备苯乙烯的过程,学会设计实验流程和操作;
(2)掌握乙苯脱氢操作条件对产物收率的影响,学会获取稳定的工艺条件之方法。
(3)掌握催化剂的填装、活化、反应使用方法。
(4)掌握色谱分析方法。
二 实验原理
2.1主副反应
乙苯脱氢生成苯乙烯和氢气是一个可逆的强烈吸热反应,只有在催化剂存在的高温条件下才能提高产品收率,其反应如下:
主反应
 C6H5C2H5 C6H5C2H3 + H2
C6H5C2H5 C6H5C2H3 + H2
副反应
 C6H5C2H5 C6H6 + C2H4
C6H5C2H5 C6H6 + C2H4
 C2H4 + H2 C2H6
C2H4 + H2 C2H6
 C6H5C2H5 + H2 C6H6+ C2H6
C6H5C2H5 + H2 C6H6+ C2H6
C6H5C2H5 C6H5-CH3+ CH4
 此外,还有部分芳烃脱氢缩合、聚合物以及焦油和碳生成。
此外,还有部分芳烃脱氢缩合、聚合物以及焦油和碳生成。
2.2 影响因素
2.2.1温度的影响
乙苯脱氢反应为吸热反应,△H0>0,从平衡常数与温度的关系式 可知,提高温度可增大平衡常数,从而提高脱 氢 反应的平衡转化率。但是温度过高副 反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适应的反应温度。
可知,提高温度可增大平衡常数,从而提高脱 氢 反应的平衡转化率。但是温度过高副 反应增加,使苯乙烯选择性下降,能耗增大,设备材质要求增加,故应控制适应的反应温度。
2.2.2 压力的影响
乙苯脱氢为体积增加的反应,从平衡常数与压力的关系式 可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。实验中加入惰性气体或减压条件下进行,通常均使用水蒸气作稀释剂,它可降低乙苯的分压,以提高平衡转化率。水蒸气的加入还可向脱氢反应提供部分热量,使反应温度比较稳定,能使反应产物迅速脱离催化剂表面,有利于反应向苯乙烯方向进行;同时还可以有利于烧掉催化剂表面的积碳。但水蒸汽增大到一定程度后,转化率提高并不显著,因此适宜的用量为:水:乙苯=1.2~2.6:1(质量比)。
可知,当△γ>0时,降低总压P总可使Kn增大,从而增加了反应的平衡转化率,故降低压力有利于平衡向脱氢方向移动。实验中加入惰性气体或减压条件下进行,通常均使用水蒸气作稀释剂,它可降低乙苯的分压,以提高平衡转化率。水蒸气的加入还可向脱氢反应提供部分热量,使反应温度比较稳定,能使反应产物迅速脱离催化剂表面,有利于反应向苯乙烯方向进行;同时还可以有利于烧掉催化剂表面的积碳。但水蒸汽增大到一定程度后,转化率提高并不显著,因此适宜的用量为:水:乙苯=1.2~2.6:1(质量比)。
2.2.3 空速的影响
乙苯脱氢反应中的副反应和连串副反应,随着接触时间的增大而增大,产物苯乙烯的选择性会下降,催化剂的最佳活性与适宜的空速及反应温度有关,本实验乙苯的液空速以0.6~1h-1为宜。
2.2.4 催化剂
乙苯脱氢技术的关键是选择催化剂。此反应的催化剂种类颇多,其中铁系
催化剂是应用最广的一种。以氧化铁为主,添加铬、钾助催化剂,可使乙苯的转化率达到40%,选择性90%。在应用中,催化剂的形状对反应收率有很大影响。小粒径、低表面积、星形、十字形截面等异形催化剂有利于提高选择性。
为提高转化率和收率,对工业规模的反应器的结构要进行精心设计。实用效果较好的有等温和绝热反应器。实验室常用等温反应器,它以外部供热方式控制反应温度,催化剂床层高度不宜过长。
三 实验装置及仪器
实验流程见图1。
反应器有石英玻璃管和不锈钢管式反应器两种,内部中心轴向有测温热电偶插入管,结构如图2、图3。
图1 实验装置流程图
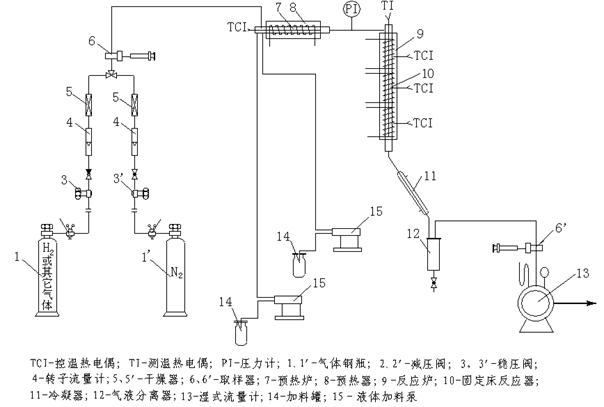

反应器有石英玻璃管和不锈钢管式反应器两种,内部中心轴向有测温热电偶插入管,结构如图2、图3。
所用仪器如下:
(1)柱塞式液体加料泵 2台;
(2)氮气钢瓶 1个;
(3)注射器(10μl) 1支;
(4)色谱仪 1台;
(5)取样瓶 5只;
(6)分液漏斗 1个;
(7)反应器及温度控制仪 1套;
(8)冷却器 1个;
(9)气液分离器 1个;
(10)储液瓶 2支;
(11)催化剂 20ml。
四 实验步骤
(1)组装流程(将催化剂按图2、3所示装入反应器内),检查各接口,试漏(空气或氮气)。
(2)检查电路是否连接妥当。
(3)上述准备工作完成后,开始升温,预热器温度控制在200~300℃。待反应器温度达到200℃后,开始启动注水加料泵,同时调整流量(控制在0.3ml/min以内)持续升温,温度升至500℃时,恒温活化催化剂3个小时,此后逐渐升温至550℃,启动乙苯加料泵。调节流量在水:乙苯=2:1(体积比)范围内,并严格控制进料速度使之稳定。反应温度控制在550℃、575℃、600℃、625℃。考查不同温度下反应物的转化率与产品的收率。
(4)在每个反应条件下稳定30分钟后,取20分钟样品二次,取样时用分液漏斗分离水相,用注射器进样至色谱仪中测定其产物组成。分别称量油相及水相重量,以便进行物料恒算。
(5)反应完毕后停止加乙苯原料,继续通水维持30~60分钟,以清除催化剂上的焦状物,使之再生后待用。
(6)实验结束后关闭水、电。
五 数据记录与处理
根据实验内容自行设计记录表格,记录实验数据:
原始记录 室温:16 ℃ 大气压:1.01325MPa
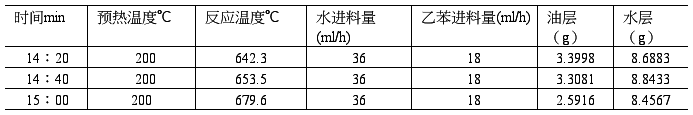
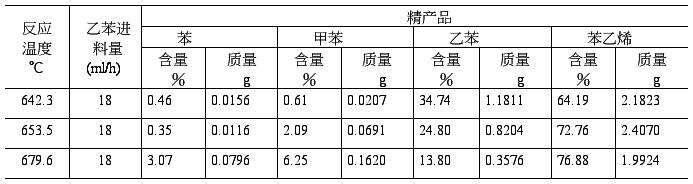
以642.3℃数据计算为例
乙苯转化率=1-34.74%=65.26%
苯乙烯选择性=×100%=98.36%
苯乙烯收率=0.6526×0.9836=0.6419
数据处理如下表:
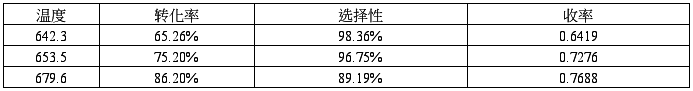
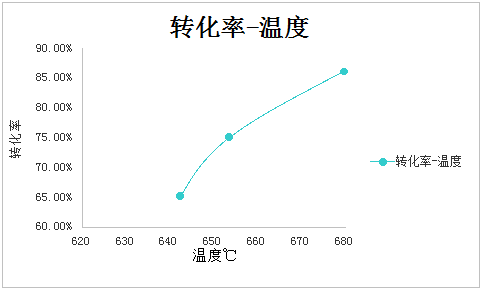
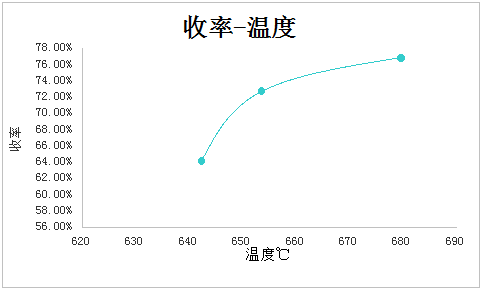
六 结果分析
乙苯脱氢生成苯乙烯和氢气是一个可逆的强烈吸热反应,其反应如下:
主反应
 C6H5C2H5 C6H5C2H3 + H2
C6H5C2H5 C6H5C2H3 + H2
副反应
 C6H5C2H5 C6H6 + C2H4
C6H5C2H5 C6H6 + C2H4
 C2H4 + H2 C2H6
C2H4 + H2 C2H6
 C6H5C2H5 + H2 C6H6+ C2H6
C6H5C2H5 + H2 C6H6+ C2H6
C6H5C2H5 C6H5-CH3+ CH4
温度升高有利于主反应的进行,转化率明显升高;由于副反应的存在,温度升高有利于副反应的进行,选择性降低。
附录
(1)色谱仪使用方法
实验采用双气路恒温型热导检测器气相色谱仪进行乙苯及其反应后的产物分析。色谱条件如下:
色谱柱:SE30/6201 填充柱:¢3mm,长2m
载气:柱前压:0.05Mpa 桥流:120mA
气化器:150℃ 柱温:120℃
检测器:120℃
(2)质量校正因子:
苯:1.000 甲苯:0.8539 乙苯:1.006
苯乙烯:1.032
乙苯密度:0.867g/ml
-
乙苯脱氢制苯乙烯实验报告 浙大化工
实验报告课程名称:化工专业实验指导老师:王晓钟成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学…
-
乙苯脱氢制苯乙烯实验思考题
1乙苯脱氢生成苯乙烯反应是吸热还是放热反应如何判断如果是吸热反应则反应温度为多少本实验采用的什么方法工业上又是如何来实现的答乙苯脱…
-
乙苯脱氢制苯乙烯
实验报告课程名称:化工专业实验指导老师:XX成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学生…
-
实验22 乙苯脱氢制苯乙烯
实验22乙苯脱氢制苯乙烯一实验目的与要求1了解苯乙烯制备过程设计合理工艺流程并安装好实验装置2掌握检查实验装置漏气的方法3学会稳定…
-
网上试验乙苯脱氢制苯乙烯
实验名称实验五乙苯脱氢制苯乙烯块名称预习考查题目权重1乙苯脱氢反应实采用哪种反应器A绝热列管式反应器B等温列管式反应器C流化床反应…
-
乙苯脱氢制苯乙烯实验报告 浙大化工
实验报告课程名称:化工专业实验指导老师:王晓钟成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学…
-
乙苯脱氢制苯乙烯实验报告
乙苯脱氢制苯乙烯实验报告一实验目的1了解以乙苯为原料在铁系催化剂上进行固定床制备苯乙烯的过程学会设计实验流程和操作2掌握乙苯脱氢操…
-
乙苯脱氢制苯乙烯实验思考题
1乙苯脱氢生成苯乙烯反应是吸热还是放热反应如何判断如果是吸热反应则反应温度为多少本实验采用的什么方法工业上又是如何来实现的答乙苯脱…
-
乙苯脱氢制苯乙烯
实验报告课程名称:化工专业实验指导老师:XX成绩:__________________实验名称:乙苯脱氢制苯乙烯实验类型:同组学生…
-
实验22 乙苯脱氢制苯乙烯
实验22乙苯脱氢制苯乙烯一实验目的与要求1了解苯乙烯制备过程设计合理工艺流程并安装好实验装置2掌握检查实验装置漏气的方法3学会稳定…