��ѧ��Ӧ���ʽ�ѧ���
��ѧ��Ӧ���ʽ�ѧ���
һ����ѧ���
1.��ѧĿ�꣺
(1)��֪ʶĿ���뼼��
�١�֪����ѧ��Ӧ���ʵĶ�����ʾ�����������м��㡣
�ڡ�����ʵ��ⶨijЩ��ѧ��Ӧ���ʵ�ԭ���ͳ��÷�����
�ۡ�ͨ��ѧϰ����ʹѧ������ѧ�����û�ѧ�ӽǣ�ȥ�۲����������������йػ�ѧ��Ӧ���ʵ����⡣
(2)�������뷽��
ѧϰʵ��̽���Ļ����������ܹ��ڲ��롢̽����ʵ������ɻ�ѧ��Ӧ���ʵĶ�����ʾ�����������м��㼰ʵ��ⶨһЩ��ѧ��Ӧ���ʵ�̽��������ѧ���۲�������˼ά������ʵ��������
(3)�����̬�����ֵ��
�١����黯ѧʵ���ϲ�ã������Ի�ѧ��Ӧ�о�����Ȥ����ǿѧ����������ʵ����
�ڡ�����ѧ���ıȽϷ���˼άƷ�ʡ�
2.�̲ķ�����
����Ԫ�������ڸ��л�ѧ����2�жԻ�ѧ��Ӧ���ʺ�����ʶ�Ļ�����չ���ġ����л�ѧ����2�ӻ�ѧ��Ӧ�����뷴Ӧ����������������ѧ�����������ʶ��ѧ��Ӧ��ʹѧ���ڽ��һЩ�Ļ�����������ʱ����ữѧ����ѧϰ����Ҫ�ԡ���ѧ��Ӧ�����DZ�ר��Ŀ�ƪ��ͨ��ѧϰʹѧ������ѧ�����û�ѧ�ӽǣ�ȥ�۲����������������йػ�ѧ��Ӧ���ʵ����⡣�ⲿ�������Ǻ���ѧϰӰ�컯ѧ��Ӧ���ʵ����ء���ѧƽ�⡢��ѧ��Ӧ���еķ���Ļ�������ѧ���ĺ���ѧϰ������Զ��Ӱ�졣
3.���ѵ�
�ص㣺��ѧ��Ӧ���ʵĶ�����ʾ����������
�ѵ㣺ͨ��ʵ��ⶨijЩ��ѧ��Ӧ���ʡ�
4��ѧ��
�� ý �壺��ѧ��Ӧ���ʿμ�
5����ѧ����
������̽�������ۡ������ȡ�
������ѧ����
�����������
һ����ѧ��Ӧ����
1����ѧ��Ӧ���ʵı�ʾ������
2����ѧ����ʽ��
V == ��C/ ��t ��λ��mol/��L·s����mol/��L·min��
3����ѧ��Ӧ���ʵ�Ӧ�á�������
��1��������ʽ�����㷨
��2������
������ѧ��Ӧ�����ʵIJ���
1��ԭ��
2�� ����
3�� ʵ��2-1 ���ۣ�
�ġ����ù�����ϰ����ý��ͶӰ
�塢�κ���ҵ���̲�P18��1��5��
�ڶ�ƪ������ѧ��Ӧ�����ʺ��ȡ���ѧ���
����ѧ��Ӧ�����ʺ�������ѧ���
��һ��ʱ
��άĿ�꣺
֪ʶ�뼼�ܣ�
1��ͨ��ʵ����ʵ�������ʶ��ѧ��Ӧ�����ʼ���Ӱ�����ء�
2. ��Ƚϻ�ѧ��Ӧ���ʵĿ�����
�����뷽����
1. ͨ��ʵ��̽���ܽữѧ��Ӧ���ʵ�Ӱ�����ء�
2������ѧ���Ի�ѧ��ѧ����Ȥ����У���ữѧѧϰ�ļ�ֵ��
���̬�����ֵ�ۣ�
1�� ��ѧ���ճ������еĻ�ѧ�����ʵ���г�����йصĸ����ԭ�����γ�һ���ɺ�� ���ۡ��ɸ��Ե����ԡ��ɼ����ӵĿ�ѧ̽�����̡�
2�� ����ѧ�����õ�ʵ��ϰ�ߣ�����Ĺ۲�������
��ѧ���㣺��ѧ��Ӧ���ʸ���˽�Ӱ�컯ѧ��Ӧ���ʵ����ء�
��ѧ�ѵ㣺Ӱ�컯ѧ��Ӧ���ʵ����ء�
��ѧ�þߣ�ʵ����Ʒ
��ѧ������ͼƬչʾ����ʵ��̽������С�����ۡ��������ܽᡪ��ϰ���
��ѧ���̣�
�¿����룺
[ͶӰ]��ͼ2-17 �������ܴ�Ļ�ѧ��Ӧ
[˼���뽻��]��ͨ��ͶӰ�۲쵽�����ǵ������У��еķ�Ӧ�ܿ죬�еķ�Ӧ�����������෴Ӧ����ϣ���죬��Щ��Ӧϣ����������ϣ���ܿ��Ʒ�Ӧ���ʵĿ���Ϊ�����츣������ͶӰͬѧ�ǽ���һ����ըҩ��ը��������ʴ��ʳ�︯�ܡ������ϻ����ܶ��γɡ�ʯ�ͼ�ú���ɵȷ��棬��һЩ����ϣ���죿��һЩ����ϣ������
[ѧ���]��
[����]��������һ�ھ�Ҫ������������ĵĻ�ѧ��Ӧ���ʵĿ������⡣
[����]�������� ��ѧ��Ӧ�����ʺͼ���
һ����ѧ��Ӧ������
[����]����ͬ�Ļ�ѧ��Ӧ���ʿ���ǧ����𣬿���������Զ��ԣ��ڿ�ѧ�о�����Ҫһ��ͳһ�Ķ�������������Ƚϡ�������ѧ��������˶������á��ٶȡ���ʾ�����ƣ���ѧ��Ӧ�Ĺ��̽��еĿ����á���Ӧ���ʡ�����ʾ��
��ѧ����ݣ�ѧ�������Ķ��̲ģ�����˶����ʵ����⣬��ѧ��ѧ��Ӧ���ʵ�֪ʶ���ݡ�
�����ʣݣ���һλͬѧ�ش�һ�»�ѧ��Ӧ���ʵĶ�����ʲô����
�ۻش�ݣ�ͨ���õ�λʱ���ﷴӦ��Ũ�ȵļ��ٻ�������Ũ�ȵ���������ʾ������������ѧ��Ӧ���п����̶ȵġ�
�۰���ݣ�1. ��ѧ��Ӧ���ʵĸ���õ�λʱ���ﷴӦ��Ũ�ȵļ��ٻ�������Ũ�ȵ���������ʾ��
�����ʣݣ���ѧ��Ӧ���ʵij��õ�λ����Щ�أ���
�ۻش�ݣ�����Ũ�ȣ����ʵ���Ũ�ȣ��ĵ�λ��mol·L-1����ʱ��ĵ�λ��s��min��h�ȣ����ԣ���ѧ��Ӧ���ʵij��õ�λ��mol/(L·s����mol/(L·min)�ȡ���
�۰���ݣ���λ��mol/(L·s)��mol/(L·min)
�����ʣݣ�����Ƿ��ܸ��ݻ�ѧ��Ӧ���ʵĸ�����ɳ�������ѧ����ʽ�أ���
�ۻش�ݣ�Ũ�ȵı仯��һ���æ�c(B)����λʱ���æ�t��ʾ�����Ի�ѧ��Ӧ����v(B)=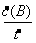
[˼��]��ij��Ӧ�ķ�Ӧ��Ũ����5min����6mol/L�����2mol/L�����Ը÷�Ӧ��Ũ�ȵı仯��ʾ�ĸ÷�Ӧ�����ʱ���ڵ�ƽ����Ӧ�����Ƕ��٣�
[�ش�]��0. 8 mol/(L·min)
[����]������Щ������Ӱ�컯ѧ��Ӧ�������أ�����ͨ��ʵ��������̽����
[ʵ��2-5]��[ʵ��2-6]��
[����]ʵ��Ҫ�㣺1.ʵ��ʹ�õ�˫��ˮŨ�Ȳ��ܹ���ֹ�������������졣
2.�����ǶԱ�ʵ�飬����ע�ⷴӦ�������Ҫ�����ܵ���ͬ���Թܹ��ҲҪ��ͬ��
3.Ϊ����ʵ���Ȥζ�ԣ����Խ���ʵ��Ľ����磺ʹ�������ʢ�к�īˮ��ѹ�������ܵȡ�
[ʵ�����] 1���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ��̽��
������������������ҩƷ���ʵ�鷽���������װ�á�
�ٰ�����װ�ú�ʵ�鲽����жԱ�ʵ�顣�ڼ�¼���۴�������ʵ�����ܵó����ۡ�
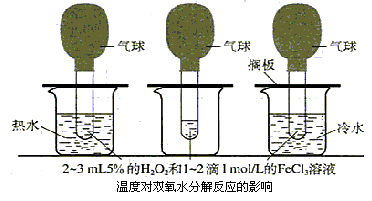
��������������֧��ͬ���Թ��зֱ����2��3 mlԼ5%��H2O2��Ȼ����ÿһ֧�Թ��еμ�2��1 mol/L��FeCl3��Һ��������������С��ͬ��������֧�Թ��ϵ������С�����ͬʱ��ͬʱ���������ձ��й۲�����
2.�����Ի�ѧ��Ӧ����Ӱ���ʵ��̽��
������������������ҩƷ���ʵ�鷽���������װ��(ѡ�ý̲�ʵ��)��
�� ������װ�ú�ʵ�鲽����жԱ�ʵ�顣�� ��¼���� ��������ʵ������ �ó����ۡ�
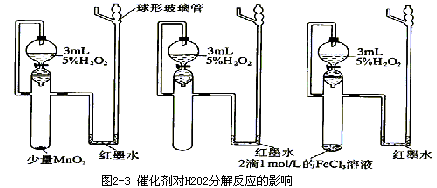
������������������ͬ�Ĵ�������©���зֱ����2��3 mLԼ5%��H2O2��Ȼ����һ֧��
���еμ�2��1 mol/L��FeCl3��Һ����һ֧�Թ��м�������MnO2���塣ͬʱ����֧�Թ��з���©���е�ȫ����Һ���۲��īˮ���������
[С��]����дʵ�鱨�棬�㱨ʵ����ۡ�
[����]: ��ʵ��2-5���ǹ۲쵽�����¶ȣ�H2O2�ֽ������������¶ȣ�H2O2�ֽ����ʼ�С����ʵ��2-6���ǿ���MnO2 ��FeCl3���ӿ���H2O2�ֽⷴӦ�����ʡ�
[̽��]: ����ʵ��Ҳ�����ձ����壬��ͬѧ���ܽ�����߶����ʵ�Ӱ����ɡ�
[�ش�]:��ʦ���ۣ�����϶���
[����]:2���������������������£������¶�������Ӧ���ʣ�ʹ�ô���������Ӧ���ʡ�
[����]:��������������ն�Ҫʹ�ô����͵����¶������Ʒ�Ӧ���ʡ�
[����]:Ӱ�컯ѧ��Ӧ���ʵ��������¶��⣬�Ƿ�������������
[�ش�]:�У�����������Ũ�ȵȡ�
[˼���뽻��]:
1������Ϊʲôʹ�õ���䴢��ʳ�
2��������ʵ���ҽ��л�ѧ��Ӧʱ���������÷��鷴Ӧ�ԭ����ʲô��
3��ʵ���ҽ��л�ѧ��Ӧʱ��ͨ�������巴Ӧ������ˮ�У������Һ���з�Ӧ��Ϊ
ʲô��
4��ʵ���ҳ���Ũ��30%���ҵ�������п����Ӧ��ȡ����������Ӧ���е�һ��ʱ������ݱ��ϡ�٣�п����ʣ�ࣩ���������һЩ�ʵ�Ũ�ȵ�������Һ����������������������ԭ����ʲô��
[�㱨]:�����¶ȣ����鷴Ӧ����������Ӵ���������巴Ӧ������ˮ���������Ӵ��������һЩ�ʵ�Ũ�ȵ�������Һ����������Ũ�ȡ�
[����]:�϶������䣬�ܽᡣ
[����]:�����������������Ӧ��Ũ������Ӧ���ʡ�
[ѧ���Ķ�]:��ѧ��Ұ-����Ĵ�����ͶӰͼ2-18��
˼������������Щ���ԣ�
[С��]:��һ��ѧ������С�ᡣ
[�������]��
������ ��ѧ��Ӧ�����ʺ���
һ����ѧ��Ӧ������
1�� ��ѧ��Ӧ���ʵĸ���õ�λʱ���ﷴӦ��Ũ�ȵļ��ٻ�������Ũ�ȵ���������ʾ��
��λ��mol/(L·s)��mol/(L·min)
2��Ӱ�컯ѧ��Ӧ���ʵ����أ�
�������������������£������¶�������Ӧ���ʣ�
ʹ�ô���������Ӧ���ʡ�
�����������������Ӧ��Ũ������Ӧ���ʡ�
- ����ѧ��Ӧ���ʡ���ѧ��˼
- ��ѧ��Ӧ���ʽ�ѧ����뷴˼
-
��ѧ��Ӧ���ʽ�ѧ��˼
��ѧ��Ӧ���ʽ�ѧ��˼�¿γ���Ľ�ѧ���׳̶�һֱ�Ǻ��Ѱ��յı��ڿλ�ѧ��Ӧ���ʵĸ���������ص����ݶ�Ӱ�컯ѧ��Ӧ���ʵ��������½̲ġ�
-
��ѧ��Ӧ���ʽ�ѧ��˼
��ѧ��Ӧ���ʽ�ѧ��˼�¿γ̳�����quot������������̽�����������quotΪ��Ҫ������ѧϰ��ʽ���ǹ���ʦ���ý�ѧ����Ҫ����̽���ġ�
-
��һ��ѧ����ѧ��Ӧ�����ʡ���ѧ��˼
��һ��ѧ��ѧ��Ӧ�����ʽ�ѧ��˼�����йػ�ѧ��Ӧ���ʵ���Ƶ���кܴ�ĸд������Լ��ڽ�ѧ����һ���Ĵٽ������ڽ��뱾���õ�����֮ǰ��ʦ�ȡ�
- �߿�������ܽ�
-
��ʻԱ��ʦ��ȹ����ܽ�
��ʻԱ��ʦ�����ܽ�20xx��x��x���ĸ�λ��ʦ����λͬ�ʣ�����19xx��μӹ������¼�ʻԱ����������ʮ�������ļ�ʻ����������Ҫ��
-
10�·ݹ����ܽ�
�����ܽ�ϵ��Ӧ�õ�����ͨ�ż���ϵ���ţ��ͼ����ʱ�䣺20xx��x��x�չ����ܽ�20xx��x��x���ɵ���ϵѧ����ͼ����
- �������ʦʵϰ�����ܽ�3000��
-
��ѧ��ʦ��ְ�ƹ����ܽ�
�Թ�������,�ұ��Ż��������̬��Ͷ����ѧУ�ĸ������ȥ,���Ŭ������Լ���˼������ˮƽ�ͽ�ѧҵ������.�µ�ʱ��,�µĽ�������,�̡�