实验论文 乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定
学号:1505100103 班级:应化1005 姓名:苑蕊蕊
摘要:根据乙酰苯胺在各种溶剂中的溶解度与温度的关系,采用重结晶的方法提纯粗乙酰苯胺,得其收率为70%。此外,利用提勒管法测定提纯后乙酰苯胺的熔点,初熔温度114℃,终熔温度为115℃。
关键字:乙酰苯胺;重结晶;提勒管法;熔点
前言:重结晶法是提纯固体有机物的常用方法,通常实验中提取到的乙酰苯胺不纯净,提纯时应把未反应完的苯胺、乙酸、水及不溶性杂质除去。提纯后测其熔点,初步判断是否提纯完全并回收利用。
实验部分:
一、实验目的
1、学习重结晶的基本原理、用途。
2、掌握重结晶提纯固体有机物的操作步骤。
3、学习热过滤和减压过滤的操作技术。
4、了解熔点测定的方法和意义。
二、实验原理
重结晶法是提纯固体有机物的常用方法。固体有机物在溶剂中的溶解度一般随温度的升高而增大,反之溶解度降低。把固体有机物溶解在热的溶剂中制成饱和溶液,然后冷却至室温以下,则原溶液变成过饱和溶液,这时有机物又重新析出晶体。利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。让杂质全部或大部分留在溶液中,从而达到提纯的目的。
乙酸苯胺在水中的溶解度与温度的关系(相关参数)

三:实验仪器与试剂
1、 仪器:电炉、烧杯、玻璃棒、抽滤瓶、布氏漏斗、滤纸、表面皿、b型管、缺口木塞、橡皮筋、铁架台、温度计
2、 试剂:粗乙酰苯胺、活性炭、石蜡油
四:实验流程
a. 重结晶:
1、 选择合适的溶剂--水
2、 制成热饱和溶液(溶剂药过量20%左右,防止热过滤时析出晶体)
3、 活性炭脱色
4、 热过滤,除去不溶性杂质
5、 冷却析出晶体
6、 抽滤,除去母液
7、 晶体的洗涤和干燥
b. 测熔点:
1、 制熔点管
2、 将乙酰苯胺装入毛细管(样品高度约为2mm)
3、 将熔点管固定在温度计上,样品位于温度计水银球中部
4、 向b型管中倒入石蜡油至上叉管处
5、 将b型管固定在铁架台上
6、 将温度计插入软木塞中,置于b型管上
7、 加热b型管,观察样品熔化情况
数据处理及分析:
一、 乙酰苯胺收率
粗乙酰苯胺质量:2.0g
表面皿质量:25.0g
烘干后表面皿及产品质量:26.4g
乙酰苯胺收率:(26.4-25.0)/2.0*100%=70%
二、 乙酰苯胺熔点
初熔温度:114℃ 终熔温度:115℃
熔程:(115-114)℃=1℃
操作要点:
一、减压过滤:剪好的滤纸平铺在漏斗底板上,先用少量溶剂润湿,然后开动抽气泵,使滤纸紧贴在漏斗上,然后缓慢倒入待过滤的混合物,一直抽气至无液体滤出为止。
二、活性炭脱色:活性炭用量的多少视反应液颜色而定,不必准确称量,通常加半牛角勺即可;特别注意不可在溶液沸腾时加活性炭,以防暴沸。
三、热过滤:短颈漏斗必须先在水浴中充分预热,尽量减少产物在滤纸上结晶析出。
四、测熔点时,灯加热的位置,水银球与样品的位置,必须是开口塞,石蜡油的高度与支管上沿水平即可,橡皮筋的位置在油浴之上。
五、在测乙酰苯胺熔点时,一定要在石蜡油冷却降温后才能重新测量。
六、当样品开始塌陷并有液滴出现时为初熔点,固体完全消失呈透明状为终熔点。
结论:
利用重结晶的方法提纯了乙酰苯胺,且收率达70%。测熔点时,初熔温度(114℃)和终熔温度(115℃)相差不大,熔程较小,表明提纯后的乙酰苯胺纯度较高,可回收利用。
参考文献:
【1】罗一鸣,唐瑞仁,有机化学实验与指导,长沙:中南大学出版社,2007,73~82
【2】刘保启,丁天慧,康书凤,刘素娥,分析实验室,1993,12(3)52~57
第二篇:实验四 重结晶及熔点的测定
实验四 重结晶及熔点的测定
预习内容:实验教材P48~53,P54~58。
一、实验目的:
1. 学习通过重结晶提纯固体有机物的原理和方法;
2. 掌握折叠滤纸、热过滤、抽滤等基本操作;
3. 学习并掌握毛细管法测熔点的方法。
二、仪器和药品
仪器:烧杯(250mL)、表面皿、无颈漏斗、烘箱(公用)、减压水泵(公用)、熔点管、水银温度计等;
药品:粗苯甲酸、活性炭、液体石蜡等;
其他:滤纸(热过滤用,抽滤用)、玻棒、沸石等。
三、实验原理及教师讲解要点:
1.重结晶的基本原理:
重结晶是纯化固体物质的一种方法。它是利用在不同温度下被提纯物质与杂质在溶剂中的溶解度不同,将杂质分离出去的提纯方法。
大多数有机物的溶解度都随着温度的升高而增大。选择溶剂,在较高温度(接近溶剂的沸点)下,制成被提纯有机物的饱和或接近饱和的浓溶液,趁热过滤后,让被提纯物从过饱和溶液中的以结晶析出,而杂质则全部或大部分仍留在溶液中,或者在热过滤时被分离出去。
重结晶只适用于提纯杂质含量在5%以下的固体有机物。(Why?)
重结晶时,应根据下列条件选择溶剂:
(1) 不与被提纯物质起化学反应;
(2) 对被提纯物质的溶解度随温度变化较大;(Why?)
(3) 对杂质的溶解度非常大或非常小;(Why?)
(4) 易挥发,易除去;
(5) 能给出较好的结晶。
在实际的选择过程中,主要是根据相似相溶原理,查阅数据手册,选出几种溶剂用试管进行实验观察,选出符合上述五个条件的溶剂。必要时,可使用混合溶剂。
2.折叠滤纸的折叠:(略)
3.热过滤的操作和技巧:准备充分,快速协调,趁热过滤。
4.测熔点的原理和方法:
一般认为固态物质受热后变为液体时的温度,就是该物质的熔点。实验证明,同一物质在不同的压力下,熔化温度并不完全相同。熔点的严格定义为:物质的固液两态在大气压力下达到平衡状态时的温度。
有机物的熔点通常用毛细管法来测定。实际上由此法测得的熔点数据不是一个温度点,而是一个熔程,即样品从开始熔化到完全熔化为液体的温度范围。
纯的固态物质通常都有固定的熔点(熔程约0.5°C)。如有其他物质混入,则对其熔点有显著的影响:熔点降低,熔程拉长。因此,可借助熔点的测定来定性地判断固体样品的纯度。
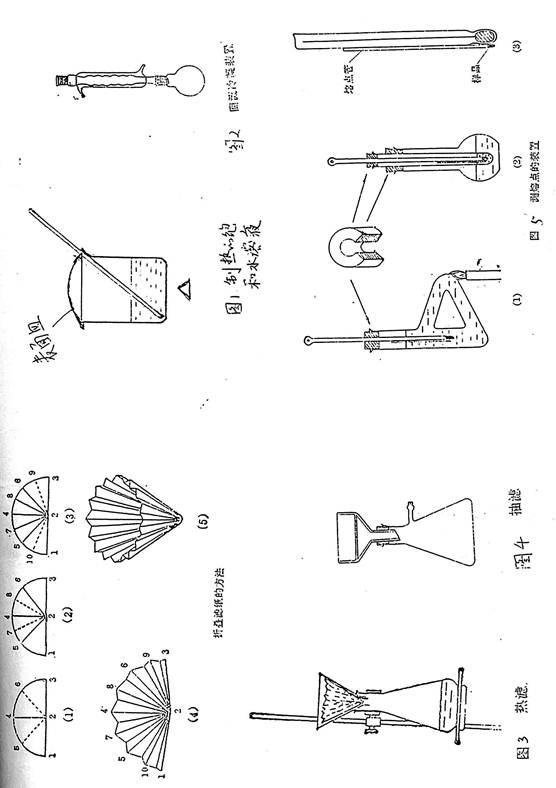
四、仪器装置:
重结晶各种装置如图1,图2,图3,图4所示。
图1适用于用水做溶剂的情况,图2适用于用其他低沸点有机溶剂。
测熔点的装置见图5。
五、操作步骤:
(一)重结晶的简单过程为:
溶解®脱色®热过滤®冷却®抽滤,洗涤®干燥®称重,计算产率。
最后,还要用测熔点的方法检查产品纯度是否达到要求。
1.溶解:
250mL烧杯中:3g粗苯甲酸+80mL水+2粒沸石,盖上表面皿,用小火加热至沸,其间可用玻棒搅动。观察样品是否完全溶解,若有未完全溶解的样品,则需补加水(记下补加水的体积),直到样品完全溶解为止。再加入总用水量12%的水[1],加热至沸。移去火源,稍冷,加入适量活性炭[2],搅拌,沸煮5~10min,待热过滤。对易挥发性溶剂要用回流装置。
2.热过滤:
从烘箱中取出预热好的无颈漏斗,将事先叠好的折叠滤纸放入其中,并用少量热水润湿[3],将上述热溶液趁热过滤。
热过滤时,无颈漏斗上可加盖表面皿,以防止溶剂挥发,并有保温作用。使用有机溶剂重结晶时,周围火源要熄灭。
3.结晶:
骤冷得小颗粒,自然冷却得大颗粒。有时有油状物或胶状物存在,结晶不易析出,可采用搅拌、加入晶种、磨擦仪器内壁、过滤等办法使晶体析出。
4.抽滤,干燥。
5.称重,计算收率。
数据记录:
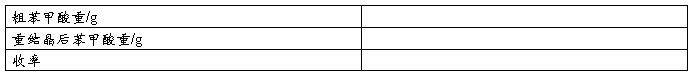
(二)测熔点:
毛细管法测熔点的主要过程为:准备热浴®装样®加热,观察®读数。
1.准备热浴:
设计熔点浴的原则是使样品受热均匀,通常有b形管和双浴式,本实验采用双浴式。
首先,选择大小合适的橡皮塞,在中心处用打孔器打孔以插入温度计,并在边缘开一小槽以接通大气。然后,在b形管中倒入适量的浴液。常用的浴液有:浓硫酸、液体石蜡、甘油、机油、硅油等。本实验采用腐蚀性小的液体石蜡做浴液。
2.装样:
将0.1g样品在表面皿上研细[4],堆起来,将事先准备好的熔点管的管口朝下,插入样品粉未中,然后管口朝上利用自由落体运动使样品粉未落入并填实管底[5],如此反复几次,装样高度为2~3mm。最后擦去管外粘附的粉未,将熔点管固定在水银温度计上,注意使样品处于水银球的中部。
3.测定熔点:
将带有样品的温度计插入b形管中,其水银球位于b形管上、下两叉口的中间。用小火加热b形管远离样品的一端,浴液开始对流循环,温度计读数上升。加热速度开始可稍快,接近熔点时必须调整火焰,放慢升温速度(约每分钟上升1°C),直到样品全部熔化。
记录样品的萎缩温度、初熔温度、全熔温度。平行两次实验[6]。
对未知样品,先要进行粗测,以知道样品的大致熔点,再按已知样进行两次平行实验。
数据记录:
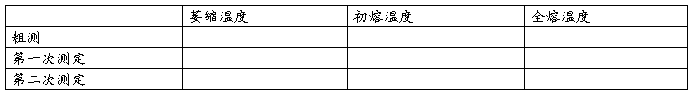
六、注释:
[1]为了防止热过滤时,样品过早析出而造成损失,又不至于由于溶剂用量过多而造成溶解损失,经验结果表明,溶剂的实际用量应为理论用量的120%。
[2]活性炭用量过少时脱色效果不好,但用量过大时,会吸附样品,损失收率。一般活性炭用量为样品量的1~5%。
[3]使用有机溶剂时,则要用相应的热溶剂润湿滤纸。
[4]样品一定要研细,否则装样时不易填紧。
[5]若装样时未填紧,会在样品中产生小的空气室,使样品受热不均匀,熔程拉长。
[6]每次测定都必须用新的熔点管重新装样测定;每次测定时浴液温度都要降至熔点30°C以下。
七、回答思考题:
1.重结晶一般包括哪几个操作步骤?各步操作的目的是什么?
答:重结晶一般包括:溶解、脱色、热过滤、冷却结晶、抽滤、干燥等操作步骤。各步操作的目的如下:
熔解:配制接近饱和的热溶液;
脱色:使样品中的有色杂质吸附于活炭上,便于在热过滤时将其分离;
热过滤:除去样品中的不溶性杂质;
冷却结晶:使样品结晶析出,而可溶性杂质仍留在溶液中;
抽滤:使样品可溶性杂质与样品分离。
干燥:使样品结晶表面的溶剂挥发。
2.在什么情况下需要加活性炭?应当怎样加活性炭?
答:样品颜色较深时,需要加入活性炭进行脱色。为了防止爆沸,加活性炭时应将热溶液取下稍冷后再加。
3.为什么热过滤时要用折叠滤纸?
答:增大过滤面积,加快过滤速度。
4.为什么利用重结晶只能提纯杂质含量低于5%的固体有机物?
答:如果样品中杂质含量大于5%,则可能在样品结晶析出时,杂质亦析出,经抽滤后仍有少量杂质混入样品,使重结晶后的样品纯度仍达不到要求。
-
实验6_乙酰苯胺熔点的测量
实验六乙酰苯胺等物质熔点的测量一实验目的1掌握毛细管法测定乙酰苯胺等物质的熔点2掌握用测量熔点的方法鉴定物质的种类和检验物质的纯度…
- 熔点的测定实验报告
-
实验三:乙酰苯胺的重结晶及熔点的测定
实验二乙酰苯胺的重结晶及熔点的测定一实验目的1学习重结晶的基本原理用途2掌握重结晶提纯固体有机物的操作步骤3学习热过滤和减压过滤的…
-
1乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定实验目的1熟悉重结晶的基本操作2了解乙酰苯胺的结晶制备3了解熔点测定的原理4掌握毛细管法测定熔点的操作…
-
实验论文 乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定学号1505100103班级应化1005姓名苑蕊蕊摘要根据乙酰苯胺在各种溶剂中的溶解度与温度的关系采用…
-
实验三:乙酰苯胺的重结晶及熔点的测定
实验二乙酰苯胺的重结晶及熔点的测定一实验目的1学习重结晶的基本原理用途2掌握重结晶提纯固体有机物的操作步骤3学习热过滤和减压过滤的…
- 熔点的测定实验报告
-
实验6_乙酰苯胺熔点的测量
实验六乙酰苯胺等物质熔点的测量一实验目的1掌握毛细管法测定乙酰苯胺等物质的熔点2掌握用测量熔点的方法鉴定物质的种类和检验物质的纯度…
-
乙酰苯胺的制备实验报告南昌大学
南昌大学有机化学实验报告学生姓名彭以振学号专业班级实验类型验证综合设计创新实验日期20xx年9月28日实验地点同组学生姓名指导教师…
-
1乙酰苯胺的重结晶及熔点的测定
乙酰苯胺的重结晶及熔点的测定实验目的1熟悉重结晶的基本操作2了解乙酰苯胺的结晶制备3了解熔点测定的原理4掌握毛细管法测定熔点的操作…
-
乙酰苯胺的制备(实验报告实验总结范文模板)
(实验报告)乙酰苯胺的制备【目的要求】⑴熟悉氨基酰化反应的原理及意义,掌握乙酰苯胺的制备方法;⑵进一步掌握分馏装置的安装与操作;⑶…