实验二 蒸馏与沸点的测定
时间: 年 月 日 地点:生科院B108实验室 温度:
实验名称:蒸馏与沸点的测定 实验性质:基础 实验要求:必修
实验二蒸馏与沸点的测定
一. 实验目的
1.掌握蒸馏的基本原理和操作方法
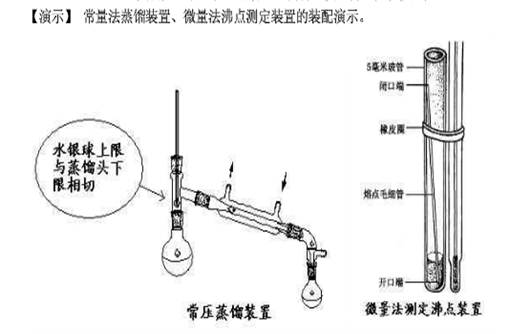
2.学习常量法和微量法测定沸点的原理和方法,并明确实用意义.
二. 实验内容
1.液体的蒸汽压与温度有关,将液体加热,其蒸汽压随温度升高而增大,当液体的蒸汽压增大至与外界液面的总压力(通常是大气压力)相等时,开始有气泡不断从液体内部逸出,即液体沸腾,此时的温度为该液体的沸点。
沸点通常指101.3kPa(760mmHg)压力下沸腾的温度。在其他压力下应注明压力如bPH2O=50℃/12.3Pa
2.蒸馏就是将液体混合物加热到沸腾,使液体气化,然后将蒸汽冷凝为液体的过程。这是分离纯化液体物质的一种重要方法,混合液的沸点差别大于30℃可以完全蒸馏分离,
3.沸程(沸点距)第一滴馏出液开始的温度到蒸发完全时的温度范围。纯的液体有机物在一定压力下具有固定的沸点(物理常数)。纯液体沸程0.5℃~1℃,混合液沸程长。共沸混合物有些也具有固定沸点,例如:95.6%乙醇和4.4%水混合物沸点是78.2℃ 。
4.常见沸点的测定方法有:
常量法:蒸馏,液体用量大,10mL以上。
微量法:沸点管,液体用量少,纯的液体。
三. 实验器材
蒸馏烧瓶,冷凝管,接收瓶,牛角管,温度计,沸点管,电热套,提勒管,酒精灯,橡皮管
四. 操作步骤
(一)蒸馏
1.安装蒸馏设备:
(1)装置主要由汽化、冷凝和接收三大部分组成
(2)仪器有蒸馏烧瓶、冷凝管、接收瓶等
(3)安装原则:从头到尾顺序,且使一起处于同一个垂直桌面的平面内
(4)注意:
a.温度计水银球的位置,其上限应与烧瓶支管的下限处于同一个水平线;
b.冷凝水的方向(下进上出);
c. 整套装置中各仪器连结时不能扭曲受力,安装牢固后开始试验。
2. 加料:待测液装入烧瓶(小于2/3)→加入助沸物→装好温度计→检查装置气密性
注意:助沸物的作用,若忘加,不可在加热接近沸点时加,否则引起剧烈暴沸。
3. 加热:接通冷却水,引入水槽,开始加热→调小火待水银球上液滴与蒸汽两者温度平衡→稍大火,控制蒸馏速度,1-2滴/秒
4. 收集馏分:前馏分更换或弃去,记录沸程(开始,结束的温度)
5. 蒸馏完毕,停火→移去热源→待稍冷关冷水→拆除仪器
(二)沸点的测定
1.安装设备(提勒管,酒精灯);
2.沸点管内加几滴待测液体,倒插测沸点内管,加热提勒管
3.气泡连续不断外冒,即停止加热
4.记下看到气泡不再冒出而液体刚要进入沸点管时的即刻温度
5.测3 次,取平均值
注意:a.加热时不能太快,被测液体不能太少,以防液体全部汽化
b.沸点管内空气尽量赶干净(沸点管:毛细管一端封口,一端朝下在套管)
c.多测几次,误差不得超过1℃
五. 思考题:
1. 微量法测沸点时,如遇一下情况将会如何:
a、沸点内管空气未除干净 b、沸点内管未封好 c、加热太快
2. 测得某种液体有固定的沸点,能否认为该物质是单纯的物质,为什么?
3. 微量法和常量法有何差异,为什么会有这种情况?
4. 加入助沸物的正确方法?
5. 微量法测量沸点的原理?
第二篇:实验二:乙醇的蒸馏及沸点的测定
实验二:乙醇的蒸馏及沸点的测定
一、实验目的
1.了解蒸馏提纯液体有机物的原理、用途。
2.掌握蒸馏提纯液体有机物的操作步骤。
3.了解沸点测定的方法。
4.了解折光率测定的方法和意义。
二、实验原理
将液体加热至沸,使液体变为气体,然后再将蒸气冷凝为液体,这两个过程的联合操作称为蒸馏。
蒸馏是分离和纯化液体有机混合物的重要方法之一。当液体混合物受热时,由于低沸点物质易挥发,首先被蒸出,而高沸点物质因不易挥发或挥发的少量气体易被冷凝而滞留在蒸馏瓶中,从而使混合物得以分离。蒸馏法提纯工业乙醇只能得到95%的乙醇,因为乙醇和水形成恒沸化合物(沸点78.1℃),若要制得无水乙醇,需用生石灰、金属钠或镁条法等化学方法。
三、主要试剂及产品的物理常数:(文献值)
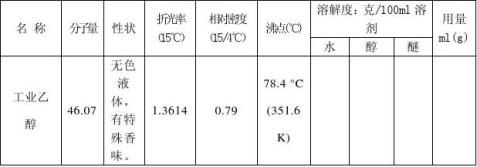
四、实验装置图
六、数据处理
实际产量=
回收率=
nDt =
nD20=
七、思考题:
1
1.什么叫沸点?液体的沸点和大气压有什么关系?
2.蒸馏时加入沸石的作用是什么?如果蒸馏前忘记加沸石,能否立即将沸石加至将近沸腾的液体中?当重新蒸馏时,用过的沸石能否继续使用?
3.如果液体具有恒定的沸点,那么能否认为它是单纯物质?
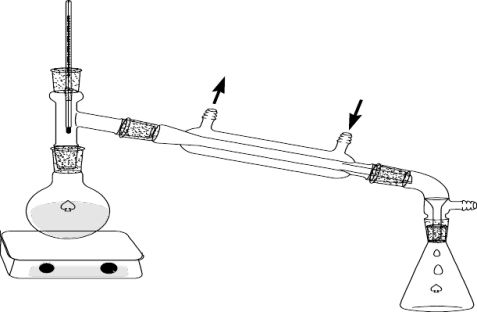
五、操作流程和实验记录
工业乙醇 + 沸石 +
蓝墨水
时间 实验记录:
100ml圆底烧瓶
工业乙醇=? 沸石=? 蓝墨水=?
第一滴馏出液流出时t1=?℃

工业乙醇
蒸馏结束时t2=?℃
沸程?(后馏分的起始温度)
称量

前馏分=总重-瓶重 后馏分=总重-瓶重
2
产品状态? nDt=?
-
实验五 蒸馏和沸点的测定
实验五蒸馏和沸点的测定一实验目的1了解沸点测定的原理和意义2掌握常量法测定沸点的原理方法和操作二实验原理1蒸馏的概念分类2沸点的定…
-
乙醇的蒸馏及沸点测定 实验报告
报告题目:乙醇的蒸馏及沸点测定实验报告报告题目:乙醇的蒸馏及沸点测定专业班级:生物工程指导老师:***学生姓名:**学号:**20…
-
有机化学实验三蒸馏及沸点的测定
有机化学实验三蒸馏及沸点的测定实验三蒸馏及沸点的测定一实验目的1了解测定沸点和蒸馏的意义2掌握蒸馏法测定沸点的原理和操作方法3掌握…
-
乙醇的蒸馏与沸点的测定实验方案
乙醇的蒸馏与沸点的测定工业乙醇的蒸馏与沸点的测定一实验目的1掌握简单蒸馏与分馏的操作技术2掌握微量法测定沸点的方法实验原理液体物质…
-
有机化学实验-----蒸馏及沸点的测定技术
实验报告姓名班级同组人项目蒸馏及沸点的测定技术课程学号一实验目的1了解蒸馏和沸点测定的基本原理和意义2掌握蒸馏和沸点测定的操作技术…
-
有机化学实验-----蒸馏及沸点的测定技术
实验报告姓名班级同组人项目蒸馏及沸点的测定技术课程学号一实验目的1了解蒸馏和沸点测定的基本原理和意义2掌握蒸馏和沸点测定的操作技术…
-
乙醇的蒸馏及沸点的测定
大学化学基础实验II实验报告课程名称物理化学实验实验名称乙醇的蒸馏及沸点的测定姓名张玉学号1108110191专业化学工程与工艺班…
-
乙醇的蒸馏及沸点测定 实验报告
报告题目:乙醇的蒸馏及沸点测定实验报告报告题目:乙醇的蒸馏及沸点测定专业班级:生物工程指导老师:***学生姓名:**学号:**20…
-
熔点.沸点的测定实验报告
有机化学实验报告实验学专班姓指导日名称院业级名教师期熔点的测定沸点的测定化学工程与工艺化工133班王腾飞学号134020xx330…
-
实验二:乙醇的蒸馏及沸点的测定
实验二乙醇的蒸馏及沸点的测定一实验目的1了解蒸馏提纯液体有机物的原理用途2掌握蒸馏提纯液体有机物的操作步骤3了解沸点测定的方法4了…
-
有机化学实验报告实例熔沸点的测定
有机化学实验报告姓名班级学号郑州轻工业学院化工系实验名称熔点沸点的测定姓名班级学号实验日期实验目的1掌握用齐列管法测定有机化合物熔…