羧酸及其衍生物的物理性质
目前位置:首页—>羧酸及其衍生物—>K2 羧酸及其衍生物的物理性质
羧酸及其衍生物的物理性质
教学目标:
1.了解羧酸一般物理性质及其影响因素。
2.掌握羧酸及其衍生物 IR 特征。
教学重点:IR特征
教学安排:B5, K1—>K2;10min
一、一般物理性质
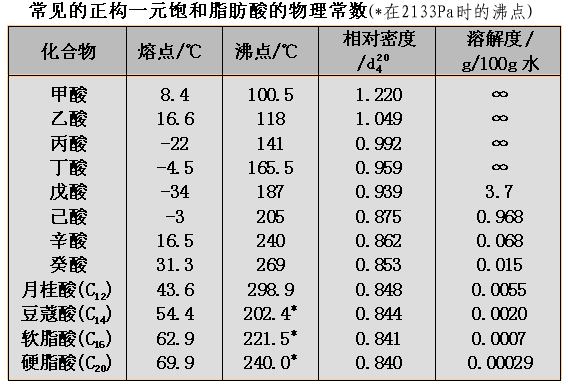
低级的一元羧酸(C1-C9)是液体,C1-C3的羧酸有一定挥发性,并且有较强的刺激性;C4-C9的羧酸不同程度地具有腐败气味,并且是具有一定粘度的油状液体。C10以上的羧酸则是石蜡状固体,气味很小。二元羧酸以及芳香族羧酸都是晶体。
羧酸的沸点较分子量相近的醇高,这是由于羧基的强极性和分子间的氢键所致。在气态时,甲酸、乙酸等是以双分子缔合形态出现。与烷烃相似,偶数碳原子的羧酸其熔点要比与之相邻的奇数碳原子羧酸的熔点高。
C1-C4 的正构羧酸由于分子的极性大,与水分子可很好地形成氢键,所以它们的溶解度很大;但正戊酸在水中的溶解度只有3.7g/100g水。高级的一元酸在水中的溶解度非常小,甚至不溶于水。常见的二元酸在水中都有很好的溶解度。
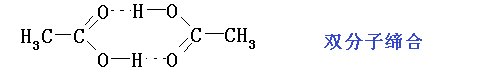
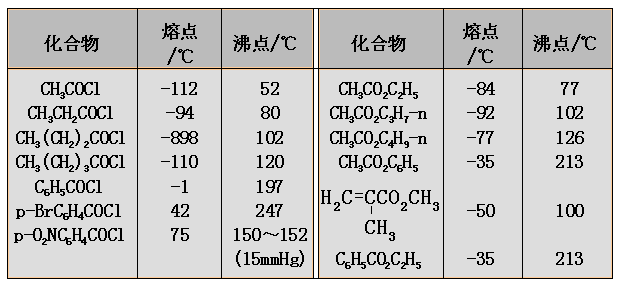
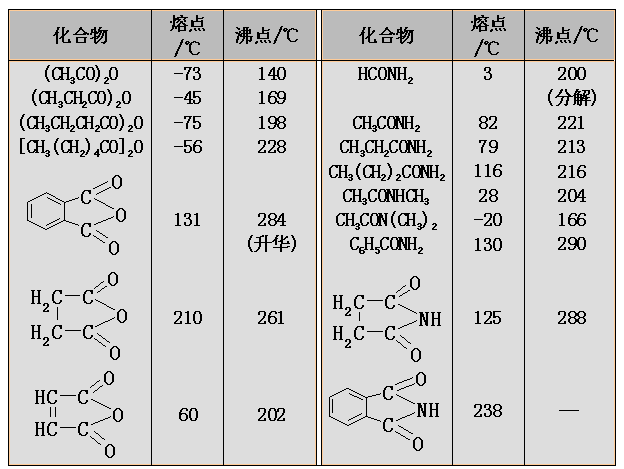
酰氯、酸酐和酯的沸点与分子量相近的醛酮大体相近,酰胺由于分子间可形成氢键,而具有很高的沸点。低级的酯和酰胺在水中有一定的溶解度;但低级的酰氯和酸酐在水中容易发生水解。一般情况下,酰氯和酯的熔点比较低,酰胺的熔点较高,不同的酸酐的熔点变化是较大的。
低级的酰氯和酸酐都有刺鼻气味,而低级的酯却有芳香气味并可用作香料;低级的酰胺是良好的非质子型极性溶剂。常见的羧酸及其衍生物在一般的有机溶剂中有良好的溶解性。
一些常见的羧酸衍生物的熔点和沸点如下表:
二、光波谱性质
由于羧酸分子的羟基之间可形成氢键,在 3300cm-1 处有非常强而宽的羟基的特征峰,并且该峰可含盖烃基中的 CH3 和 CH2 的 C-H 键伸缩振动吸收峰的区域;在 2500-2700cm-1 处,还有 O-H 键的伸缩振动。另外,OH 的弯曲摆动(面外摇摆)在 925cm-1 处有一个比较宽的特征吸收峰。脂肪族羧酸中的羰基在 1700-1725cm-1 处有中等强度的吸收,而芳香族羧酸的羰基在 1680-1700cm-1 处有吸收。在羧酸的各种衍生物中,羰基在红外光谱中出现吸收的位置是不同的,羰基越缺电子,吸收波数越高;羧酸根据负离子的红外吸收波数是最低的。 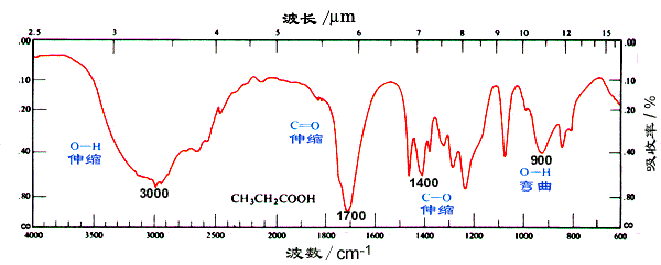
丙酸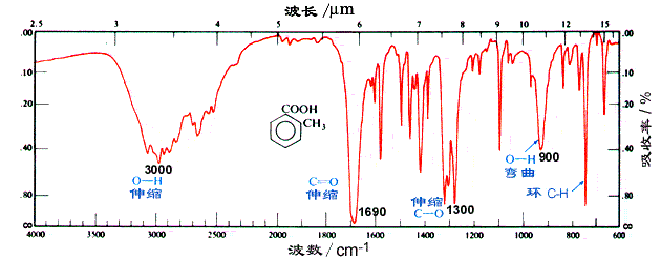
邻甲苯甲酸
邻甲苯甲酰氯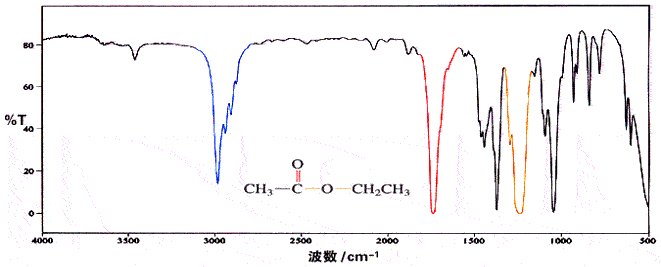
乙酸乙酯
邻甲苯甲酰氯
乙酸乙酯
x羰基的影响下,其化学位移多在δ=2.2-2.5。
三、关键词
羧酸的物理性质、羧酸的光波谱性质
第二篇:烃的衍生物第三单元羧酸的性质和应用
烃的衍生物第三单元羧酸的性质和应用
【学习目标】
1.通过对乙酸性质的探究活动,了解羧酸具有酸性的原因,认识酯化反应的特点。
2.认识甲酸的性质
【教学的重点和难点】
乙酸的性质,甲酸的性质
【复习提问】乙醛能够用被氧气氧化成乙酸,写出反应的化学化学方程式
所得有机物为 它的官能团是 ,含有该官能团的一类物质我们称之为 。
一、羧酸的概念及结构
1、概念:
2、官能团:
3、分类:
(1)根据烃基不同可分为:
(2)根据羧基数目不同可分为:
(3)根据烃基中碳原子数目多少可分为:
4、饱和一元羧酸的分子通式为:
5、乙酸的分子式 结构式 结构简式
二、羧酸的物理性质:
1、乙酸的物理性质:
乙酸俗称 ,为 色 体,有强烈的 气味,易溶于 ,0℃时,乙酸凝结成冰一样的物质,所以纯净的乙酸又叫做 。
2、饱和一元羧酸的物理性质:
随碳原子数增多,熔沸点升高,在水中的溶解度降低,C1~C4的羧酸能与水互溶,(酸性减弱)。
三、羧酸的化学性质:
1、酸的通性:
乙酸可以使湿润的蓝色石蕊试纸
用方程式表示下列过程:
① 乙酸在水中电离:
② 与金属钠的反应:
比较乙酸,乙醇,苯酚,水与金属钠反应的剧烈程度,分析原因:
③ 与氧化铜的反应:
④ 与NaOH的反应:
⑤ 与碳酸钠的反应:
比较乙酸,碳酸,苯酚的酸性强弱:
2、酯化反应:
乙酸乙酯的生成:
反应方程式:
反应特点:
根据乙酸与乙醇酯化反应的原理,对比乙酸乙酯发生水解时的共价键断裂的情况,两者之间有何联系?
【练习】:完成下列酯化反应:
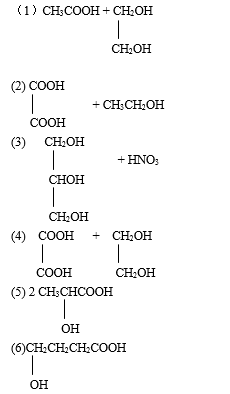
3、缩聚反应:
通过酯化反应,可以得到高分子化合物,如聚对苯二甲酸乙二酯的生成
比较加聚反应与缩聚反应的区别:
【练习】:对苯二甲酸和1,4-丁二醇作用生成高分子酯
四、甲酸的结构和性质:
甲酸俗称 ,分子式为 ,结构式 ,结构简式 ,甲酸中既有
,又有 。
【问题解决】根据甲酸的结构预测它可能具有的性质。归纳整理。
【课后巩固】:
1.某有机物既能被氧化,又能被还原,且氧化后与还原后的产物能发生酯化反应,所生成的酯又能发生银镜反应,则该有机物是 ( )
A.CH3OH B.HCHO C.HCOOH D.CH3CH2CHO
2.在下列物质中,既能使溴水褪色,又能使酸性高锰酸钾溶液褪色,还能使紫色石蕊试液变为红色的是 ( )
A.苯 B.苯酚 C.丙烯酸 D.甲酸甲酯
3.只用水就能鉴别的一组物质是 ( )
A.苯、乙酸、四氯化碳 B乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯 D.苯酚、乙醇、甘油
4.用括号内的试剂和分离方法,除去下列物质中的少量杂质,正确的是 ( )
A.乙酸乙酯中的乙酸(饱和Na2CO3溶液,分液)
B.苯中的甲苯(溴水,分液)
C.溴苯中的溴(KI溶液,分液)
D.乙醇中的乙酸(NaOH,蒸馏)
5.重氮甲烷(CH2N2)能与酸性物质反应:R-COOH+CH2N2→R-COOCH3+N2。下列物质中能与重氮甲烷反应但产物不是酯的是 ( )
A.H-CHO B.C6H5OH C.C6H5CH2OH D.C6H5COOH
6.某物质中可能有甲醇、甲酸、乙醇、甲酸乙酯几种物质中的一种或几种,在鉴定时有下列现象:①有银镜反应 ②加入新制Cu(OH)2悬浊液,沉淀不溶解 ③与含有酚酞的氢氧化钠溶液共热时发现溶液中红色逐渐变浅至无色,下列叙述中正确的是 ( )
A.有甲酸乙酯和甲酸 B.有甲酸乙酯和乙醇
C.有甲酸乙酯,可能有甲醇 D.几种物质都有
7.以乙醇为原料,用下述6种类型的反应:①氧化;②消去;③加成;④酯化;⑤水解;⑥加聚,来合成环乙二酸乙二酯()的正确顺序是 ( )
A.①⑤②③④ B.①②③④⑤ C.②③⑤①④ D.②③⑤①⑥
8. 胆固醇是人体必需的生物活性物质,分子式为C27H46O。一种胆固醇酯是液晶材料,分子式为C34H50O2。生成胆固醇的酸是:( )
A.C6H50O2 B.C6H5COOH C.C7H15COOH D.C6H5CH2COOH
9 .有A、B、C、D、E五种有机物,分别由碳、氢两种元素或碳、氢、氧三种元素组成。五种有机物各取0.1mol,分别完全燃烧,都能得到4.48L(标准状况下)二氧化碳。
(1) A氧化能得到B,E氧化能得到A;
(2) D在一定条件下跟水反应能得到E,D跟氢气加成得到C;
(3) B易溶于水,水溶液呈酸性。
则这五种有机物的结构简式分别为:A___________,B___________,C___________,D___________,E___________。
10.酸牛奶中含乳酸,
⑴乳酸跟足量金属钠反应的化学方程式 ;
⑵乳酸与少量碳酸钠溶液反应的化学方程式: ;
⑶乳酸在浓硫酸存在下,两分子相互反应生成链状化合物的化学方程式
;
⑷乳酸在浓硫酸存在下,两分子相互反应生成环状化合物的化学方程式
;
⑸乳酸在浓硫酸条件下,分子内脱水且脱水后的产物能使溴水褪色,则此产物的结构简式为
⑹乳酸在浓硫酸条件下,分子内脱水且脱水后的产物不能使溴水褪色,则此产物的结构简式为
11.分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
为了合成该物,某实验室的科技人员设计

了下列合成路线:
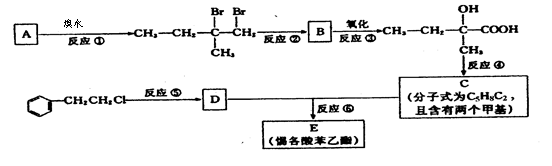
试回答下列问题:
(1)试写出:A的结构简式 ;B的结构简式 。
(2)反应②中另加的试剂是 ;反应④的一般条件是 。
(3)试写出反应生成E的化学方程式: 。
(4)上述合成路线中属于取代反应的是 (填编号)。
-
实验四 醇、酚、醛、酮、羧酸以及衍生物的性质
实验报告学院第二临床医学院专业临床医学年级级班级班姓名学号日期20xx55实验课程有机化学实验实验名称实验四多元醇酚醛酮羧酸以及衍…
-
醛、酮、羧酸及其衍生物的性质和乙酸乙酯的制备
实验二醛、酮、羧酸及其衍生物的性质和乙酸乙酯的制备(一)醛、酮、羧酸及其衍生物的性质课时数:4学时教学目标:通过本项目的学习,使学…
-
羧酸及其衍生物的性质
实验四羧酸及其衍生物的性质一实验目的:1验证羧酸及其衍生物的性质.2了解肥皂的制备原理和性质二实验内容:1羧酸的性质2羧酸衍生物的…
-
羧酸及其衍生物的性质
羧酸及其衍生物的性质目的验证羧酸及其衍生物的主要化学性质原理羧酸最典型的化学性质是具有酸性酸性比碳酸强故羧酸不仅溶于氢氧化钠溶液而…
-
苏州大学有机化学实验-羧酸及其衍生物的性质
苏州大学化学化工学院课程教案实验名称羧酸及其衍生物的性质教学目标知识与技能通过实验验证羧酸及其衍生物的性质进一步加深对羧酸及其衍生…