盐酸标准溶液的配置及标定
实验题目:盐酸溶液浓度的标定
一、 实验目的:
1、掌握酸式滴定管的使用和操作方法;
2、学会酸碱溶液浓度的标定方法;
3、学会使用电子天平“差重法”称量。
二、实验原理:
滴定反应Na2CO3 + 2HC l = 2NaCl + CO2 + H2O
106g 2mol
W(g) (C(HCl)·V/1000)mol
C(HCl) =(2 W×1000)/(106 ×V)=1000W/53V
基准物—硼砂(Na2B4O7·10H2O),Na2CO3(无水,放于干燥器内,本次实验用); 指示剂—甲基橙
终 点:黄色—变为橙色(pH=3.1—4.4)
三、仪器及试剂:
HCl标准溶液,无水Na2CO3,甲基橙,酸式滴定管,烧杯,锥形瓶;电子天平。
四、实验步骤:
1、计算Na2CO3的称量范围;
2、用“差重法”准确称取称量范围的Na2CO3于洁净的锥形瓶中;
3、在锥形瓶中加入约30 cm3纯水,在温水浴中加热,摇动使之完全溶解,并滴加2~3滴甲基橙;
4、用50 cm3的酸式滴定管装入标准盐酸,调节好刻度,记下初读数后,左手控制玻璃塞,右手摇动锥形瓶使锥形瓶中液体作圆周运动,控制好滴速,当黄色—变为橙色(即为滴定终点),停止滴定,取下滴定管,正确读数(终读数)并记下读数,读数结果小数点后保留两位。
5、再分别称取称量范围的Na2CO3于洁净的锥形瓶中,按上述方法重复两次。
五、数据记录与数据处理:
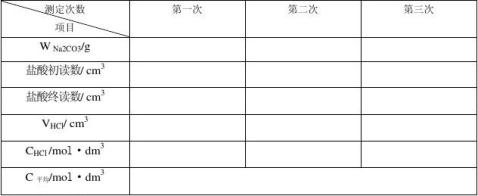
六、结果与讨论
实验注意事项:
1、计算Na2CO3的称量范围Na2CO3 + 2HC l = 2NaCl + CO2 + H2O
106g 2mol
W(g) 0.2×(20~30)/1000)mol
W =0.2120~0.3180g即称取(0.2~0.3g)
2.用差量法准确称取(0.2~0.3g)Na2CO3于锥形瓶中
(1)将锥形瓶用自来水冲洗,再用纯水淌洗三遍。(2)称量瓶的取放要用纸条,不能用手直接拿。(3)用差量法称一份在称量范围的Na2CO3与锥形瓶中(4)不能有Na2CO3洒在锥形瓶外(5)记录数据(四位有效数字)
3.配制Na2CO3溶液
(1)在锥形瓶中加入30 cm3纯水(2)在温水浴中加热,摇动使之完全溶解
4. 酸式滴定管的准备
(1)检查玻璃塞是否配套,有无橡皮套。
(2)用自来水冲洗,然后装满自来水后放在滴定管架上约2分钟,观察有无漏水,若漏水更换(或重新涂油脂)。
(3)若不漏水用自来水、纯水分别淌洗三遍,再用盐酸标准溶液溶液淌洗三遍(每次5~10 cm3左右)。(三三步骤)
(4)将盐酸标准溶液装入洗好的酸式滴定管中,装到零刻度线以上。
(5)检查滴定管玻璃塞上下有无气泡,若有气泡,把气泡排出。
(6)将盐酸标准溶液弯月面最低点调节到零刻度或零刻度以下。
5. 盐酸标准溶液的标定
(1)往锥形瓶中加入1~2滴甲基橙指示剂
(2)记录滴定前滴定管内盐酸标准溶液体积读数,读数时保持滴定管垂直,数据的小数点后有两位。
(3)左手控制玻璃塞,右手摇动锥形瓶使锥形瓶中液体向一个方向作圆周运动,边滴边摇,刚开始滴定时滴定速度可以较快,当黄色消失较慢时,一滴一滴的滴定,滴一滴摇匀了,观察颜色,直到溶液由红色变为橙色,停止滴定。滴定过程中盐酸标准溶液不能洒到锥形瓶外。
(4)记录滴定后滴定管内盐酸标准溶液体积读数,读数时保持滴定管垂直,记录数据,小数点后有两位。
6、电子天平使用方法及注意事项
注意事项:
(1)FA/JA1004型电子天平最大称量为100g,称量时不能超过此值;
(2)腐蚀物不能与称量盘接触;
(3)不能随意开关电子天平;
(4)其它功能键(RNG UNT INT ASD CAL PRT COU)供维修人员调校天平使用,未经允许,不得使用;
(5)由于天平在使用时需要较长时间预热,故请同学们在使用后不用关机;
使用方法:
(1)轻按一下“ON

2秒后,显示天平的型号
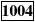

后是称量模式
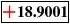
(2)置称量瓶或容器于称量盘上(最好是正中间)(3)然后
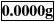
轻按去皮键,显示消隐,随即出现全零状态,容器质量已去除,即“去皮重”:
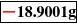
再轻按去皮键,显示器为全零,即天平清零;当从容器中倒出一部分,再把容器放回称量室,就出现一个负值,此负值即为
从容器中倒出的那部分的质量(在实际操作过程中,我们就是这样称量的)
(4)从干燥器中取称量瓶的方法是:左手护着干燥器的主体,右手握住干燥器的盖子,向一个方向平推即打开了干燥器的盖子(不能向上直接提),用一张纸条取出称量瓶(不能用手直接拿称量瓶),然后打开电子天平的门,把称量瓶放到称量室,再把电子天平的门关好,准备称量。
第二篇:盐酸标准溶液的标定
盐酸标准溶液的标定
一.仪器与试剂
仪器:全自动电光分析天平 1台
(1)称量瓶 1只
(2)试剂瓶 1000ml 1个
(3)锥形瓶 250ml 3个
(4)酸式滴定管 50ml 1支
(5)量筒 50mL 1只
试剂:
(1)0.1mol/L盐酸待标定溶液
(2)无水碳酸钠(固基准物)
(3)溴甲酚绿-甲基红混合指示剂
二、步骤
0.1mol/L盐酸标准溶液的标定
1.标定步骤
用称量瓶按递减称量法称取在270~300℃灼烧至恒重的基准无水碳酸钠0.15~0.22g(称准至0.0002g),放入250ml锥形瓶中,以50ml蒸馏水溶解,加溴甲酚绿-甲基红混合指示剂10滴(或以25ml蒸馏水溶解,加甲基橙指示剂1~2滴),用0.1mol/L盐酸溶液滴定至溶液由绿色变为暗红色(或由黄色变为橙色),加热煮沸2分钟,冷却后继续滴定志溶液呈暗红色(或橙色)为 终点。平行测定3次,同时做空白实验。以上平行测定3次的 算术平均值为测定结果。
2.计算
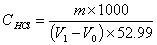
式中: m—基准无水碳酸钠的质量,g;
V1—盐酸溶液的用量,ml;
V0—空白试验中盐酸溶液的用量,ml;
52.99—1/2 Na2CO3摩尔质量,g/mol
CHCL—盐酸标准溶液的浓度,mol/L.
氢氧化钠溶液的标定
1、试剂:
(1)0.1000mol/L氢氧化钠待标定溶液
(2)酚酞指示剂
2、仪器:
(1)全自动电光分析天平 1台
(2)称量瓶 1只
(3)碱式滴定管 (50mL) 1支
(4)锥形瓶 (250mL) 3支
(5)烧杯 (250mL) 2只
(6)洗瓶 1只
(7)量筒 (50mL) 1只
3、测定步骤:
准确称取在110℃~120℃准确称取在110~120℃烘至恒重的基准邻苯二甲酸氢钾0.5~0.6g(称准至0.0002g),放入250ml三角瓶中,加入250ml的蒸馏水溶解,加酚酞指示剂2滴,用0.1mol/LNaOH溶液滴定至由无色变为红色30秒不褪色为终点,平行测定3次,同时作空白试验。
4、计算:C(NaOH)=
式中:m—邻苯二甲酸氢钾的质量,g
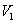 —NaOH溶液的用量,ml
—NaOH溶液的用量,ml
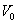 —空白试验NaOH溶液的用量,ml
—空白试验NaOH溶液的用量,ml
204.22 —邻苯二甲酸氢钾的摩尔质量,g/mol
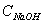 —NaOH标准溶液的浓度,mol/L
—NaOH标准溶液的浓度,mol/L
混合碱的组成及其含量的测定
一、仪器和试剂
1.仪器
(1)全自动电光分析天平 1台
(2)酸式滴定管 50ml 1根
(3)称量瓶 1只
(4)锥形瓶 250mL 2只
(5)洗瓶 1只
(6)容量瓶 250mL 1只
(7)烧杯 250mL 2只
2.试剂
0.1%甲基橙指示剂;0.1%酚酞指示剂;混合碱试样、 0.1mol/LHCI标准溶液。
二、实验步骤
1.准确称取混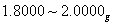 合碱试样于烧杯中,溶解并定量转移于250ml容量瓶中,用蒸馏水稀释到刻度,摇匀。
合碱试样于烧杯中,溶解并定量转移于250ml容量瓶中,用蒸馏水稀释到刻度,摇匀。
2.用处理好的移液管准确移取25.00ml试液于锥形瓶中,加入酚酞指示剂1~2滴,用0.1mol/LHCI标准溶液滴定至红色刚刚褪去,记录消耗0.1mol/LHCI标准溶液体积记为V1ml,然后加入甲基橙指示剂1滴,继续用0.1mol/LHCI标准溶液滴定至溶液由黄色变为橙色为终点,记录消耗HCl标准溶液的总体积V总,平行测定3次。根据两次消耗0.1mol/LHCI标准溶液的体积,计算出V1和V2,判断出此混合碱是由哪两种物质组成。
另:准确称取混混合碱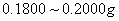 试样于锥形瓶中,加入50mL蒸馏水溶解,加入酚酞指示剂1~2滴,用0.1mol/LHCI标准溶液滴定至红色刚刚褪去,记录消耗0.1mol/LHCI标准溶液体积记为V1ml,然后加入甲基橙指示剂1滴,继续用0.1mol/LHCI标准溶液滴定至溶液由黄色变为橙色为终点,记录消耗HCl标准溶液的总体积V总,平行测定3次。根据两次消耗0.1mol/LHCI标准溶液的体积,计算出V1和V2,判断出此混合碱是由哪两种物质组成。
试样于锥形瓶中,加入50mL蒸馏水溶解,加入酚酞指示剂1~2滴,用0.1mol/LHCI标准溶液滴定至红色刚刚褪去,记录消耗0.1mol/LHCI标准溶液体积记为V1ml,然后加入甲基橙指示剂1滴,继续用0.1mol/LHCI标准溶液滴定至溶液由黄色变为橙色为终点,记录消耗HCl标准溶液的总体积V总,平行测定3次。根据两次消耗0.1mol/LHCI标准溶液的体积,计算出V1和V2,判断出此混合碱是由哪两种物质组成。
3、结果计算
1、若V1<V2,则:
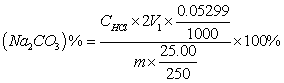
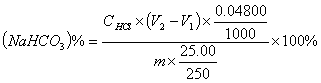
2、若V1>V2,则:
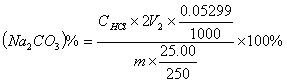
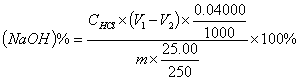
式中: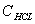 ——盐酸标准溶液的浓度,mol/L;
——盐酸标准溶液的浓度,mol/L;
V1——以酚酞为指示剂,滴定至终点时盐酸标准溶液的用量,mL;
V2——以甲基橙为指示剂,滴定至终点时盐酸标准溶液的用量,mL;
0.05300——碳酸钠的毫摩尔质量,g/mmol/L;
0.08400——碳酸氢钠的毫摩尔质量,g/mmol/L;
0.04000——氢氧化钠的毫摩尔质量,g/mmol/L;
高锰酸钾溶液的标定
一、仪器和试剂
1、仪器
(1)全自动电光分析天平 1台
(2)称量瓶 1只
(3)棕色酸式滴定管 50mL 1根
(4)锥形瓶 250mL 3只
(5)量筒 50mL 1只
2、试剂
(1)0.1mol/L高锰酸钾待标定溶液
(2)草酸钠(基准试剂)
(3)3mol/L的硫酸溶液
二、步骤
1、准确称取于105~110℃烘干至恒重的基准试剂草酸钠0.18~0.22g(准确至0. 0002g),于锥形瓶中,加入50ml蒸水溶解后,再加入3mol/L的硫酸溶液15mL,加热到75~85℃,趁热用待标定的0.1mol/L高锰酸钾待标定溶液滴定至溶液呈粉红色,并保持30S不褪色,平行测定3次,同时做空白试验。
2、结果计算
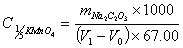
式中: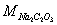 ——基准试剂草酸的质量,g;
——基准试剂草酸的质量,g;
V1——高锰酸钾标准溶液的消耗量,mL;
V2——空白试验高锰酸钾标准溶液的用量,mL;
67.00——草酸钠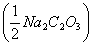 的摩尔质量,g/mol/L;
的摩尔质量,g/mol/L;
 ——高锰酸钾标准溶液的浓度,mol/L;
——高锰酸钾标准溶液的浓度,mol/L;
铵盐中氮含量的测定
一、仪器和试剂
1、仪器
(1)全自动电光分析天平 1台
(2)碱式滴定管 50mL 1根
(3)容量瓶 250mL 1只
(4)锥形瓶 250mL 3只
(5)移液管 25mL 1支
(6)吸量管 5mL 1只
(7)吸耳球 1只
(8)称量瓶 1只
(9)烧杯 250mL 1只
2、试剂
(1)0.1mol/L氢氧化钠标准溶液
(2)硫酸铵试样
(3)18%甲醛溶液
(4)酚酞指示剂
二、步骤
1、准确称取1.20~1.40g(精确至0.0002g)的硫酸铵试样,于250mL烧杯中,加入约50mL的蒸馏水溶解试样,定量移入250mL容量瓶中,用少量的水洗涤烧杯2~3次,洗涤液并入容量瓶中,平摇,稀释至刻度,摇匀。
2、准确移取25mL硫酸铵试液,于锥形瓶中,加入5mL18%的中性甲醛试液,放置5分钟后,加入1~2滴酚酞指示剂,用0.1mol/L氢氧化钠标准溶液滴定至溶液呈浅粉红色,并保持30S不褪色,记录氢氧化钠溶液的消耗量(V),平行测定3次。
3、结果计算

式中: 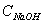 ——氢氧化钠标准溶液的摩尔浓度,mol/L;
——氢氧化钠标准溶液的摩尔浓度,mol/L;
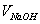 ——氢氧化钠标准溶液的消耗量,mL;
——氢氧化钠标准溶液的消耗量,mL;
0.01401——氮的毫摩尔质量,g/mmol/L;
m——硫酸铵试样的质量,g;
总碱含量的测定
1、试剂:
(1)0.1000mol/LHCl标准溶液
(2)甲基橙指示剂
2、仪器:
(1)全自动电光分析天平 1台
(2)称量瓶 1只
(3)容量瓶 (250mL) 1只
(4)称液管 (25mL) 1支
(5)酸式滴定管 (50mL) 1支
(6)锥形瓶 (250mL) 3支
(7)烧杯 (250mL) 2只
(8)洗瓶 1只
3、测定步骤:
准确称取1.3~1.5克工业碳酸钠试样(准确至0.0001g)于250mL烧杯中,加入蒸馏水溶解后(可适当加热溶解完全),称入250mL容量瓶中,稀释至刻度。用称液管吸取25.00mL试液于锥形瓶中,加入1~2滴甲基橙指示剂,用0.1000mol/LHCl标准溶液滴定至溶液由黄色变为橙色。平行测定3次。
4、计算:总碱的质量分数,以Na2CO3表示。
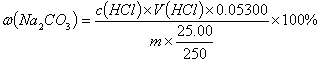
式中: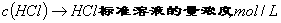
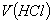 ——消耗
——消耗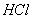 标准溶液的体积,mL
标准溶液的体积,mL
m——试样的质量,g
混合物中草酸和草酸钠含量的测定
一、试剂和材料:
硫酸 8+92
酚酞指示剂 10g/L
氢氧化钠标准溶液 0.1000mol/L
高锰酸钾标准溶液 0.1000mol/L
二、分析步骤
准确称取1.8~2.0(精确至0.0002g),于250mL的烧杯中,加入50mL水溶解,转移至250mL的容量瓶中,用水稀释至刻度,摇匀。此为溶液A。
(1)草酸含量的测定
用移液管吸取样品溶液(A)25.00mL于250mL锥形瓶中,加入50mL水,加2滴酚酞指示剂,用0.1000mol/LNaOH标准溶液滴定至溶液呈粉红色为终点,记下V1
(2)草酸钠含量的测定
用移液管吸取样品溶液(A)25.00mL于250mL烧杯中,加入100mL硫酸溶液(8+90),加热至75℃,立即用用0.1000mol/LKMnO4标准溶液滴定至溶液呈粉红色,并保持30S不褪色为终点,记下V2
二、数据的记录与结果的处理
(1)混合物中草酸质量分数X1(%)按下式计算:

(2)混合物中草酸钠质量分数X2(%)按下式计算


工业用水中微量铁含量的测定(邻菲啰啉法)
1、仪器
(1)721或723分光光度计 1台
(2)容量瓶(50mL) 6只
(3)烧杯(100mL) 2只
(4)刻度吸量管(10mL) 1支
(5mL) 3支
(1mL) 1支
(5)吸耳球 1只
2、试剂
(1)0.01mg/mL铁标准溶液
(2)10%盐酸羟胺溶液
(3)0.1%邻菲啰啉溶液
(4)乙酸—乙酸钠缓冲溶液
3、步骤
(1)标准曲线的绘制
依次吸取铁标准溶液0.00;1.00;3.00;5.00;7.00于50ml容量瓶中,加入1mL10%盐酸羟胺溶液、5mL乙酸—乙酸钠缓冲溶液及5mL0.1%邻菲啰啉溶液,加蒸馏水稀释至刻度,摇匀,静置15分钟。即组成铁标准系列,用721或723分光光度计选择波长在510nm处测定吸光度。
(2)根据测定出的吸光度及溶液的浓度,绘制出标准曲线。
(3)样品的配制及测定
准确移取5.00mL的待测试样,于50ml容量瓶中,加入1mL10%盐酸羟胺溶液、5mL乙酸—乙酸钠缓冲溶液及5mL0.1%邻菲啰啉溶液,加蒸馏水稀释至刻度,摇匀,静置15分钟。用721或723分光光度计选择波长在510nm处测定吸光度(以空白试液作参比液)。
4、计算
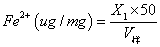
5、数据记录与结果计算
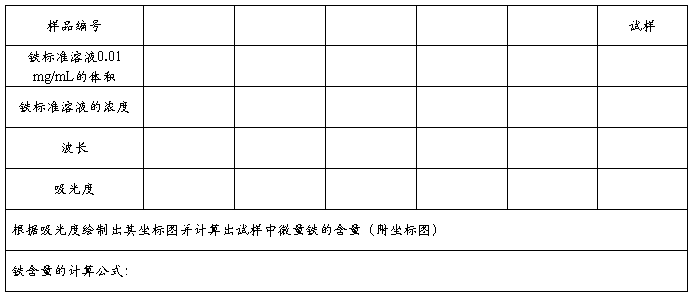
-
实验5 盐酸标准溶液的配制和标定
实验五盐酸标准溶液的配制和标定一实验目的1掌握减量法准确称取基准物的方法2掌握滴定操作并学会正确判断滴定终点的方法3学会配制和标定…
-
盐酸标准溶液的配制与标定
盐酸标准溶液的配制与标定一实验目的与要求1掌握用无水碳酸钠作基准物质标定盐酸溶液的原理和方法2正确判断甲基橙指示剂的滴定终点二实验…
-
盐酸和氢氧化钠标准溶液浓度的标定实验报告
盐酸和氢氧化钠标准溶液浓度的标定实验报告一实验目的1掌握NaOH标准溶液的标定方法2了解基准物质邻苯二甲酸氢钾的性质及应用3进一步…
-
化学实验报告——盐酸溶液的标定
化学实验报告无机及分析化学题目盐酸溶液的标定学院班级姓名学号指导老师年月日制时间盐酸浓度的标定一实验目的1练习酸碱标准溶液的标定方…
-
盐酸标准溶液的配制与标定
一考核目的1学会直接法配制标准溶液的方法2学会盐酸溶液的标定方法3学会使用分析天平称取试样4练习容量瓶移液管滴定管的操作方法二实验…
-
化学实验报告——盐酸溶液的标定
化学实验报告无机及分析化学题目盐酸溶液的标定学院班级姓名学号指导老师年月日制时间盐酸浓度的标定一实验目的1练习酸碱标准溶液的标定方…
-
实验5 盐酸标准溶液的配制和标定
实验五盐酸标准溶液的配制和标定一实验目的1掌握减量法准确称取基准物的方法2掌握滴定操作并学会正确判断滴定终点的方法3学会配制和标定…
-
实验报告式样标定盐酸电子(2)
YANGZHOUUNIVERSITYCHEMICALEXPERMENTPAPER实验名称23HCl标准溶液的配制和标定时间地点班级…
-
盐酸和氢氧化钠标准溶液浓度的标定实验报告
盐酸和氢氧化钠标准溶液浓度的标定实验报告一实验目的1掌握NaOH标准溶液的标定方法2了解基准物质邻苯二甲酸氢钾的性质及应用3进一步…
-
实验七 氢氧化钠标准溶液的标定及盐酸溶液浓度的测定
氢氧化钠标准溶液的标定及盐酸溶液浓度的测定一实验目的1掌握电子天平的使用方法用剃减法称取碳酸钠试样一份称量次数不超过3次2正确掌握…