苯甲醇和苯甲酸的制备
苯甲醇和苯甲酸的制备
185.本实验根据什么原理来分离纯化苯甲醇和苯甲酸这两种产物的?
答:根据苯甲酸钠、苯甲醇在水中和在乙醚中的溶解度不同。苯甲醇在乙醚中易溶,苯甲酸钠易溶于水。用乙醚可在反应混合物中萃取苯甲醇,再经蒸馏除去萃取剂乙醚,便可得到产物苯甲醇;将萃取后的水溶液酸化就得到苯甲酸固体,经抽滤,就可以得到另一产物苯甲酸。
186.醚层用饱和NaHSO3 及NaCO3溶液洗涤,是洗去什么杂质?
答:醚层中加饱和NaHSO3 溶液是为了除去醚层中未反应完的苯甲醛。用NaCO3溶液是洗去醚层中极少量的苯甲酸。
187.本实验中所用的苯甲醛为何应重蒸馏?
答:苯甲醛很容易被空气中的氧气氧化成苯甲酸。为除去苯甲酸,所以在实验前重新蒸馏苯甲醛。
实验十四 苯甲醇和苯甲酸的制备
一.实验目的
1. 理解苯甲醛由Cannizzaro歧化反应制备苯甲醇和苯甲酸的原理和方
2. 通过萃取分离粗产物熟练掌握,洗涤,蒸馏及重结晶等纯化技术
3. 掌握低沸点,易燃有机溶剂的蒸馏操作。
4. 掌握有机酸的分离方法。
二.实验原理
芳醛和其他无α-氢原子的醛在浓的强碱溶液作用下,发生Cannizzaro反应,一分子醛被氧化成羧酸(在碱性溶液中成为羧酸盐),另一分子醛则被还原成醇。本实验是应用Cannizzaro反应,以苯甲醛为反应物。在浓氢氧化钠作用下生成苯甲醇和苯甲酸。
反应式:
三.物理常数

四.实验装置
五.试剂与器材
试剂:苯甲醛、氢氧化钠、浓盐酸、乙醚、饱和亚硫酸氢钠、10%碳酸钠、无水硫酸镁。
器材:锥形瓶、圆底烧瓶、直形冷凝管、接引管、接受器、蒸馏头、温度计、分液漏斗、烧杯、短颈漏斗、玻璃棒、布氏漏斗、吸滤瓶。
六.实验步骤

七.产率计算
苯甲醇: 理论产量: 实际产量: 理论折射率:
产率:
苯甲酸:理论产量(m理论): 一半粗产物的质量(m粗): 重结晶质量(m重结晶):
产率:
八.产物纯化
九.实验讨论
1. 原料苯甲醛易被空气氧化,所以保存时间较长的苯甲醛,使用前应重新蒸馏;否则苯甲醛已氧化成苯甲酸而使苯甲醇的产量相对减少。
2.在反应时充分摇荡目的是让反应物要充分混合,否则对产率的影响很大。
3.在第一步反应时加水后,苯甲酸盐如不能溶解,可稍微加热;
4. 用分液漏斗分液时,水层从下面分出,乙醚层要从上面倒出,否则会影响后面的操作。
5.合并的乙醚层用无水硫酸镁或无水碳酸钾干燥时,振荡后要静置片刻至澄清;并充分静置约30min。干燥后的乙醚层慢慢倒入干燥的蒸馏烧瓶中,应用棉花过滤。
6.蒸馏乙醚时严禁使用明火。 乙醚蒸完后立刻回收,直接用电热套加热,温度上升到140℃,用空气冷凝管蒸馏苯甲醇;
7. 水层如果酸化不完全,会使苯甲酸不能充分析出,导致产物损失。
第二篇:苯甲酸和苯甲醛的合成暨Cannizzaro反应
苯甲酸和苯甲醛的合成暨Cannizzaro反应
作者:段璞
摘要:本文是第四次合成化学实验的实验报告,主要介绍了以苯甲醛为原料进行的
Cannizzaro反应制备苯甲酸与苯甲醇的方法。反应后通过萃取分离苯甲酸与苯甲醇,并分别运用重结晶和加压蒸馏提纯两产物。本次实验投放原料苯甲醛10mL(10.4g,0.1mol),共制得提纯产物苯甲酸4.38g、苯甲醇3.68g。
实验原理:
无-α-氢的醛(如芳香醛、甲醛等)在浓碱的作用下发生歧化反应,一分子醛失去氢被氧化为酸,而另一分子醛得到氢而被还原为醇,此反应即为Cannizzaro反应。
如本次反应中使用的苯甲醛歧化反应:
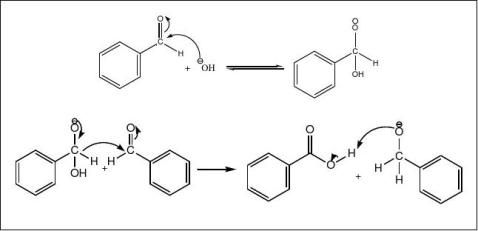
Cannizzaro反应的实质是羰基的亲核加成。反应的机理是OH-对一个醛分子的羰基进行亲核进攻生成负离子,此负离子使原来醛基上的氢带着一对电子对另一分子芳香醛进行亲核加成。反应机理如下:
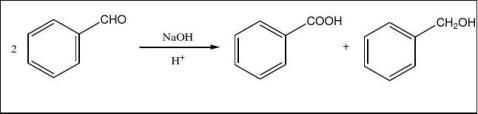
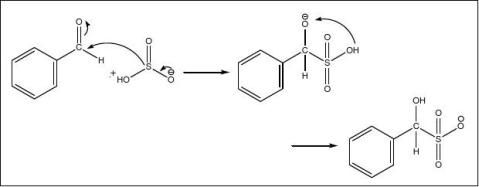
由于第一步反应为可逆反应,且平衡偏向反应物一侧,所以Cannizzaro反应需要非常高的碱度,常用过量一倍以上的浓度为50%的强碱。本次反应中使用了10g氢氧化钠(0.25mol,即2.5当量)。
利用产物苯甲酸与苯甲醇在碱性溶液与乙醚中溶解度的不同(苯甲酸以苯甲酸盐的形式存在于碱液,而苯甲醇主要存在于乙醚)达到分离两种产物的效果。接着利用未反应完全的苯甲醛易与亚硫酸氢钠反应生成α-羟基苄磺酸钠,从而达到与苯甲醇分离的效果。反应机理如下:
实验操作及现象:
1. 于150mL锥形瓶中称取10g氢氧化钠(0.25mol)加入10mL水。溶解并冷却至室温后,
边振摇边加入10mL苯甲醛(10.4g,0.1mol)。加完后用称量纸封口,剧烈振摇,充分混合,数分钟后,原料凝结成固体,呈现微黄色,后逐渐变为淡粉色。于避光处放置两礼拜。
2. 取适量水溶解,转移至分液漏斗,乙醚萃取3次,每次25mL。初次醚层呈红褐色,水
层微浑浊,萃取若干次后基本澄清。合并醚层,倒入分液漏斗中,先用10mL饱和亚硫
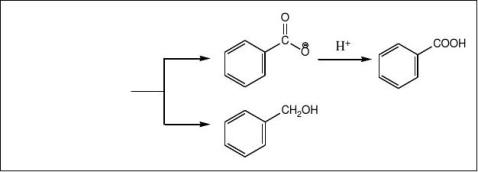
酸氢钠洗涤;再用20mL碳酸氢钠洗涤,放出少量气泡;最后用10mL水洗。醚层盛放在干燥具塞瓶中,加入适量无水硫酸钠,防止干燥0.5h以上。
3. 醚液过滤至蒸馏瓶中,先常压蒸馏、旋转蒸发蒸去大部分乙醚,后搭建加压蒸馏装置,
于0.4kPa收集到78~79℃无色透明馏分(苯甲醇)3.68g,产率69.4%。
4. 水层边搅拌边加入浓盐酸,至刚果红变蓝,析出大量白色粉末状固体。冷至室温,抽滤、
压干,得粗产10.73g白色粉末状晶体。向粗产品逐步加入约70g水加热至沸腾溶解,后再加入约70g水加入半角勺活性炭,加热至沸。趁热过滤,滤液盛放在烧杯中盖上表面皿,放置冷却结晶,抽滤,晶体以少量水洗后干燥至恒重,于滤纸上析出较多晶体。得片状白色晶体4.38g,产率73.2%。
实验问题与讨论:
1. 为何产物中苯甲醇的产量小于苯甲酸?
苯甲醛极易被空气等氧化。反应第一步加入的苯甲醛本应是事先提纯的,但实际使用的并未提纯,已有一定量苯甲酸;其次,反应过程中,因反应容器未除氧,密封也不彻底,也有一部分苯甲醛会被空气氧化,故会有更多的苯甲酸生成。
2. 为何会在热水漏斗上析出大量晶体?
我在进行该步操作时,未等热水漏斗中的水沸腾即加入粗品溶液,导致苯甲酸在滤纸上受冷析出,损失较多产物。
3. 为何要使用瓦楞状滤纸?
使用瓦楞状滤纸而非普通滤纸是为了加大表面积,加快过滤速度,防止溶液受冷,减少产品在滤纸上析出。
4. 查阅《大学有机化学实验》教材p162中苯甲酸在水中溶解度随温度变化的表格,可以
看到苯甲酸在100℃水中的溶解度为5.88g。而本次试验中,我最终获得的苯甲酸纯品达
4.38g,之前溶解在了70mL水中,这意味着苯甲酸在100℃水中的溶解度至少为
6.26g/100g。而其他同学获得的苯甲酸纯品均至少有这一水平,部分达到6g以上,而溶解所用的水均在70mL左右,溶解度远远大于数据表中参考值。这一点我一直无法解释。
5. 为何反应进行后出产物固体呈现淡粉色?
由于该反应剧烈放热,且体系中存在氧气和苯甲醇,很有可能是因为局部过热导致氧气氧化苯甲醇生成了少量的醌,故呈现出红色。
6. 为何反应初期体系呈现黄色?为何反应粗产混合物呈现,溶于乙醚后却呈现红棕色?
网上查阅资料发现,苯甲醛在水中呈现无色,但在乙醚,尤其是苯甲醇中呈现明显的黄色,原因为不同的溶剂化效应。在反应初期,体系中苯甲醇、苯甲醛的量均较多,故呈现出苯甲醛溶于苯甲醇中特有的黄色,后苯甲醛逐渐较少,颜色变浅直至无法明显分辨;混合物溶于乙醚后,呈现出苯甲醛的黄色,与醌的红棕色混合后,呈现最后的红褐色。
-
苯甲醇和苯甲酸的制备
南昌大学有机化学实验报告学生姓名小田田学号专业班级实验类型验证综合设计创新实验日期20xx年4月24日实验地点同组学生姓名指导教师…
-
实验十苯甲醇和苯甲酸的制备
实验十苯甲醇和苯甲酸的制备一实验目的1学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法2进一步熟悉机械搅拌器的使用3进一步掌握萃取洗涤蒸…
-
苯甲醇和苯甲酸的制备
苯甲醇和苯甲酸的制备185本实验根据什么原理来分离纯化苯甲醇和苯甲酸这两种产物的答根据苯甲酸钠苯甲醇在水中和在乙醚中的溶解度不同苯…
-
苯甲醇和苯甲酸的制备预习报告及思考题
苯甲醇和苯甲酸的制备一实验目的1学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法2巩固机械搅拌器的使用3进一步掌握萃取洗涤蒸馏干燥和重结…
-
实验化学 实验六 苯甲醇和苯甲酸的合成
实验化学刘晓庚实验六苯甲醇和苯甲酸的合成一实验目的1掌握坎尼查罗反应的原理和方法2了解苯甲醇和苯甲酸的其他制备方法3了解苯甲醇和苯…
-
苯甲醇和苯甲酸的制备预习报告及思考题
苯甲醇和苯甲酸的制备一实验目的1学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法2巩固机械搅拌器的使用3进一步掌握萃取洗涤蒸馏干燥和重结…
-
苯甲醇和苯甲酸的制备
南昌大学有机化学实验报告学生姓名小田田学号专业班级实验类型验证综合设计创新实验日期20xx年4月24日实验地点同组学生姓名指导教师…
-
实验十苯甲醇和苯甲酸的制备
实验十苯甲醇和苯甲酸的制备一实验目的1学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法2进一步熟悉机械搅拌器的使用3进一步掌握萃取洗涤蒸…
-
苯亚甲基苯乙酮的制备(期末实验报告)
苯亚甲基苯乙酮的制备一实验的目的和要求1掌握羟醛缩合反应的原理和机理学会苯亚甲基苯乙酮的合成方法2掌握水蒸气蒸馏3掌握反应温度控制…
- 实验课教案呋喃甲醇和呋喃甲酸的制备