醋酸电离度和电离常数的测定
实验一 醋酸电离度和电离常数的测定
[目的要求]
1.测定醋酸的电离度和电离常数。
2.学习使用pH计。
[实验原理]
1. 酸度法
HAc H+ + Ac-
H+ + Ac-
起始浓度 c 0 0
平衡浓度 c-ca ca ca
电离常数 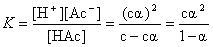 (1)
(1)
在一定温度下,用酸度计测定一系列已知浓度的醋酸溶液的pH值,根据pH=lg[H+]和a=[H+]/c可以求得一系列对应的a和K值。所取得的一系列K值的平均值,即为该温度下醋酸的电离常数。
2. 电导法
电解质溶液导电能力的大小可用电阻R的倒数——电导L(单位:西门子,S)来描述(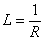 ) 根据欧姆电阻定律,在电极面积为A,距离为l时,溶液的电导为
) 根据欧姆电阻定律,在电极面积为A,距离为l时,溶液的电导为
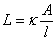 或
或  (
(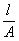 为电极常数,k为电导率)。对于给定电极,A与l都是固定值,因此,电导与电极的结构无关。在一定温度下,电解质溶液的电导决定于溶液的性质及浓度。为了比较不同电解质的导电能力,引入摩尔电导(Lm)这一概念,它是把含有1mol溶质的电解质置于相距为1m、面积为1m2的两个电极之间的电导。
为电极常数,k为电导率)。对于给定电极,A与l都是固定值,因此,电导与电极的结构无关。在一定温度下,电解质溶液的电导决定于溶液的性质及浓度。为了比较不同电解质的导电能力,引入摩尔电导(Lm)这一概念,它是把含有1mol溶质的电解质置于相距为1m、面积为1m2的两个电极之间的电导。
Lm=kV=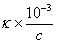 (电导率k由实验测定) (2)
(电导率k由实验测定) (2)
(k单位:S·m-1,Lm单位:S·m2·mol-1,c单位:mol·L-1)
弱电解质溶液在无限稀释时,可看作完全电离(a→1),此时溶液的摩尔电导叫做极限摩尔电导(L∞)。在一定温度下,弱电解质的电离度a等于在溶液浓度c时的摩尔电导Lm与溶液的极限摩尔电导L∞之比,即
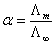 (3)
(3)
这样,由实验测定浓度为c的HAc溶液的电导率k,带入(2)式,算出其电导摩尔Lm;代入(3)式,算出a;再代入(1)式,可算出电离常数K
[实验步骤]
1.配制不同浓度的醋酸溶液
用移液管分别取25.00 mL、5.00 mL、2.50 mL的标准醋酸溶液于3个50 mL容量瓶中,再用蒸馏水稀释到刻度,摇匀。
2.测定醋酸溶液的pH值和电导率(k),并计算醋酸的电离度和电离常数
把以上四种不同浓度的醋酸溶液分别加入4只洁净干燥的50 mL烧杯中,按由稀到浓的次序在酸度计上测定它们的pH值,记录数据和室温。计算电离度和电离常数,结果填入下表。
表1酸度法测定结果
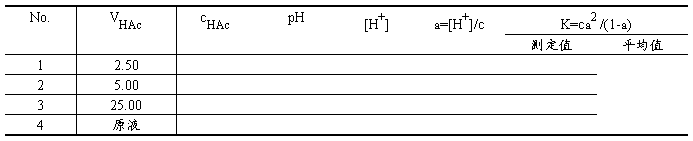
表2电导率法测定结果

本实验测定K值在1.0´10-5~2.0´10-5范围内合格
[思考题]
1.烧杯是否必须烘干?还可以作怎样处理?
2.如果改变所测醋酸溶液的温度或浓度,它的电离度和电离常数有无变化?若有变化,会有怎样的变化?
PHS-3D型pH计使用方法
1. 电极用蒸馏水清洗、吸水纸吸干后,插入复合电极插座。
2. 仪器的自动标定
(1) 按“模式”键一次,仪器浸入溶液温度显示状态,按“△”或“▽”键调节温度上升或下降,使温度显示值和溶液温度一致,然后按“确认”键。
(2) 将电极插入pH=6.86的标准缓冲溶液中,待读数稳定后按“模式”键两次(显示器下方显示“定位”),然后按“确认”键,仪器显示该温度下标准缓冲溶液的pH值(显示6.92或6.86)。
(3) 电极用蒸馏水冲洗、吸水纸吸干,插入pH=4.00的标准缓冲溶液中,待读数稳定后按“模式”键三次(显示器下方显示“斜率”),然后按“确认”键,仪器显示该温度下标准缓冲溶液的pH值。
3. 电极用蒸馏水冲洗、吸水纸吸干后即可对待测溶液进行测量(此时所有按键固定不动)。
注:由于待测溶液均为稀醋酸,故每次测定前不用蒸馏水冲洗电极,只需用吸水纸将电极吸干即可。
DDS-11A电导率仪使用方法
1.插上电极,按下ON/OFF,开机(此时,温度自动显示为25℃,电导池常数K=1.0)。
2.按“SET”键两次(“K=1.000”闪烁显示)。
3.按“MODE”键进入电导率测定状态(显示S)。
4.电极准备:先用蒸馏水冲洗,再用少量待测液润洗。
5.依次测定1-4号溶液的电导率(测定不同浓度溶液时,不要用蒸馏水冲洗电极,只需用少量待测液润洗电极)。
特别注意:为保护Pt黑电极,一定不要用吸水纸擦拭电极。使用时,只需先用蒸馏水冲洗,再用少量待测液润洗。
注:HAc溶液的极限摩尔电导的文献值

若室温不同于上表中所列温度,可用内插法求得所需的L¥值。例如,室温为11℃时,HAc无限稀释的摩尔电导L¥可计算如下:

x=0.00635 S·m2·mol-1,则11℃时L¥=0.0245+0.00635=0.03085 S·m2·mol-1
第二篇:醋酸电离度和电离常数的测定—pH法
醋酸电离度和电离常数的测定—pH法
实验目的:
测定醋酸的电离度和电离常数.
实验原理:
HAc → H++ Ac-
C:HAc的起始浓度;[H+]、[Ac-]、[HAc]:分别为平衡浓度;
α:电离数;K:平衡常数
α =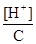 × 100%
× 100%
Ka = 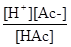 =
=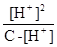
当α小于5%时,C - [H+]≈C,所以Ka≈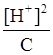
根据以上关系,通过测定已知浓度HAc溶液的pH值,就可算出[H+],从而可以计算该HAc溶液的电离度和平衡常数。(pH=-lg[H+],[H+]=10-pH)
三.仪器和试剂
1.仪器
PHS-2F型pH计、温度计、电磁搅拌器、吸量管(5mL)、容量瓶(50 mL)等。
2.试剂
0.200 mol·L-1HAc标准溶液、pH标准缓冲溶液(邻苯二甲酸氢钾、混合磷酸盐、四硼酸钠)、广泛试纸。
四.实验步骤
一.如何准确测量醋酸电离度和电离常数?
二.师生共同讨论,提出实验方案。
三.教师展示溶液pH测定整个过程
1.接通电源,打开PHS-2F型pH计的电源开关,预热仪器。
2.电极的准备、检查和处理,安装电极。
3.双点标定酸度计。
4.配制不同浓度的HAc溶液
用移液管分别取2.50 mL、5.00 mL、25.00 mL已测得准确浓度的HAc溶液,分别加入3只50 mL容量瓶中,用去离子水稀释至刻度,摇匀,并计算出三个容量瓶中HAc溶液的准确浓度。将溶液从稀到浓排序编号为:1、2、3,原溶液为4号。
5. 测定HAc溶液的pH值,并计算HAc的电离度、电离常数
把以上四种不同浓度的HAc溶液分别加入四只洁净干燥的杯中,按由稀到浓的顺序在pH计上分别测定它们的pH值,并记录数据和室温。将数据填入下表,计算HAc电离度和电离常数。

K值在1.0×10-5~2.0×10-5范围内合格(文献值25℃1.76×10-5)
四、学生对此过程中不理解处提问,教师解惑。
五、醋酸电离度和电离常数的测定。
六、提问
烧杯是否必须烘干?还可以做怎样的处理?
答:不需烘干,用待测溶液荡洗2~3次即可。
七、思考题
1.若所用HAc溶液的浓度极稀,是否还能用近似公式Ka=[H+]2/C来计算K,为什么?
答:若CHAc很小,则C酸/Ka就可能不大于500,就不能用近似公式Ka=[H+]2/C,如用近似公式,会造成较大的误差。
2.改变所测HAc溶液的浓度或温度,则有无变化?
答:CHAc减小,α增大,Ka不变;
Ka随T改变而变化很小,在室温范围内可忽略。
八、注意事项
1.测定HAc溶液的pH值时,要按溶液从稀到浓的次序进行,每次换测量液时都必须清洗电极,并吸干,保证浓度不变,减小误差。
2.PHS计使用时,先用标准pH溶液校正。
3.玻璃电极的球部特别薄,要注意保护,安装时略低于甘汞电极,使用前用去离子水浸泡48小时以上。
4.甘汞电极使用时应拔去橡皮塞和橡皮帽,内部无气泡,并有少量结晶,以保证KCl溶液是饱和的,用前将溶液加满,用后将橡皮塞和橡皮帽套好。
-
无机化学实验六 醋酸电离度和电离常数的测定1
实验六醋酸电离度和电离常数的测定pH法一实验目的1测定醋酸的电离度和电离常数2学习pH计的使用教学重点醋酸的电离度电离常数的测定教…
-
醋酸电离常数和电离度的测定
实验三醋酸电离常数和电离度的测定一实验目的1测定醋酸的电离常数加深对电离度的理解2学习正确使用pH计二实验原理醋酸CH3COOH或…
-
实验十五 醋酸电离度和电离常数的测定
实验十五醋酸电离度和电离常数的测定一教学要求1学习测定醋酸离解度和离解常数的基本原理和方法2学会酸度计的使用方法3巩固溶液的配制及…
-
醋酸电离度和电离常数的测定
实验题目醋酸电离度和电离常数的测定教材p5759一实验目的1测定醋酸的电离度和电离常数2掌握滴定原理滴定操作及正确判断滴定终点3练…
-
醋酸电离度和电离常数的测定—pH计的使用
醋酸电离度和电离常数的测定pH计的使用实验目的测定醋酸的电离度和电离常数进一步掌握滴定原理滴定操作及正确判断滴定终点学习使用pH计…
-
第四版无机化学实验报告实验十三:醋酸解离度和解离常数的测定——pH计的使用
实验名称醋酸解离和解离常数的测定pH计的使用实验日期温度气压一实验目的1测定醋酸的解离度和解离常数2掌握滴定原理滴定操作及正确判断…
-
采用分光光度法测定弱电解质的电离常数实验报告
采用分光光度法测定弱电解质的电离常数实验报告一实验目的1了解一种测定弱电解质电离常数的方法2掌握分光光度计的测试原理和使用方法3进…
-
四川理工实验报告电导法测定乙酸电离平衡常数 (2)
实验六电导法测定乙酸电离平衡常数报告人曾辉实验时间20xx年03月07日一实验目的1掌握电导电导率摩尔电导率的概念以及它们之间的相…
-
实验3 食用白醋的总酸度、电离度和电离常数的测定
实验3食用白醋的总酸度电离度和电离常数的测定教学目的与要求1学习食用白醋的总酸度电离度和电离常数的的原理和方法2学习酸度计的原理和…
-
报告示例:实验三__醋酸解离度和解离常数的测定
山东轻工业学院实验报告成绩课程名称基础化学实验1指导教师周磊实验日期院系专业班级实验地点实验楼A座412学生姓名学号同组人实验项目…
-
实验四 醋酸解离常数的测定
实验四醋酸解离常数的测定一pH法一实验目的1学习溶液的配制方法及有关仪器的使用2学习醋酸解离常数的测定方法3学习酸度计的使用方法二…