�������Ⱥ͵��볣���IJⶨ���� pH�Ƶ�ʹ��
ʵ��ʮ pH���ⶨ����ĵ��볣��Ka�͵����
Ŀ�ģ�1����ϤpH���ⶨ������볣��Ka��ԭ���ͷ�����
2��ѧ��ʹ����ȼƲⶨ��Һ��pHֵ��
3����һ����ϰ���Ʋ�ͬŨ�ȵ���Һ�IJ�����
ԭ����
������һԪ���ᣬ��ˮ��Һ�д�������ƽ�⣺
HAc = H+ + Ac�C
���ᣨHAc����������ʣ���ˮ��Һ�д��������е���ƽ�⣺
HAc 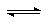 H�� �� Ac��
H�� �� Ac��
��ʼŨ�ȣ�mol·L-1�� c 0 0
ƽ��Ũ�ȣ�mol·L-1�� c��c�� c�� c��
Ka = 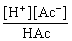
Ka��HAc�ĵ��볣����c��HAc����ʼŨ�ȣ���H���ݡ���Ac���ݡ���HAc�ݾ�Ϊƽ��Ũ�ȣ�����HAc��Һ��Ũ��Ϊcʱ�ĵ���ȡ�
����볣��K���ı���ʽΪ��
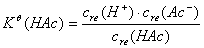
(1)
������ԭʼŨ��ΪC��ƽ��ʱ��[H+] = [Ac�C]��[HAc] = C �C [H+]�������(1)ʽ��
Ka = 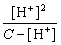 (2)
(2)
һ������£���K/c��500��������ĵ���Ȧ�С��5%����ʱ���ý��Ƽ�������������ԼΪ2%��
c-[H+]��c
��: Ka =[H+]2 /c
���ݵ���ȶ���ã� ���� [H+]/c × 100%
pH �Ķ��壺pH=-lg[H+] ����ҺpH ֵ�ķ����������ָʾ���� ������һ���¶���,pH �Ʒ�.
��ã�[H+]=10-PH
����һ���¶��£���pH�Ʋⶨһϵ����֪Ũ�ȵĴ����pHֵ����[H+] = 10�C pH������(2)ʽ���ɵõ�һϵ�е�Kaֵ��ȡ��ƽ��ֵ����Ϊ���¶��µĴ���ĵ��볣����
��һ���¶��£�����ȼƲⶨһϵ����֪Ũ��HAc��Һ��pHֵ,����pH����lg��H������ã�[H+]=10-PH
������Ka =[H+]2 /c�� Ka = 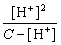 �ͦ�����H����/c�������æ���Ka��
�ͦ�����H����/c�������æ���Ka��
����������ͼ����Ka��
������ƽ�ⳣ������ʽKa=[ H+ ]2/C ����ȡ������lgKa=2lg[H+]��lgC=-2pH��lgC��
2pH=-lgKa-lgC ����Һ��2pH ��lgC ��ͼ���ɵ�һֱ�ߣ�б��Ϊ�������ؾ�Ϊ-lgKa����lgKa �������Ka ��
������ҩƷ��
1������
pH��һ�ף�50mL��100mL�ձ�5ֻ��50mL��ʽ�ζ���2֧������4����
2��ҩƷ
0.2000 mol?dm�C 3HAc����Һ��
ʵ������
һ��HAc��ҺŨ�ȵIJⶨ�������ȱ궨�ã� ���ң�
���ң�
�������Ʋ�ͬŨ�ȵ�HAc��Һ��2��һ�飩
�ֱ���ȡ2.5ml��5.0ml��10.0 ml��15.0 ml ��20.0 ml��Һ��5ֻ50ml����ƿ�У�ϡ�͡����ݡ�ҡ�ȡ����⡣
�����ⶨ��ͬŨ�ȵ�HAc��Һ��PHֵ���������K����
������3����Һ��Լ30��40ml���ֱ������ྻ��С�ձ��У�����ϡ��Ũ��˳��ֱ�ⶨ��ͬŨ�ȵ�pHֵ��
������ͬŨ�ȵĵ�HAc��Һƽ��ʱ��pHֵ ����_______��
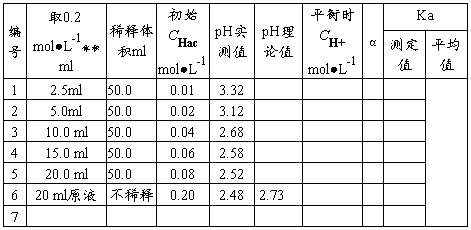
ʵ��ⶨֵ��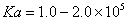 �� 25��ʱ������ֵ
�� 25��ʱ������ֵ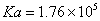
���ݴ�����
ƽ��ֵ��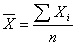
ƽ��ƫ�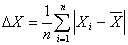
���ƫ������������ƽ��ֵ�İٷֱȽ����ƫ�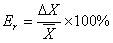
����ʹ�÷���(PHS-3C����ȼ�)
��1�� ʹ��ǰ����
�ٽ�ͨ��Դ�����أ�Ԥ��30min��
��2�������� PHһ���������
�ٽ�ѡ����PH���� ��б�ʡ���ť������100�������� ���¶ȡ� ��ť����Һ�¶ȡ�
��������ˮϴ���缫������ֽ���ɡ����ݴ���PHֵ����Ʒ��Һ֮�������ѡ����PHֵ����ı�������Һ���ѵ缫���뻺����Һ�У�ʾֵ�ȶ����ڡ���λ����ť��ʹ����ָʾֵΪ�ñ�������Һ�ڶ�¶��µı�PHֵ���ɡ�
�� 4 ����Ʒ��δ֪����ҺPHֵ�IJ���
���궨���������ɽ�����Ʒ��ҺPH�IJⶨ���ڲⶨǰ���Ƚ�������ˮϴ���缫������ֽ���ɡ�Ȼ�缫���������Һ�У���ʾֵ�ȶ�������Ϊ��Ʒ��PHֵ����ע�⣬��ʱ����ť�����ٶ���������Ҫ���±궨����
��5��������Ϻ��缫�γ�����ˮ��ϴ�ɾ����ɵ缫 ���رյ�Դ������ȼƷ����������ڡ�
3��ע�����
��Ҫʮ��ע�ⲣ���缫�ı�����������š�
��ÿ�θ����ⶨҺǰ��Ҫ���缫��ˮ��ϴ�ɾ������ɡ�
�۸ʹ��缫��Ҫ���������Ȼ�����Һ�������缫���ݲ�Ҫ��Ⱦ��
�ܲ����缫��ʹ��ǰҪ������ˮ�н���24Сʱ��
���ۣ�˵��һԪ�����Ũ���������Ⱥ͵���ƽ�ⳣ���Ĺ�ϵ��
��ʵ��ϰ�⡿
1����һ���¶��£��ı�Ũ�ȣ�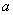 �仯��K���䣻��Ũ�Ȳ��������£��¶ȱ仯����K�����һ���¶��£�K���䣬�ɹ�ʽ
�仯��K���䣻��Ũ�Ȳ��������£��¶ȱ仯����K�����һ���¶��£�K���䣬�ɹ�ʽ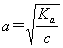 ��
��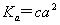 ֪��
֪��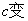 С��
��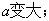 ����[H+]=
����[H+]=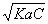 ������
������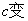 Сʱ��[H+]��С��
Сʱ��[H+]��С��
2����ȷ�궨������Һ��Ũ�ȣ���ȷ�ⶨ�¶ȣ���У��pH�ƣ���ϴ���缫ͷ��
3���Ų��ԡ���Ϊ��Һ��[H+]��[Ac-]������ȷ����Ȼ�������ЧӦ�����ǵ���ȩ�5����
�ڶ�ƪ����̪����ƽ�ⳣ���IJⶨ
��̪����ƽ�ⳣ���IJⶨ
����������ȷ�
������ ѧ�ţ�
�༶��2 ָ����ʦ��
һ��ʵ��Ŀ��
1���÷ֹ��ȼƺ�PH�Ʋⶨ��̪�ĵ���ƽ�ⳣ����
����ʵ��ԭ��
��̪��һԪ�л����ᣬ��HR��ʾ����ˮ��Һ�а���ʽ���ֵ��룺
HR===H++R- (1)
��ɫ ��ɫ
��һ���¶��£�������Ӧ�ﵽƽ������ı���ϵ�����Ũ�ȣ�����ƽ���ƶ����µ�ƽ���ʱ������Ӧ��Ũ�Ⱦ������仯����ƽ�ⳣ�����䡣��ʵ���Բ�ͬ��PH�Ļ�����ҺΪ��Ӧ�����ڶ����²ⶨ��̪�ĵ���ƽ�ⳣ����
����[HR]0��ʾ��̪��ԭʼŨ�ȣ���Ӧ�У�
[HR]= [HR]0 - [R-]
�����Ȧ�=[R-]/[HR]0 ��ã�
KT=[H+] [��/(1-��)]
��ʵ���÷ֹ��ȼƲ�����ȣ���PH�Ʋ���PH��
���ݱȶ����ɣ�һ��ɫ����֮Ũ�ȣ��ڹ⾶����ʱ����Ũ������ܶȳ����ȡ�����ȡһ������ķ�̪��Һ�ӵ�һ��֪PHֵ�û�����Һ�в�ù��ܶ�ΪE������ͬ�����£���������NaOH��ʹ��̪��ȫ���룬��ù��ܶ�ΪE �����ݵ���ȵĶ���ͱȶ����ɣ���ʽ����
��=[R-]/[HR]0=E/ E0
�Ӷ��ó�KT�ļ��㹫ʽΪ��
KT=[E/(E0-E)]x10-PH
����������ҩƷ
7721�ͷֹ��ȼơ�PH�ơ�100 ml ����ƿ6����50ml�ձ���6��1ml�̶���Һ��2֧����ͷ�ι�1֧��2ml�̶���Һ��1֧��1N NaOH��Һ��AҺ����0.4N���ᣨHAc,��������0.5�� ��̪��0.1N NaOH��Һ.
�ġ�ʵ�鲽��
1. ��1��5�ŵ�100ml����ƿ�зֱ����1.00ml0.5�� ��̪��1.00ml 0.4N�����������ˮ������ƿ�����2/3.ҡ�ȡ�
2.����ͷ�ι���ȡ1N NaOH�ֱ�μ�������5ֻ����ƿ�иպõ����죬Ȼ����� 0.4N NaOH��ʹ1����5������ƿ����Һ�ĺ�ɫ��dz�����γ�һ��ɫ�ף����������ˮϡ�����̶ȡ�
3.����һֻ100ml����ƿ�����6���У�����0.10ml 0.5����̪��2.00ml 0.1N NaOH��������ˮϡ�����̶ȴ���Ѹ�ٲⶨ1~6����Һ�Ĺ��ܶȺ�PHֵ��
�塢ʵ���¼�����ݴ���
1.���ⶨ��1~6����Һ�Ĺ��ܶȣ�E)��PH��¼���±���
ʵ���¶ȣ�25��
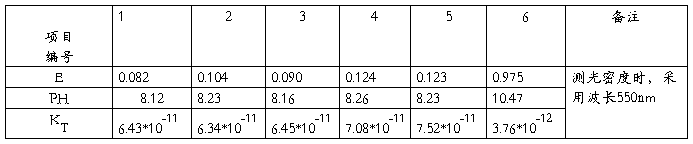
����������
1.��Һʱ����������ʵ���������
2.����ƿ�����Ǵ�����������ʵ���������
3.��ɫ�����ϴ�����ף����ʵ�����һ����
4.�����ʵIJⶨ��PH�IJⶨ����ͬʱ����Ҳ�����һ��ʵ����
5.����ʵ����������ʹ�ã������һ����ĥ����ʹʵ�������ľ��ܶȽ��ͣ�������ʵ�������һ��Ӱ�졣
�ߡ�˼����
1.������Һɫ����ɫ̫���ʵ������Ӱ�죿1��5��ƿ���з�̪������һ�¶�ʵ��������Ӱ�죿
����Ӱ�죬��Һ���������0.1��0.7�����Χȷ����ߣ�����ȳ��������Χ������Ӧ��Ũ�ȳ��������Χ��ȷ��Ҫ���ۿۡ��������0.434ʱ��ȷ����ߣ�Խ�ӽ����ֵ������Խ�ߣ�û��Ӱ�죬ƽ�ⳣ������һ���ض��ķ�Ӧ��˵�����¶�ȷ��ʱ������һ�������������ŷ�Ӧ������ı仯���仯����1��5��ƿ���еķ�̪�������Բ�һ�¡���
-
����ѧʵ���� �������Ⱥ͵��볣���IJⶨ1
ʵ�����������Ⱥ͵��볣���IJⶨpH��һʵ��Ŀ��1�ⶨ����ĵ���Ⱥ͵��볣��2ѧϰpH�Ƶ�ʹ�ý�ѧ�ص����ĵ���ȵ��볣���IJⶨ�̡�
-
������볣���͵���ȵIJⶨ
ʵ����������볣���͵���ȵIJⶨһʵ��Ŀ��1�ⶨ����ĵ��볣������Ե���ȵ�����2ѧϰ��ȷʹ��pH�ƶ�ʵ��ԭ������CH3COOH��
-
ʵ��ʮ�� �������Ⱥ͵��볣���IJⶨ
ʵ��ʮ��������Ⱥ͵��볣���IJⶨһ��ѧҪ��1ѧϰ�ⶨ�������Ⱥ���ⳣ���Ļ���ԭ���ͷ���2ѧ����ȼƵ�ʹ�÷���3������Һ�����Ƽ���
-
�������Ⱥ͵��볣���IJⶨ
ʵ����Ŀ�������Ⱥ͵��볣���IJⶨ�̲�p5759һʵ��Ŀ��1�ⶨ����ĵ���Ⱥ͵��볣��2���յζ�ԭ���ζ���������ȷ�жϵζ��յ�3����
-
�������Ⱥ͵��볣���IJⶨ��pH�Ƶ�ʹ��
�������Ⱥ͵��볣���IJⶨpH�Ƶ�ʹ��ʵ��Ŀ�IJⶨ����ĵ���Ⱥ͵��볣����һ�����յζ�ԭ���ζ���������ȷ�жϵζ��յ�ѧϰʹ��pH�ơ�
-
���İ�����ѧʵ�鱨��ʵ��ʮ�����������Ⱥͽ��볣���IJⶨ����pH�Ƶ�ʹ��
ʵ�����ƴ������ͽ��볣���IJⶨpH�Ƶ�ʹ��ʵ�������¶���ѹһʵ��Ŀ��1�ⶨ����Ľ���Ⱥͽ��볣��2���յζ�ԭ���ζ���������ȷ�жϡ�
-
���÷ֹ��ȷ��ⶨ������ʵĵ��볣��ʵ�鱨��
���÷ֹ��ȷ��ⶨ������ʵĵ��볣��ʵ�鱨��һʵ��Ŀ��1�˽�һ�ֲⶨ������ʵ��볣���ķ���2���շֹ��ȼƵIJ���ԭ����ʹ�÷���3����
-
�Ĵ�����ʵ�鱨��絼���ⶨ�������ƽ�ⳣ�� (2)
ʵ�����絼���ⶨ�������ƽ�ⳣ������������ʵ��ʱ��20xx��03��07��һʵ��Ŀ��1���յ絼�絼��Ħ���絼�ʵĸ����Լ�����֮����
-
ʵ��3 ʳ�ð״�����ȡ�����Ⱥ͵��볣���IJⶨ
ʵ��3ʳ�ð״�����ȵ���Ⱥ͵��볣���IJⶨ��ѧĿ����Ҫ��1ѧϰʳ�ð״�����ȵ���Ⱥ͵��볣���ĵ�ԭ���ͷ���2ѧϰ��ȼƵ�ԭ���͡�
-
����ʾ����ʵ����__�������Ⱥͽ��볣���IJⶨ
ɽ���ṤҵѧԺʵ�鱨��ɼ��γ����ƻ�����ѧʵ��1ָ����ʦ����ʵ������Ժϵרҵ�༶ʵ��ص�ʵ��¥A��412ѧ������ѧ��ͬ����ʵ����Ŀ��
-
ʵ���� ������볣���IJⶨ
ʵ���Ĵ�����볣���IJⶨһpH��һʵ��Ŀ��1ѧϰ��Һ�����Ʒ������й�������ʹ��2ѧϰ������볣���IJⶨ����3ѧϰ��ȼƵ�ʹ�÷�������