离子推断练习
竞赛专题
离子推断题
例1 中性溶液中含有k+、Fe3+、Cl—、SO42—四种离子,其中K+、Fe3+、Cl—三种离子的个数比为5∶2∶3。
则溶液中Fe3+与SO42—的个数比( )
A 1∶2 B 1∶3 C 2∶3 D 3∶5
例2 测得某溶液中仅含有Na+、Mg2+、SO42—、Cl—四种离子,其中Na+与Mg2+的个数比为4∶5,则Cl—和
SO42—个数比可能为( )
A 8∶3 B 3∶2 C 4∶1 D 2∶3
例3 在FeCl3和Fe2(SO4)3的混合溶液中,已知Fe3+与Cl—的个数比为4∶3,若溶液中Fe3+为4n个,则
硫酸根离子用n表示的个数为
+1 +6 -2 +1 +1
例4 在给定的H、 S、 O、 K、 Na五种元素中,最多可以组成 种化合物
例5 已知某无色溶液中可能含有H+、Ag+、Cu2+、Na+、OH—、Cl—、NO3—、CO32—等八种离子中的四种,
往该溶液中滴入几滴石蕊试液,石蕊试液变红,则原溶液中大量存在的离子可能为
或 。
例6 某溶液中可能含有Na+、H+、Cl—、SO42—欲证明两种阴离子确实存在,选用的最佳方案是:先向溶液
中滴入足量的 溶液至沉淀完全,再取上层清液滴加 溶液,又出现白色沉淀,则可得
出结论。
例7 在A、B、C、D四种物质的溶液中含有Na+、Fe3+、Ag+、Cu2+、SO42—、Cl—、OH—、 NO3—等八种离
子,现将这四种物质的稀溶液两两混合,有如下现象产生
⑴ A+B →蓝色沉淀 ⑵ D+C→白色沉淀(此沉淀不溶于稀硝酸)
⑶ B+D→红色沉淀
根据上述现象,推断并写出各物质的化学式:A _____ B__________ C_________ D 例8 某工业品盐酸中含有Fe3+、Cl—、H+;该盐酸中所含杂质的化学式 ,若溶液中H+与Cl—的个
数比为60∶63,则Fe3+与Cl—的个数比是 。 例9 某无色透明溶液 ,可能含有下面两离子的几种:阳离子组:Cu2+、Ba2+、Mg2+、H+;阴离子组:Cl—、
OH—、NO3—、CO32—;已知该溶液能和铝粉反应放出氢气,如果确定该溶液中含有Mg2+,试推断溶液中一定
含有 离子,可能含有 离子,不定没有 离子。
例10 在A、B 两组溶液中共含有离七种:Na+、 Cu2+、Ba2+、Mg2+、NO3—、OH—、SO42—;已知两溶液中
含离子各不相同,A溶液中含有四种离子,且能使紫色石蕊试液蓝色,则B溶液中含有的离子是 例11 某工厂的废渣中混有少量锌粉和氧化铜(其它成分不跟酸反应)跟大量的废盐酸接触形成污水,产和
生公害。若向污水中撒入铁粉,且反应完,铁粉有特殊需要剩余,此时污水中一定含有的金属离子是( ) 例12 在分开盛放的A、B两种溶液中,共含有Na+、H+、Ag+、Ba2+、NO3—、Cl—、CO32—七种离子,已知A
溶液中含有三种阳离子和一种阴离子,则B溶液中所含的离子是 。取少量A溶液滴入CuCl2
至不再有沉淀生成后,过滤,将此滤液加入B溶液中,则发生化学反应
有 , 。
练习
1.测得某溶液中仅含有Na+、Mg2+、SO42—、Cl—四种离子,其中离子个数比Na+∶Mg2+∶Cl—===4∶5∶8,如果Na+为4n个,则SO42—的离子可能为( )
A 2n B 3n C 6n D 8n
2.经测得某溶液中有Cu2+、k+、SO42—、Cl—四种离子,其中k+与Cu2+的个数比为4∶3,那么SO42—与Cl—的个数比可能为( )
A 3∶2 B 1∶3 C 2∶5 D 1∶8
3.从给定化合价O—2、Cl—1、Mg0、H+1、Cu+2、C+4六种元素中,选择适当的元素按下列要求组成物质(用化式填写)
⑴单质 ⑵无氧酸 ⑶酸性氧化物 ⑷难溶性碱
⑸碱性氧化物 ⑹碱式盐 ⑺可溶性正盐
4.某校课外活动小组,将一些可溶性化合物溶于水,配成甲、乙两种溶液中共有H+、Ag+、k+、Ba2+、OH—、Cl—、NO3—、CO32—八种离子,两种溶液中所含离子各不相同,已知向甲溶液里滴入石蕊试液,溶液呈蓝色。则乙溶液里含有的离子应该是(填离子符号) 。
5.某溶液中含有Na+、Zn2+、SO42—、NO3—四种离子,已知Na+∶Zn2+∶SO42—===2∶3∶2,则该溶液中Zn2+和NO3—的离子个数比 。
6.工业品盐酸中因含有Fe3+而带黄色,若某工业品盐酸中H+和Cl—的个数比为91:94,则该盐酸中Fe3+和Cl—的个数比为( )
A.1:1 B.1:3 C.91:94 D.1:94
7.现有五种离子及其化合价依次是:H+1、S+6、O—2、Na+1、K0;它们相互结合,最多可组成化合物种类是( )
A 5 B 6 C 7 D 8
8.在分开盛放的A、B 两组溶液共有Na+、 Fe3+、Ba2+、Mg2+、Ca2+、NO3—、OH—、SO42—8种离子,两溶液所含离子各不相同,已知,A溶液中共有4种阳离子和2种离子阴离子,则B溶液中所含的离子应该是 。
9.经测定某溶液中含有大量的Cu2+、SO42—、Cl—、6X(离子)四种离子,其中Cu2+与Cl—的个数为1:1,则X可能为( )
A Na+ B OH— C NO3— D Zn2+
10.某工厂排出的污水中可能含有Ba2+、k+、OH—、SO42—、Cl—、CO32—等离子,为了进一步确定,进行如下实验:
(1)取污水仔细观察。呈无色透明的均一状态。
(2)取污水少许,滴入稀硫酸产生大量白色沉淀,再加入足量稀硝酸,白色沉淀不消失。
(3)经测试,该污水PH>7。
由此推断,污水中肯定含有的离子是 ,肯定不含的离子是 。
第二篇:离子推断强化练习
高三化学一轮复习:离子推断强化练习
1.某溶液中含有NO3-、SiO32-、AlO2-、S2-等四种离子,若向其中加入过量的盐酸溶液,微热并搅拌,再加入过量NaOH溶液,溶液中大量减少的阴离子是 ( D )
A.NO3 SiO32 B.SiO32 S2- C.AlO2---- NO3- D.S2 NO3- -
2.在甲、乙两烧杯溶液中,共含有Cu2+、K+、H+、Cl-、CO32-、OH-6种离子。已知甲烧杯的溶液含其中3种离子并呈蓝绿色,则乙烧杯的溶液中含有的另3种离子是C
A.Cu2+、H+、Cl- B.K+、CO32-、Cl-
C.K+、OH-、CO32- D.K+、H+、Cl-
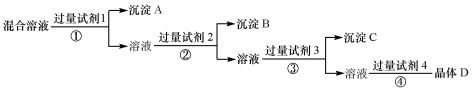
3.现有含NaCl、Na2SO4和NaNO3的混合溶液,采用下列实验流程加入适当的试剂将其转化为相应的沉淀或固体,实现Cl-、SO42-和NO3-的相互分离:
其中试剂1、2、4分别为A
A.氯化钡溶液 硝酸银溶液 稀硝酸
B.氯化钡溶液 稀硝酸 硝酸银溶液
C.氢氧化钠溶液 硝酸银溶液 稀硝酸
D.硝酸银溶液 硝酸钡溶液 稀硝酸
4、某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该
溶液进行如下实验:⑴取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;⑵ 在 ⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;⑶ 在⑵所得溶液
中加入过量Ba(OH)2溶液也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定 存在的有:B
A.SO42-、AlO2─、Na+ B.Na+、CO32─、AlO2─
C.CO32─、Na+ 、Al3+ D.MnO4─、
Na+、CO32─
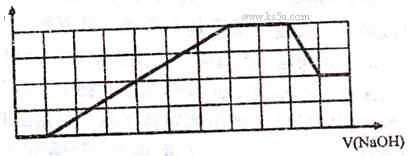
5.某溶液中可能含有H+、Na+、NH4+、Mg2+、
Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液
中加入一定物质的量浓度的NaOH溶液时,发
现生成沉淀物质的量随NaOH溶液的体积变
化的图象如右所示,下列说法正确的是 (C )
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4
6.某溶液中可能存在Br、CO32、SO32、Al3+、I、Mg2+、Na+等7
种离子中的几种。现----
取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液中肯定不存在的离子组是A .....
A.Al3+、Mg2+、I、SO32 B.Mg2+、Na+、CO32、I ----
C.Al3+、Na+、SO32、I D.Al3+、CO32、Br、SO32 -----
7. 今有一混合物的水溶液,只可能含有以下离子中的若干种:K、NH4、Cl、Mg2、
+--Ba2、CO32、SO42,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是 ( A )
+-A. K一定存在 B. 100mL溶液中含0.01mol CO32
-++C. Cl一定存在 D. Ba2一定不存在,Mg2可能存在
---8.在甲、乙两烧杯溶液中,含有大量的Cu2+、Na+、H+、SO42、CO32、OH等6种离子。
已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( B )
--- A.Cu2+、H+、SO42 B.Na+、OH、CO32
---- C.CO32、OH、SO42 D.Na+、H+、SO42 ++-+
9.甲、乙、丙三种溶液各含有一种X离子(X为Cl、Br、I),向甲中加淀粉和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙依次含有 B
A.Br、Cl、I B.Br、I、Cl C.I、Br、Cl D.Cl、I、Br 10.某无色溶液含有①Na+ 、②Ba2 +、 ③Cl、 ④Br、⑤SO32、⑥SO42 离子中的若
一一一一-----------------
下列结论正确的是 A A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑥
C.不能确定的离子是① D.不能确定的离子是③⑤
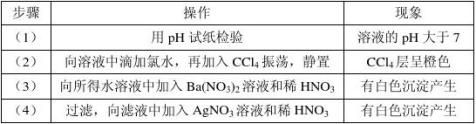
-------11.(4分)某钠盐溶液可能含有阴离子NO3、CO32、SO32、SO42、Cl、Br、I、为鉴
别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑
浊;③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
该溶液一定含有的离子是 ,上述5个实验不能确定是否存在的离子是 。
11.肯定含有CO32、SO42、 Cl,可能含有NO3(每个一分共4分) ----
12.(11分)某钠盐溶液可能含有阴离子NO3、CO32、SO32、SO42、Cl、Br、I、为-------鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解; ⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
(1)分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ;
实验② ;
实验③ ;
实验④ ;
实验⑤ ;
(2)上述5个实验不能确定是否存在的离子是 。
12.(1)①说明可能含有CO32或者含有SO32 因为二者水解均显碱性;
--②肯定含有CO32 ,肯定不含SO32、因SO2有刺激性气味
--③肯定不含有Br、I,因两者均能与氯水反应后生成单质溴和单质碘,溴和碘单质溶
解于CCl4显色;
-④肯定含有SO42,因BaSO4不溶于盐酸。
-⑤肯定含有Cl,因AgNO3与Cl-反应生成的AgCl不溶于稀HNO3。
-(2)NO3
13.(6分)某白色固体混合物,可能含有NaHSO4、BaCl2、MgCl2、NaCl、NaHCO3、NaAlO2(或Na[Al(OH)4])中的一种或几种,对试样进行检测,有如下的实验现象:①取少量该固体物质,加水溶解,最终得到澄清溶液,没有沉淀和气体;②向所得澄清溶液中滴加NaOH溶液,有白色沉淀生成,加至过量时沉淀消失。
请回答下列问题:
(1)原混合物中一定含有的物质是________________________ ___(写化学式,下同);
(2)原混合物中一定不含有的物质是__________________ _。
13.(6分)(1) NaHSO4、NaAlO2 (3分) (2) BaCl2、MgCl2、NaHCO3(3分)
14.(4分) --
某一无色溶液,可能含有Na、Cu
??2?、NH4、Fe?3?、Al3?、Mg2?、CO32?、SO42?、K等离子中的一种或几种,为确定其组成,做如下实验:
①取少量待测溶液,向其中滴入盐酸酸化的氯化钡溶液,生成白色沉淀;
②另取少量待测溶液,向其中加入过氧化钠,产生无色无味气体,并生成白色沉淀;加入过量过氧化钠时,沉淀部分溶解。
试判断:溶液中一定存在的离子有 ;一定不存在的离子有 。不确定的是 为验证此离子的存在,还应进行 实验。
14.(4分)
Al3?、Mg
?2?、SO4?2?;NH4、Cu?2?、Fe3?、CO32?(每空1分,错填或漏填皆不得分) K、Na;焰色反应
?2??15.有一瓶澄清溶液, 可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO2 4、CO3、NO3、
Cl、I现进行如下实验:
(1)测知溶液显强酸性;
(2)取样加少量四氯化碳和数滴新制氯水、CCl4层为紫红色;
(3)另取样滴加稀NaOH溶液, 使溶液变为碱性, 此过程无沉淀生成;
(4)取少量上述碱性溶液, 加Na2CO3溶液出现白色沉淀;
(5)将实验(3)中的碱性溶液加热, 有气体放出, 该气体能使湿红色石蕊试纸变蓝。
问:①原溶液中肯定存在的离子是②肯定不存在的离子是; ; --③不能确定是否存在的离子是。
②Fe3+、NO3-、Mg2+、SO42-、CO32-、Al3+ 15.①I-、Ba2+、NH4+
③K+、Cl-
16.(6分)某溶液只可能含有以下离子中的若干种:K+、NH+4、Cl-、Mg2+、Ba2+、CO2-3、
SO2-4,现取三份溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成。
(2)第二份加入足量NaOH溶液并加热后,收集到气体0.04mol。
(3)第三份加入足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤,干燥后,沉
淀质量为2.33g。根据上述实验,作出判断:
该溶液中一定存在的离子是 该溶液中一定不存在的离子是 该溶液中可能存在的离子是16.CO2-3、SO2-4、NH+4、K+、Mg2+、Ba2+、Cl-、
17、(四川延考区28)(15分)有一白色固体混合物,可能含有有的阴、阳离子分别是
K+ Ba2+ Ag+ Mg2+ NH4+ Na+ 阳离子
----阴离子 SO42 SO32 CO32 AlO2
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12。
排除的离子 排除的依据
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。
肯定存在的离子 判断依据
排除的离子 排除的依据
(3)尚待检验的离子及其检验方法
尚待检验的离子 检验方法
17(15分)
(1)
排除的离子 排除的依据
NH4+ 由于溶液呈碱性,且未嗅到刺激性气味
Ag+、Mg2+ 碱性溶液中无沉淀生成
(2)
肯定存在的离子 判断依据
-AlO2 加酸有沉淀,继续加酸沉淀溶解
-CO32 加酸后有无色无味气体逸出
排除的离子 排除的依据
-Ba2+ 有CO32 存在时原溶液无沉淀
-SO32 酸化后逸出的气体没有刺激性气味
(3)
尚待检验的离子 检验方法
-
离子共存判断规律总结
1、因发生复分解反应而不能大量共存:(1)H?与OH(2)OH——、弱酸的酸式酸根离子不能大量共存;、NH?4与H?金属活动性顺序…
-
离子共存与离子反应方程式的书写判断规律总结
离子共存与离子反应方程式的书写判断0912下列离子方程式正确的是A向盐酸中滴加氨水HOHH2OBFeOH3溶于氢碘酸FeOH33H…
-
元素推断题常考知识点总结
1号元素氢原子半径最小同位素没有中子密度最小的气体6号元素碳形成化合物最多的元素单质有三种常见的同素异形体金刚石石墨富勒烯7号元素…
-
高中化学知识点总结离子反应
燕园教育教师培训手册四离子反应1电解质的概念11电解质与非电解质辨析并举例电解质在水溶液里或熔融状态下能够导电的化合物包括酸碱盐活…
-
高一化学必修一离子推断
离子推断1在FeCl3CuCl2混合溶液中加入一定量的铁屑反应完全后将固体滤出下列说法中正确的是22A若滤出的固体中只有铜则溶液中…
-
离子共存与离子反应方程式的书写判断规律总结
离子共存与离子反应方程式的书写判断(09)12.下列离子方程式正确的是A.向盐酸中滴加氨水:H++OH-=H2OB.Fe(OH)3…
-
离子共存判断规律总结
1、因发生复分解反应而不能大量共存:(1)H?与OH(2)OH——、弱酸的酸式酸根离子不能大量共存;、NH?4与H?金属活动性顺序…
-
高中化学-高一化学-元素推断题目总结
元素周期表练习题目1.X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别…
-
初中化学常见的几种题型总结 (除杂、分离、鉴别、鉴定、推断)
初中化学常见的几种题型总结除杂分离鉴别鉴定推断知识要点1除杂题解答除杂质一类的题目时要注意三原则三要领五种常用的方法三原则不引入新…
-
初中化学常见的几种题型总结 (除杂、分离、鉴别、鉴定、推断)
初中化学常见的几种题型总结除杂分离鉴别鉴定推断知识要点1除杂题解答除杂质一类的题目时要注意三原则三要领五种常用的方法三原则不引入新…