篇一 :离子共存判断规律总结
离子共存判断规律总结
1、因发生复分解反应而不能大量共存:
(1)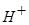 与
与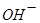 、弱酸的酸式酸根离子不能大量共存;
、弱酸的酸式酸根离子不能大量共存;
(2)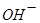 与
与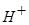 、
、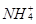 金属活动性顺序表中
金属活动性顺序表中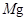 及
及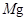 以后的金属离子、酸式酸根离子不能大量共存;
以后的金属离子、酸式酸根离子不能大量共存;
(3)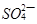 与
与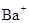 、
、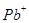 、
、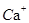 、
、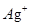 不能大量共存;
不能大量共存;
(4)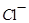 与
与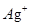 、
、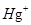 不能大量共存;
不能大量共存;
(5)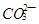 、
、 、
、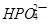 、
、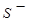 、
、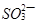 、
、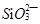 只能与
只能与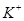 、
、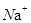 、
、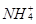 大量共存;
大量共存;
2、因发生氧化还原反应而不能大量共存:
(1)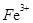 与
与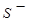 、
、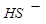 、
、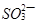 、
、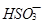 、
、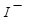 不能大量共存;
不能大量共存;
(2) 、
、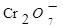 与
与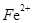 、
、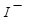 、
、 、
、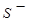 、
、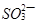 不能大量共存;
不能大量共存;
当 有
有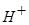 存在时,与
存在时,与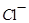 也不能大量共存;
也不能大量共存;
(3)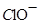 与
与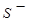 、
、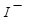 、
、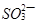 、
、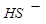 、
、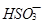 不能大量共存;
不能大量共存;
(4)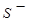 、
、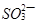 在有
在有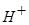 存在时,不能大量共存;
存在时,不能大量共存;
(5)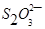 与
与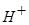 不能大量共存;
不能大量共存;
3、因生成络合物而不能大量共存:
(1)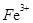 与
与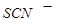 (硫氰根离子)不能大量共存;
(硫氰根离子)不能大量共存;
4、因发生双水解反应而不能大量共存:
(1)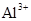 与
与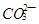 、
、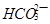 、
、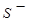 、
、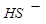 、
、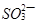 、
、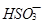 、
、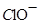 、
、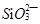 不能大量共存;
不能大量共存;
(2)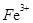 与
与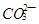 、
、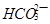 、
、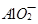 、
、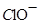 、
、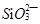 不能大量共存;
不能大量共存;
(3)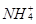 与
与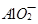 、
、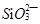 不能大量共存;
不能大量共存;
耿 艳 磊
…… …… 余下全文
篇二 :离子共存与离子反应方程式的书写判断规律总结
离子共存与离子反应方程式的书写判断
 (09) 12.下列离子方程式正确的是
(09) 12.下列离子方程式正确的是
 A. 向盐酸中滴加氨水:H+ + OH- = H2O
A. 向盐酸中滴加氨水:H+ + OH- = H2O
 B. Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B. Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
 C. 铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
C. 铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
 D. 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
D. 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
(10) 7.能在溶液中大量共存的一组离子是
A . 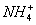 、
、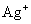 、
、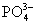 、
、 B.
B.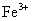 、
、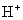 、
、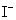 、
、 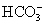
C.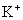 、
、 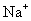 、
、 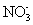 、
、 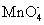 D.
D.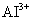 、
、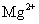 、
、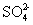 、
、 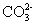
(11) 8. 能在水溶液中大量共存的一组离子是
A. H+、I―、NO3―、SiO32- B. Ag+、Fe3+、Cl―、SO42―
…… …… 余下全文
篇三 :元素推断题常考知识点总结
1号元素 氢:原子半径最小,同位素没有中子,密度最小的气体。
6号元素 碳:形成化合物最多的元素,单质有三种常见的同素异形体(金刚石、石墨、富勒烯)。
7号元素 氮:空气中含量最多的气体(78%),单质有惰性,化合时价态很多,化肥中的重要元素。
8号元素氧:地壳中含量最多的元素,空气中含量第二多的气体(21%)。生物体中含量最多的元素,与生命活动关系密切的元素,有两种气态的同素异形体。
9号元素 氟:除H外原子半径最小,无正价,不存在含氧酸,氧化性最强的单质。
11号元素 钠:短周期元素中原子半径最大,焰色反应为黄色。
12号元素 镁:烟火、照明弹中的成分,植物叶绿素中的元素。
13号元素铝:地壳中含量第三多的元素、含量最多的金属,两性的单质(既能与酸又能与碱反应),常温下遇强酸会钝化。
14号元素 硅:地壳中含量第二多的元素,半导体工业的支柱。
15号元素磷:有两种常见的同素异形体(白磷、红磷),制造火柴的原料(红磷)、化肥中的重要元素。
16号元素 硫:单质为淡黄色固体,能在火山口发现,制造黑火药的原料。
17号元素 氯:单质为黄绿色气体,海水中含量最多的元素,氯碱工业的产物之一。
…… …… 余下全文
篇四 :高中化学知识点总结离子反应
四、离子反应
1、电解质的概念
1.1 电解质与非电解质(辨析并举例)
电解质:在水溶液里或熔融状态下能够导电的化合物。包括酸、碱、盐活泼金属的氧化物某些非金属氢化物,某些有机物。
举例NaCl固体不导电,溶于水后可以导电,所以是电解质。CaSO4、BaSO4等难溶物质在水中溶解度很小,在熔融状态下可以导电,所以这些物质也是电解质。
非电解质:在水溶液里和熔融状态下不能够导电的化合物。包括大多数有机物非金属氧化物某些非金属氢化物等。
举例:CO2、SO3、NH3、蔗糖、酒精
注:我们讨论的电解质和非电解质都是化合物,单质或混合物既不是电解质也不是非电解质。
1.2 强电解质与弱电解质(辨析并举例)
强电解质: 在水溶液里或熔融状态下全部电离成离子的电解质。包括大多数盐类、强酸、强碱。在溶液中的粒子主要是离子。
弱电解质:在水溶液里部分电离成离子的电解质包括弱酸(如HAc、H2S)、中强酸(H3PO4)弱碱(如NH3·H2O)、水。
例题:CH3COOH极易溶于水,为什么它是弱电解质, Ca(OH)2微溶于水,为什么它是强电解质?
…… …… 余下全文
篇五 :高一化学必修一离子推断
离子推断
1.在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是
A.若滤出的固体中只有铜,则溶液中一定含有的阴离子是Fe2+,一定不含Cu2+
B.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含有Cu2+和Fe3+
D.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+
2.对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是
A Br- B SO42- C H2SO3 D NH4+
3.某澄清溶液,可能含有Ca2+、Na+、Cl-、CO32-、I-中的一种或几种,现做如下实验:①通入足量氯气,溶液变为棕黄色,滴加淀粉溶液后溶液显蓝色
②加入BaCl2有白色沉淀生成,再加入足量盐酸后,沉淀完全溶解,并有气体生成。
下列关于该澄清溶液的说法中错误的是
A、一定含有I- B、一定含有CO32-
C、可能含有Cl- D、一定含有Ca2+
4.某钠盐溶液中可能含有NO2-、SO42-、SO32-、CO32-、Cl-、I-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中仅含NO2-、CO32-、Cl-三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
5.今有一混合物的水溶液,含有以下离子中的若干种:Na+、NH+4、Cl—、Ba2+、HCO3—、SO42—,现取三份100mL该溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液,加热,收集到标准状况下的气体448mL
(3)第三份加足量Ba(OH)2溶液,得沉淀4.30g,再用足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,下列推测正确的是
A.Na+一定存在 B.100mL该溶液中含0.1mol HCO—3
C.Ba2+一定存在 D.Cl—一定不存在
6.A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
…… …… 余下全文
篇六 :济南中考化学推断总结
济南市推断题总结
一、加酸型
1.(7分)有一包固体混合物粉末,已知其中可能是(NH4)2CO3、Na2SO4、Fe2O3、CuO中的一种或几种。某研究小组为探究其成分,按下图所示进行实验,出现的现象如图所示(设过程中所有发生的反应都恰好完全反应)。
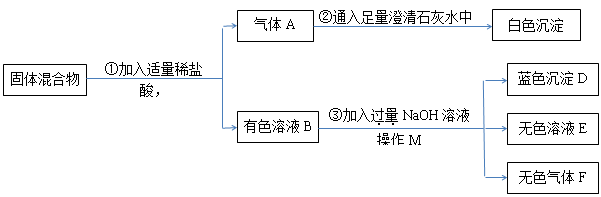
根据以上信息,回答下列问题:
(1)操作M的名称为 ,无色气体F的化学式为 。
(2)无色溶液E中一定含有的溶质的化学式是 。
…… …… 余下全文
篇七 :高中化学推断题知识点总结
高中化学推断题知识点总结
一. 基于元素周期表的推断
1. 元素的基本知识
解答这一类问题时,我们应该掌握一些有关元素的基本的特征性的常识。下面对标有红色字体的元素(单质)的基本特征性知识做一个总结。
1号元素 氢:原子半径最小,同位素没有中子,密度最小的气体。
6号元素 碳:形成化合物最多的元素,单质有三种常见的同素异形体(金刚石、石墨、富勒烯)。
7号元素 氮:空气中含量最多的气体(78%),单质有惰性,化合时价态很多,化肥中的重要元素。
8号元素氧:地壳中含量最多的元素,空气中含量第二多的气体(21%)。生物体中含量最多的元素,与生命活动关系密切的元素,有两种气态的同素异形体。
9号元素 氟:除H外原子半径最小,无正价,不存在含氧酸,氧化性最强的单质。
11号元素 钠:短周期元素中原子半径最大,焰色反应为黄色。
12号元素 镁:烟火、照明弹中的成分,植物叶绿素中的元素。
13号元素铝:地壳中含量第三多的元素、含量最多的金属,两性的单质(既能与酸又能与碱反应),常温下遇强酸会钝化。
14号元素 硅:地壳中含量第二多的元素,半导体工业的支柱。
15号元素磷:有两种常见的同素异形体(白磷、红磷),制造火柴的原料(红磷)、化肥中的重要元素。 16号元素 硫:单质为淡黄色固体,能在火山口发现,制造黑火药的原料。
…… …… 余下全文
篇八 :离子推断练习
竞赛专题
离子推断题
例1 中性溶液中含有k+、Fe3+、Cl—、SO42—四种离子,其中K+、Fe3+、Cl—三种离子的个数比为5∶2∶3。
则溶液中Fe3+与SO42—的个数比( )
A 1∶2 B 1∶3 C 2∶3 D 3∶5
例2 测得某溶液中仅含有Na+、Mg2+、SO42—、Cl—四种离子,其中Na+与Mg2+的个数比为4∶5,则Cl—和
SO42—个数比可能为( )
A 8∶3 B 3∶2 C 4∶1 D 2∶3
例3 在FeCl3和Fe2(SO4)3的混合溶液中,已知Fe3+与Cl—的个数比为4∶3,若溶液中Fe3+为4n个,则
硫酸根离子用n表示的个数为
+1 +6 -2 +1 +1
例4 在给定的H、 S、 O、 K、 Na五种元素中,最多可以组成 种化合物
例5 已知某无色溶液中可能含有H+、Ag+、Cu2+、Na+、OH—、Cl—、NO3—、CO32—等八种离子中的四种,
往该溶液中滴入几滴石蕊试液,石蕊试液变红,则原溶液中大量存在的离子可能为
或 。
例6 某溶液中可能含有Na+、H+、Cl—、SO42—欲证明两种阴离子确实存在,选用的最佳方案是:先向溶液
…… …… 余下全文