液相色谱实验报告英科新创
液相色谱分析混合样品中的抗原纯度
一、实验目的
1、掌握高效液相色谱定性和定量分析的原理及方法; 2、了解高效液相色谱的构造、原理及操作技术。
二、实验原理
高效液相色谱由储液器,泵、进样器、色谱柱、检测器、记录仪等几部分组成,储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动,经过反复多次的吸附—解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪。
三、主要仪器和试剂
主要仪器:岛津液相色谱仪(LC-10AT)[配有紫外检测器,Phenomenex ODS 柱]; 10μL微量注射器
试剂:苯标准溶液:10.0μL/mL ; 甲苯标准溶液:10.0μL/mL; 苯、甲苯混合标准溶液:10.0μL/mL ; 甲醇:80% ; 苯和甲苯混合待测溶液;
四、实验步骤
1、标准溶液的配制系列
用100μL的微量注射器分别量取10μL、20μL、 50μL 、100μL的苯和甲苯的混合标准溶液(10.0μL/mL),再分别加入90μL、80μL、50μL 、0μL甲醇将其稀释,作为待测液,其浓度分别为1μL/mL 、2μL/mL 、5μL/mL 、10μL/mL
2、色谱条件优化
①按操作规程开机,并调好色谱条件,使仪器处于工作状态。控制流动相流速为甲醇:0.8mL/min、水:0.2 mL/min;柱温30℃;检测波长254nm;观察记录保留时间,通过软件分析两峰分离效果。
②改变色谱条件,控制流动相流速为甲醇:0.95mL/min、水:0.05 mL/min;柱温30℃;检测波长254nm;观察记录保留时间,通过软件分析两峰分离效果。
③通过观察两种色谱条件下的峰分离效果,选择最佳的色谱条件。若还不能达到最佳的分离效果,可以再设定不同的色谱条件,然后根据峰分离效果,选择最佳的色谱条件。
3、苯、甲苯定性分析
在最佳条件下,待基线走稳后,用10μL微量注射器分别进样5μL苯和甲苯混合待测溶液,5μL苯标准溶液(10.0μL/mL)和5μL甲苯标准溶液(10.0μL/mL)(微量注射器用甲醇润洗3~5遍),观察并记录色谱图上显示的保留时间,确定苯和甲苯的峰。
4、苯、甲苯定量分析
最佳条件下,待基线走稳后,用10μL微量注射器分别进样1.0μL/mL 、2.0μL/mL、4.0μL/mL、10.0μL/mL的苯和甲苯混合标准溶液5μL。观察并记录各色谱图上的保留时间和峰面积。绘制苯和甲苯混合标准溶液峰面积与相应浓度的标准曲线。
5、苯和甲苯混合待测溶液分析
最佳条件下,待基线走稳后,用10μL微量注射器进样苯和甲苯混合待测液5μL,观察并记录各色谱图上的保留时间和峰面积。根据峰面积在工作曲线上查出苯和甲苯待测液的浓度,并计算试样中苯和甲苯的含量。
五、实验数据及分析
高效液相色谱数据报告
一、色谱条件优化




二、定性分析



三、 定量分析
苯、甲苯混合标准溶液浓度分别为:1 ul/ml, 2 ul/ml, 5 ul/ml, 10 ul/ml。





四、 未知样品浓度

六、 实验讨论
①由于实验中待测溶液的组分只有苯和甲苯两种物质,组分比较简单,只要在实验过程中,严格控制且定量进样,就能采用操作、计算简便的标准曲线法得出准确的实验结果,因而采用标准曲线法。若采用归一化法或内标法,虽然能得到准确更高的实验结果,但由于实验操作及计算均较为复杂,实验及数据处理的时间长,效率相对不高,故实验中采用标准曲线法作为定量的方法。
②最佳色谱条件的选择是本实验准确度的关键。若苯与甲苯的峰分离效果过小,苯与甲苯的峰未能完全分离,必定影响其保留时间和峰面积的计算,是实验准确度减小,数据误差加大;若苯与甲苯的峰分离效果过好,虽然能将苯与甲苯的峰完全分离,实验准确度好,但是耗费的实验时间较长,效率不好。因而,应选择合适的色谱条件。
③为了提高标准曲线的拟合度,可以重复进样多次,并且由同一人进样,以免因个体习惯不同引起实验误差。进样针进样时确保进样针中没有残留气泡,另外,在进不同浓度或不同的物质前因先用乙醇溶液润洗干净,以免相互影响。
第二篇:液相色谱实验报告
华南师范大学实验报告
液相色谱分析混合样品中的苯和甲苯
一、实验目的
1、掌握高效液相色谱定性和定量分析的原理及方法;
2、了解高效液相色谱的构造、原理及操作技术。
二、实验原理
高效液相色谱由储液器,泵、进样器、色谱柱、检测器、记录仪等几部分组成,储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动,经过反复多次的吸附—解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪。
三、主要仪器和试剂
主要仪器:岛津液相色谱仪(LC-10AT)[配有紫外检测器,Phenomenex ODS 柱]; 10μL微量注射器
试剂:苯标准溶液:10.0μL/mL ;
甲苯标准溶液:10.0μL/mL;
苯、甲苯混合标准溶液:10.0μL/mL ;
甲醇:80% ;
苯和甲苯混合待测溶液;
四、实验步骤
1、标准溶液的配制系列
用100μL的微量注射器分别量取10μL、20μL、 50μL 、100μL的苯和甲苯的混合标准溶液(10.0μL/mL),再分别加入90μL、80μL、50μL 、0μL甲醇将其稀释,作为待测液,其浓度分别为1μL/mL 、2μL/mL 、5μL/mL 、10μL/mL
2、色谱条件优化
①按操作规程开机,并调好色谱条件,使仪器处于工作状态。控制流动相流速为甲醇:0.8mL/min、水:0.2 mL/min;柱温30℃;检测波长254nm;观察记录保留时间,通过软件分析两峰分离效果。
②改变色谱条件,控制流动相流速为甲醇:0.95mL/min、水:0.05 mL/min;柱温30℃;检测波长254nm;观察记录保留时间,通过软件分析两峰分离效果。
③通过观察两种色谱条件下的峰分离效果,选择最佳的色谱条件。若还不能达到最佳的分离效果,可以再设定不同的色谱条件,然后根据峰分离效果,选择最佳的色谱条件。
3、苯、甲苯定性分析
在最佳条件下,待基线走稳后,用10μL微量注射器分别进样5μL苯和甲苯混合待测溶液,5μL苯标准溶液(10.0μL/mL)和5μL甲苯标准溶液(10.0μL/mL)(微量注射器用甲醇润洗3~5遍),观察并记录色谱图上显示的保留时间,确定苯和甲苯的峰。
4、苯、甲苯定量分析
最佳条件下,待基线走稳后,用10μL微量注射器分别进样1.0μL/mL 、2.0μL/mL、4.0μL/mL、10.0μL/mL的苯和甲苯混合标准溶液5μL。观察并记录各色谱图上的保留时间和峰面积。绘制苯和甲苯混合标准溶液峰面积与相应浓度的标准曲线。
5、苯和甲苯混合待测溶液分析
最佳条件下,待基线走稳后,用10μL微量注射器进样苯和甲苯混合待测液5μL,观察并记录各色谱图上的保留时间和峰面积。根据峰面积在工作曲线上查出苯和甲苯待测液的浓度,并计算试样中苯和甲苯的含量。
五、实验数据及分析
高效液相色谱数据报告
一、色谱条件优化

二、定性分析
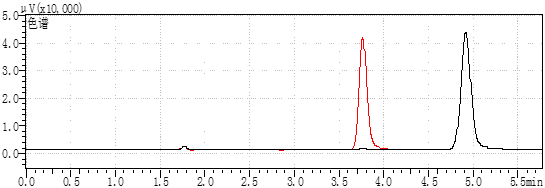

三、 定量分析
苯、甲苯混合标准溶液浓度分别为:1 ul/ml, 2 ul/ml, 5 ul/ml, 10 ul/ml。
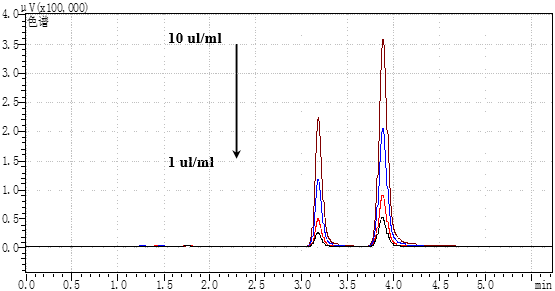
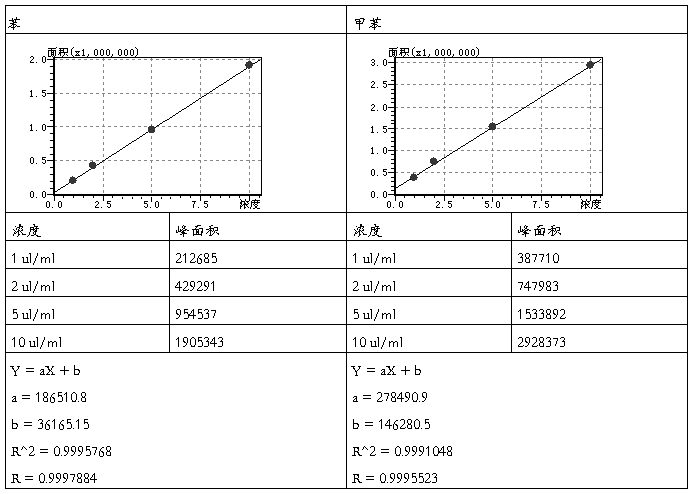
四、 未知样品浓度
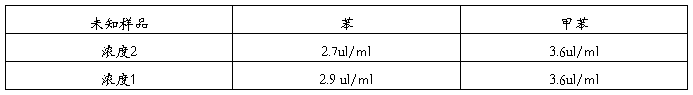
六、 实验讨论
①由于实验中待测溶液的组分只有苯和甲苯两种物质,组分比较简单,只要在实验过程中,严格控制且定量进样,就能采用操作、计算简便的标准曲线法得出准确的实验结果,因而采用标准曲线法。若采用归一化法或内标法,虽然能得到准确更高的实验结果,但由于实验操作及计算均较为复杂,实验及数据处理的时间长,效率相对不高,故实验中采用标准曲线法作为定量的方法。
②最佳色谱条件的选择是本实验准确度的关键。若苯与甲苯的峰分离效果过小,苯与甲苯的峰未能完全分离,必定影响其保留时间和峰面积的计算,是实验准确度减小,数据误差加大;若苯与甲苯的峰分离效果过好,虽然能将苯与甲苯的峰完全分离,实验准确度好,但是耗费的实验时间较长,效率不好。因而,应选择合适的色谱条件。
③为了提高标准曲线的拟合度,可以重复进样多次,并且由同一人进样,以免因个体习惯不同引起实验误差。进样针进样时确保进样针中没有残留气泡,另外,在进不同浓度或不同的物质前因先用乙醇溶液润洗干净,以免相互影响。
-
液相色谱实验报告
无标题报告用户名称System项目名称SS学生实验样品信息样品名称样品类型瓶号进样次数进样体积运行时间样品组名称样品未知17200…
-
分析实验报告 高效液相色谱
华南师范大学实验报告学号专业年级班级课程名称仪器分析实验实验项目液相色谱分析混合样品中的苯和甲苯实验时间一实验目的1掌握高效液相色…
-
高效液相色谱分析实验
实验学专班姓指导日仪器分析实验报告名称液相色谱分析实验院化学工程学院业化学工程与工艺级化工113班名号教师期20xx年5月6日一实…
-
高效液相色谱实验报告
高效液相色谱实验报告一实验目的1了解液相色谱的发展历史及最新进展2学习液相色谱的基本构造及原理3掌握液相色谱的操作方法和分析方法能…
-
高效液相色谱实验
实验1气相色谱分析条件的选择和色谱峰的定性鉴定一目的要求1了解气相色谱仪的基本结构工作原理与操作技术2学习选择气相色谱分析的最佳条…
-
研究生液相色谱实验报告
高效液相实验报告实验目的1.了解高效液相色谱仪的类型和各自的优缺点;2.了解液相色谱仪及各检测器的工作原理3.掌握高效液相色谱仪的…
-
分析实验报告 高效液相色谱
华南师范大学实验报告学号专业年级班级课程名称仪器分析实验实验项目液相色谱分析混合样品中的苯和甲苯实验时间一实验目的1掌握高效液相色…
-
液相色谱实验报告
仪器分析实验报告实习名称液相色谱分析实验学院专业化学工程与工艺班级化工班姓名学号指导教师日期一实验目的1了解液相色谱的构造原理及操…
-
液相色谱实验报告
华南师范大学实验报告液相色谱分析混合样品中的苯和甲苯一、实验目的1、掌握高效液相色谱定性和定量分析的原理及方法;2、了解高效液相色…
-
高效液相实验报告
化学与环境化学科学学院分析化学骆洪伟20xx4015016高效液相实验报告一实验目的1了解高效液相的实验原理2学习并掌握高效液相色…
-
气相色谱法实验报告
色谱与光谱实验实验五气相色谱法实验色谱与光谱实验色谱与光谱实验气相色谱法实验一实验目的1了解气相色谱仪的各部件的功能2加深理解气相…